Restaurarea metabolismului grăsimilor. Tulburarea metabolismului grăsimilor, tratament, simptome, remedii populare
Tulburările metabolismului lipidic pot apărea ca urmare a unor tulburări: 1) absorbția grăsimilor în intestin; 2) transferul de grăsime din sânge în țesut; 3) depunerea de grăsime: 4) interstițială metabolismul grăsimilor.
§ 198. Malabsorbţia grăsimii
Pentru absorbția grăsimilor alimentare din intestin, aceasta trebuie emulsionată, descompusă în glicerol și acid grasși formarea compușilor complecși cu acizi biliari - coleinați. Prin urmare, încetarea secreției biliare în duoden sau o scădere a secreției sale afectează imediat digestia grăsimilor. Blocarea căii biliare, inflamația vezicii biliare (colecistita) și unele afecțiuni hepatice asociate cu perturbarea procesului de secreție biliară duc la faptul că grăsimile neemulsionate trec prin canalul digestiv, fiind expuse doar în cantități limitate. într-o mare măsură hidroliză. Dacă hidroliza grăsimilor dietetice se realizează suficient sub acțiunea lipazelor sucurilor pancreatice și intestinale, atunci acizii grași rezultați încă nu sunt absorbiți. Același lucru se întâmplă cu scăderea sau încetarea completă a secreției enzimelor pancreatice, cu scăderea funcției epiteliului intestinal și cu scăderea semnificativă a peristaltism crescut intestinul subtire când grăsimea nu are timp să fie absorbită. Acest tip de tulburare de absorbție a grăsimilor se observă în enterită, hipovitaminoză A și B, din cauza unei perturbări în formarea enzimelor implicate în resinteza trigliceridelor din epiteliul intestinal.
Secreția de grăsime are loc în principal prin intestine și într-o măsură mai mică este realizată de sebacee și glandele sudoripare. În urină se găsesc doar urme de grăsime. Dacă există o malabsorbție a grăsimilor, fecalele conțin multă grăsime nedigerată și acizi grași mai mari și au o culoare caracteristică alb-cenușie - steatoreea. Excreția de grăsime prin urină - lipurie - poate apărea după ingerarea unor cantități foarte mari de grăsime cu alimente, cu fracturi ale oaselor lungi însoțite de zdrobire. măduvă osoasă, traumatisme pe zone mari de tesut adipos, cu nefroza lipoida.
Producția excesivă de grăsime glande sebacee- seboreea - apare in unele afectiuni ale pielii - acnee, eczeme, carente de vitamine etc.
Consecințele malabsorbției grăsimilor- deși grăsimile și lipidele sunt ușor de sintetizat în organism din produse intermediare ale metabolismului carbohidraților, excluderea completă a grăsimilor din alimente este inacceptabilă. Vitaminele vitale liposolubile (A, D, E, K) sunt introduse în organism cu grăsimi și, prin urmare, cu un aport insuficient de grăsimi din alimente, hipovitaminoza se poate dezvolta la oameni și animale. În plus, grăsimile naturale conțin întotdeauna cantități mici de acizi grași nesaturați esențiali (de exemplu, linoleic-C 18 H 32 O 2 și linolenic - C 18 H 30 O 2), care nu pot fi sintetizați în organism din alți acizi grași. În absența acestora în hrană, se dezvoltă animalele de experiment boli cronice piele (sub formă de focare necrotice). Aparent absență completă acizii grași superiori nesaturați din alimentele umane pot provoca, de asemenea, mai mult sau mai puțin tulburări grave schimb valutar.
§ 199. Încălcarea trecerii grăsimii de la sânge la țesut
Grăsimea neutră provenită din intestine circulă în sânge sub formă de chilomicroni (formate din trigliceride, esteri de colesteril, fosfolipide și β-lipoproteine) și α-lipoproteine. Conținutul normal de grăsimi neutre din sânge este de 1-2 g/l.
O creștere temporară tranzitorie a conținutului de chilomicroni din sânge - hiperlipemia - este observată cu un aport crescut de grăsimi din alimente ( hiperlipemia nutrițională). Hiperlipemia poate rezulta din mobilizarea crescută a grăsimii din depozit - hiperlipemia de transport(Fig. 35).
Mulți hormoni contribuie la mobilizarea grăsimilor din depozitele de grăsime, plămâni și măduva osoasă. De exemplu, în timpul postului, eliberarea grăsimii din depozitul său are loc ca urmare a acțiunii combinate a hormonului de creștere hipofizar, glucagon pancreatic și adrenalină. Efectul acestor hormoni asupra țesutului adipos se realizează prin sistemul adenil ciclază - tAMP. Acesta din urmă crește activitatea trigliceridei lipazei, care efectuează lipoliza în țesuturi.
Mobilizarea grăsimii din plămâni, care duce la hiperlipemie, apare în principal cu hiperventilația prelungită a plămânilor, de exemplu la cântăreții profesioniști.
Hiperlipemia de retenție(retenție - întârziere) - rezultatul unei întârzieri în trecerea grăsimilor neutre din sânge la țesuturi, apare în principal atunci când conținutul de albumină și factor de clearing (FP), o lipoprotein lipază specifică, scade în sânge. Sub influența FA, are loc descompunerea trigliceridelor asociate proteinelor și, prin urmare, „clarificarea” serului lipemic. Acizii grași liberi rezultați sunt legați de albumină (1 moleculă de albumină leagă 6-7 molecule de acizi grași), ceea ce favorizează transferul de grăsime în celule. Prin urmare, o lipsă de albumină în sânge (de exemplu, în timpul postului, boli de rinichi - nefroză) duce la hiperlipemie, precum și la niveluri insuficiente de FA și heparină. De exemplu, în ateroscleroză, hiperlipemia depinde de scăderea conținutului de heparină și de activitate scăzută a lipoprotein lipazei (LP). În diabet, o scădere a FP în sânge depinde de lipsa lipocainei.
§ 200. Acumularea excesivă de grăsime în țesutul adipos
Obezitatea este rezultatul dereglării pătrunderii grăsimilor în țesutul adipos, formării și utilizării acestuia ca sursă de energie.
Una dintre cauzele semnificative ale obezității este consumul excesiv de alimente (față de consumul de energie), asociat cu creșterea apetitului. Acesta din urmă se datorează, în special, excitabilității crescute a centrului alimentar formațiuni nervoase regiunea hipotalamica. S-a stabilit experimental că iritația nucleilor ventrolaterali ai hipotalamusului și distrugerea celor ventromediali determină lipsa de sațietate, creșterea apetitului, hiperfagie cu depunerea ulterioară de grăsime (așa-numita obezitate hipotalamică).
Analogul clinic al acestui tip de obezitate este obezitatea diencefalică, care se dezvoltă ca urmare a leziunilor infecțioase și toxice ale formațiunilor nervoase din creierul interstițial, precum și a tumorilor din această zonă.
O scădere a eliberării de grăsime din depozitul său are loc atunci când funcția este suprimată glanda tiroidași glanda pituitară, ai cărei hormoni (tiroxina, hormonul de creștere, TSH) activează mobilizarea grăsimii și oxidarea ulterioară a acesteia. Producția crescută de ACTH hipofizar, glucocorticoizi suprarenalii și insulină promovează depunerea grăsimilor și formarea acesteia din carbohidrați. Scăderea funcției gonadelor duce la depunerea excesivă de grăsime dacă este însoțită de perturbarea activității centrilor hipotalamici (vezi §§ 337, 338).
§ 201. Infiltrarea grasă a ficatului
Dacă grăsimea transportată de sânge către celule nu suferă descompunere și oxidare în ele, nu este excretată. perioadă lungă de timp rămâne în celule, apare infiltratie grasa(impregnare). Combinația sa cu o încălcare a structurii protoplasmatice se numește degenerare grasă.
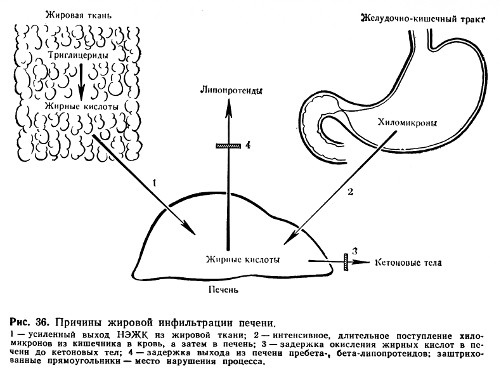
Cauza comună a infiltrației și degenerării grase este suprimarea activității enzimelor hidrolitice și oxidative ale metabolismului grăsimilor (Fig. 36), care poate fi observată în caz de otrăvire cu fosfor, arsen, cloroform, infecții virale, avitaminoza (alcoolism).
Mare importanțăîn patogeneza infiltrației hepatice grase este atribuită unei încălcări a formării fosfolipidelor. Conținutul lor suficient în ficat asigură o dispersie fină a grăsimii și, prin urmare, ieșirea acesteia din celulă. Molecula de fosfolipide catalizează oxidarea acizilor grași. Formarea insuficientă a fosfolipidelor are loc atunci când există o deficiență în corpul de colină, o parte structurală a principalului fosfolipide al ficatului - lecitina. Și sinteza colinei, la rândul său, este asociată cu grupări metil, al căror donator este aminoacidul metionina. Prin urmare, introducerea insuficientă a colinei alimentare în organism sau formarea insuficientă a acesteia din cauza lipsei de metionină poate duce la infiltrarea grasă a ficatului. Metionina, ca și proteina cazeină, care conține un numar mare de metionina, are efect lipotrop, adică ajută la eliminarea excesului de grăsime din ficat. Aceeași proprietate o deține și factorul lipotrop endogen - lipocaina (formată în epiteliul canalelor mici ale pancreasului). Lipsa lipocainei în diabetul zaharat favorizează infiltrarea grasă a ficatului.
§ 202. Tulburări ale metabolismului intermediar al grăsimilor
Produșii relativ stabili ai metabolismului interstițial al acizilor grași superiori sunt acetona, acizii acetoacetic și beta-hidroxibutiric, așa-numiții corpi cetonici sau acetonici, formați în principal în ficat și oxidați la CO2 și H2O în alte țesuturi și organe (mușchi). , plămâni, rinichi etc.). În unele procese și boli patologice (diabet zaharat, post - complet sau exclusiv carbohidrați, infecții pe termen lung cu temperatura ridicata, hipoxie, boli ale parenchimului hepatic etc.), conținutul de corpi acetonici din sânge poate crește brusc (în mod normal conținutul acestora nu depășește 0,02-0,04 g/l) (2-4 mg%). Acetonemia duce la apariția corpilor cetonici și acetonici în urină - aceturie. Acetona este excretată nu numai prin rinichi, ci și prin plămâni cu gazele expirate și transpirația. Pacientul miroase a acetonă.
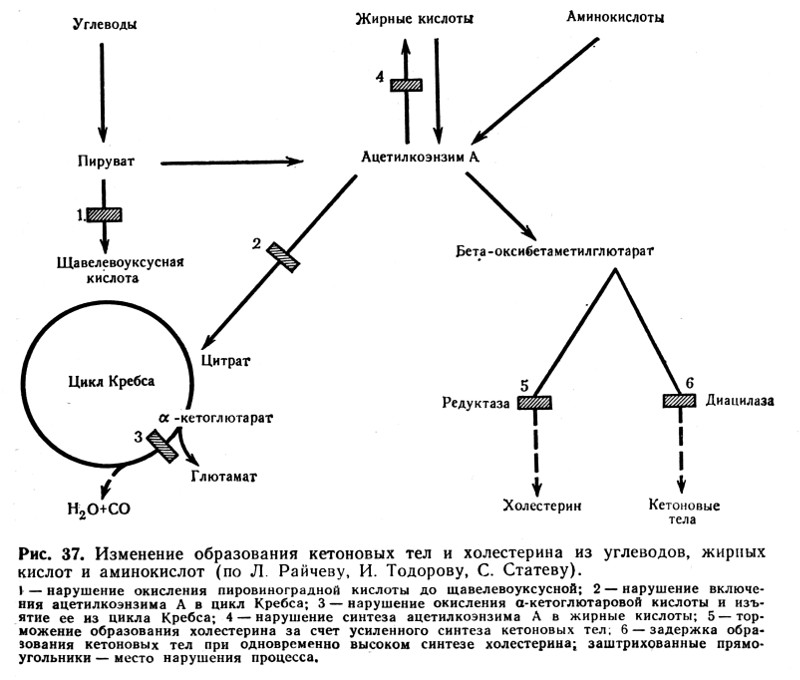
Mecanisme care conduc la o creștere corpi cetoniciîn sânge (cetoza) sunt destul de complexe.
- Unul dintre principalele motive pentru dezvoltarea cetozei este deficiența de carbohidrați (de exemplu, în diabetul zaharat, post), care duce la epuizarea ficatului în glicogen și creșterea pătrunderii grăsimilor în acesta, unde oxidarea acizilor grași la apare acidul acetoacetic. Acest lucru este facilitat și de resinteza insuficientă a acizilor grași superiori din corpii cetonici și de o încălcare a oxidării acestora în ciclul tricarboxilic (citric). Resinteza necesită energie din glicoliză. Oxidarea insuficientă a corpilor cetonici este asociată și cu o deficiență a compușilor formați în timpul metabolismului glucidic intermediar (acizi piruvic și oxaloacetic) și care sunt substraturi ale ciclului acidului tricarboxilic (Fig. 37).
- O legătură patogenetică importantă în dezvoltarea cetozei în diabetul zaharat este deficitul simultan de lipocaină și insulină.
- Cu leziuni hepatice cauzate de factori toxine-infecțioși, funcția de formare a glicogenului a ficatului este afectată, ceea ce favorizează transferul acizilor grași către ficat. Aici, formarea corpurilor cetonici prevalează în mare măsură asupra oxidării lor. Rezultatul este cetoza și ficatul gras.
§ 203. Tulburări ale metabolismului fosfolipidelor
Tulburările metabolismului fosfolipidelor (lecitine, cefaline) sunt strâns legate de metabolismul grăsimilor. Astfel, cu lipemie, nivelul de lecitină din sânge crește.
Există unele stări patologice determinate ereditar asociate cu depunerea excesivă de fosfolipide în țesuturi. De exemplu, în boala Gaucher, cerebrozidele sunt depuse în celulele macrofage ale splinei, ficatului, noduli limfatici si maduva osoasa. În boala Niemann-Pick în celule diverse organe se observă depunerea de sfingomielin fosfatid. Amaurotic (din grecescul amauros - întunecat, orb) idioția familială este rezultatul depunerii de lipoide în celule nervoase, care este însoțită de atrofie a nervului optic și demență.
§ 204. Tulburări ale metabolismului colesterolului. Ateroscleroza
Tulburările metabolismului colesterolului stau la baza dezvoltării aterosclerozei, colelitiaza, nefroza lipoidă, opacificarea corneei legată de vârstă, xantomatoza pielii, oaselor și alte boli.
Fiziopatologii ruși N.P. Anichkov și S.S. Khalatov au jucat un rol major în studiul tulburărilor metabolismului colesterolului. În 1911-1912. Ei au creat un model experimental de ateroscleroză prin hrănirea animalelor cu colesterol. Deși în patogenia aterosclerozei umane importanța colesterolului exogen (din alimente) nu este atât de semnificativă, faptul unei tulburări în metabolismul colesterolului este fără îndoială.
În condiții fiziologice, conținutul de colesterol din sângele unui adult este de aproximativ 1,8-2,3 g/l. O anumită creștere a nivelului de colesterol din sânge poate apărea după consumul de alimente bogate în colesterol ( gălbenuș de ou, creier, ficat, unt etc.), dar această hipercolesterolemie nutrițională la om trece rapid, deoarece cu un exces de colesterol din mastocitele Heparina este eliberată în sânge, activând lipoprotein lipaza, așa-numitul „factor de curățare” (FP). Acesta din urmă transformă lipidele cu moleculare mari, cu densitate scăzută, în unele fin dispersate, care sunt ușor de îndepărtat din sânge.
Modificările în metabolismul colesterolului pot fi rezultatul defectării sintezei colesterolului, ceea ce duce la hipercolesterolemie endogenă. Sinteza colesterolului este reglată în primul rând de aportul său din intestine: un aport mic activează sinteza colesterolului. Materialul de plecare pentru sinteza colesterolului este, pe lângă acidul acetoacetic, aminoacizii valină și leucină, acizii grași, carbohidrații, care în procesul de metabolism interstițial sunt transformați în acetil coenzima A. Acesta din urmă este inclus în beta- ciclul hidroxi-beta-metil-glutaril coenzima A și contribuie la dezvoltarea hipercolesterolemiei.
Un factor important în metabolismul colesterolului este activitatea enzimelor tisulare care asigură descompunerea lipidelor. Astfel, s-a dovedit că atunci când stări patologice, predispunând la ateroscleroză (diabet, stres, hipoxie), activitatea lipolitică a peretelui aortic este semnificativ redusă, iar conținutul de colesterol din acesta crește brusc. Peretele aortic al oamenilor sănătoși conține 5-50 mg colesterol, în aorta ateromatoasă - 240 mg, cu forme severe ateromatoza, continutul de colesterol din aorta poate ajunge la 500-1000 mg.
Cauza hipercolesterolemiei poate fi și o modificare a stării fizico-chimice a proteinelor din sânge, datorită căreia se formează o legătură mai puternică între colesterol și β-lipoproteine și eliberarea colesterolului din complex este dificilă sau, dimpotrivă, proteina β. complexul este rupt și dispersia micelilor de colesterol scade. În ambele cazuri, colesterolul este reținut în sânge.
În încălcarea metabolismului colesterolului, este importantă pierderea funcției tiroidei, gonadelor și glandelor suprarenale. Ce părți ale metabolismului colesterolului sunt modificate de fiecare dintre acești hormoni este o întrebare foarte complexă. Ele pot modifica rata de transfer al colesterolului în și din celulă, pot influența distribuția fracțiilor sale între plasma sanguină și lichidul interstițial și procesele de sinteza și descompunerea colesterolului.
Cea mai importantă manifestare a tulburărilor metabolismului colesterolului în corpul uman este ateroscleroza.
Lipidele- eterogen în compoziție chimică materie organică, insolubil în apă, dar solubil în solvenți nepolari.
Formele tipice de patologie a metabolismului lipidic sunt obezitatea, epuizarea, lipodistrofia, lipidoza și dislipoproteinemia.
Obezitatea
Obezitatea- acumulare în exces lipidele din organism sub formă de trigliceride.
TIPURI DE OBEZITATE
În funcție de gradul de creștere în greutate Există trei grade de obezitate.
Sunt folosite diverse formule pentru a estima greutatea corporală optimă.
♦ Cel mai simplu este indicele Broca: din indicatorul de înălțime se scade 100 (în cm).
♦ Indicele de masă corporală (IMC) se calculează și folosind următoarea formulă:
În funcție de valoarea indicelui de masă corporală, se vorbește despre normal sau suprapondere de 3 grade (Tabelul 10-1).
După localizarea predominantă a țesutului adipos distinge între obezitatea generală (uniformă) și cea locală (lipohipertrofie locală). Există două tipuri de obezitate locală.
♦ Tip feminin(gynoid) - excesul de grăsime subcutanată în principal în șolduri și fese.
Tabelul 10-1. Nivelurile de obezitate
 ♦ Tip masculin(android sau abdominal) - acumulare de grăsime în principal în zona abdominală.
♦ Tip masculin(android sau abdominal) - acumulare de grăsime în principal în zona abdominală.
Prin geneză Există obezitatea primară și formele ei secundare.
♦ Obezitatea primară (hipotalamică) este o boală independentă de origine neuroendocrină, cauzată de o tulburare a sistemului de reglare a metabolismului grăsimilor.
♦ Obezitatea secundară (simptomatică) este o consecință diverse încălcăriîn organism, determinând o scădere a lipolizei și activarea lipogenezei (de exemplu, în diabet, hipotiroidism, hipercortizolism).
ETIOLOGIE
Cauza obezității primare este o disfuncție a sistemului hipotalamus-adipocite.
Obezitatea secundară se dezvoltă din cauza excesului de calorii și nivel redus consumul de energie al organismului (în special în timpul inactivității fizice).
PATOGENEZA OBEZITATII
Există mecanisme neurogenice, endocrine și metabolice ale obezității.
Variante neurogenice ale obezității
Centrogen mecanism (cortical, psihogen) - una dintre variantele tulburării de alimentație (celelalte două: anorexia nervoasă și bulimia).
♦ Cauză: diverse tulburări psihice, manifestate printr-o dorință constantă, uneori irezistibilă de a mânca.
♦ Mecanisme posibile:
❖ activarea sistemelor serotoninergice, opioidergice și a altor sisteme implicate în formarea sentimentelor de plăcere și confort;
❖ percepția alimentelor ca un stimul puternic pozitiv (dopaj), care activează și mai mult aceste sisteme. Acest
inchide cercul vicios al mecanismului centrogen de dezvoltare a obezitatii.
Hipotalamic mecanism (diencefalic, subcortical).
♦ Cauză: afectarea neuronilor hipotalamici (de exemplu, după o comoție, encefalită, craniofaringiom, metastaze ale tumorilor la hipotalamus).
♦ Cele mai importante verigi în patogeneză:
❖ Deteriorarea sau iritația neuronilor din nucleul ventral posterolateral al hipotalamusului stimulează sinteza și secreția neuropeptidei Y și reduce sensibilitatea la leptină, care inhibă sinteza neuropeptidei Y. Neuropeptida Y stimulează foamea și crește pofta de mâncare.
❖ Formarea afectată a senzației de foame din cauza producției excesive de neurotransmițători care formează senzația de foame și cresc pofta de mâncare (GABA, dopamină, β-endorfină, encefaline). Aceasta duce la o scădere a sintezei neurotransmițătorilor care creează senzația de sațietate și inhibă comportamentul alimentar (serotonina, norepinefrina, colecistokinina, somatostatina).
Variante endocrine ale obezității
Mecanismele endocrine ale obezitatii sunt leptina, hipotiroida, suprarenala si insulina.
Mecanismul leptinei- conducând în dezvoltarea obezității primare.
♦ leptina formate în celulele adipoase. Reduce pofta de mancare si creste consumul de energie al organismului. Leptina suprimă formarea și eliberarea neuropeptidei Y de către hipotalamus.
♦ Neuropeptida Y participă la formarea foamei. Crește pofta de mâncare și reduce consumul de energie al organismului.
♦ Lipostat. Circuitul leptină-neuropeptidă Y asigură menținerea masei de grăsime corporală cu participarea insulinei, catecolaminelor, serotoninei, colecistochininei și endorfinelor. În general, acest sistem de substanțe biologic active, care asigură homeostazia dinamică a metabolismului energetic și a masei de țesut adipos din organism, se numește sistem lipostat.
Mecanismul hipotiroidian obezitatea este activată atunci când efectele hormonilor tiroidieni care conțin iod sunt insuficiente, ceea ce reduce intensitatea lipolizei, rata proceselor metabolice în țesuturi și costurile energetice ale organismului.
suprarenale(glucocorticoizi, cortizol) mecanism obezitatea este activată din cauza hiperproducției de glucocorticoizi în cortexul suprarenal (de exemplu, în boli și sindrom
Itsenko-Cushing), care promovează lipogeneza datorită hiperglicemiei și activării mecanismului insulinei.
Mecanismul insulinei Dezvoltarea obezității se dezvoltă ca urmare a activării directe a lipogenezei în țesutul adipos de către insulină.
Mecanismele metabolice ale obezității. Rezervele de carbohidrați din organism sunt relativ mici. În acest sens, a fost dezvoltat un mecanism de economisire a carbohidraților: odată cu creșterea proporției de grăsimi din dietă, rata de oxidare a carbohidraților scade. Când sistemul de reglare este perturbat, este activat un mecanism care crește apetitul și aportul de alimente. În aceste condiții, grăsimile nu se descompun și se acumulează sub formă de trigliceride.
Epuizare
Epuizare- declin patologic masa grasa, precum si musculara si țesut conjunctiv sub normal. Gradul extrem epuizarea este cașexie.
Cu epuizare, deficitul de țesut adipos este mai mare de 20-25%, iar cu cașexie - mai mult de 50%. IMC pentru epuizare este mai mic de 19,5 kg/m2.
ETIOLOGIE
Depleția poate fi cauzată de motive endogene și exogene.
Cauze exogene:
♦ Postul complet sau parțial forțat sau conștient.
♦ Conținut caloric insuficient al alimentelor.
Cauzele endogene ale epuizării sunt împărțite în primare și secundare.
♦ Cauza epuizării primare: suprimarea sintezei neuropeptidei Y în hipotalamus (cu traumatism sau ischemie a hipotalamusului, stres sever prelungit) și hiposensibilizarea celulelor țintă la neuropeptida Y.
♦ Cauze ale epuizării secundare (simptomatice): malabsorbție, deficit de glucocorticoizi, hipoinsulinism, creșterea sintezei de glucagon și somatostatine, supraproducție de TNFα de către celulele tumorale.
PATOGENEZĂ
Risipirea exogenă și cașexia. Absența sau deficiența semnificativă a alimentelor duce la epuizarea rezervelor de grăsime, la perturbarea tuturor tipurilor de metabolism, la insuficiența oxidării biologice și la suprimarea proceselor plastice.
Forme endogene primare de risipire
Cel mai grozav semnificație clinică au forme hipotalamice, cahectice si anorectice.
În forma hipotalamică (diencefalică, subcorticală) de epuizare și cașexie, are loc scăderea sau încetarea sintezei și eliberarea peptidei Y în sânge de către neuronii hipotalamici, ceea ce perturbă lipostatul.
În forma de epuizare a cachectinei (sau citokinei), sinteza TNFa (cachectinei) de către adipocite și macrofage duce la suprimarea sintezei neuropeptidei Y în hipotalamus, inhibarea lipogenezei și activarea catabolismului lipidic.
Forma anorexica.
♦ La persoanele cu predispoziție la anorexie, o atitudine critică față de greutatea lor corporală (percepută ca excesivă) duce la dezvoltarea tulburărilor neuropsihiatrice și perioade lungi refuzul de a mânca. Se observă cel mai adesea la adolescente și la fetele sub 18 ani.
♦ Derularea ulterioară a procesului este asociată cu o scădere a sintezei neuropeptidei Y și o scădere semnificativă a greutății corporale, până la cașexie.
Forme endogene secundare epuizarea și cașexia sunt simptome ale altor forme de patologie: sindroame de malabsorbție, creșterea neoplasmelor (sintetizarea TNF), hipoinsulinism, hipocortisolism, lipsa efectelor hormonilor timusului.
Lipodistrofii și lipidoze
Lipodistrofie- afecțiuni caracterizate prin pierderea generalizată sau locală a țesutului adipos, mai rar - acumularea excesivă a acestuia în țesutul subcutanat.
Lipidoze- afecțiuni caracterizate prin tulburări ale metabolismului lipidic în celule (lipidoze parenchimatoase), țesuturi adipoase (obezitate, epuizare) sau pereți vasele arteriale(de exemplu, cu ateroscleroză).
Dislipoproteinemie
Dislipoproteinemie- condiții caracterizate prin abateri de la normă în conținutul, structura și raportul diferitelor medicamente din sânge.
Natura curentului şi manifestari clinice dislipoproteinemia este determinată de:
♦ caracteristici genetice organism (de exemplu, compoziția, raportul și nivelul diferitelor medicamente);
♦ factori Mediul extern(de exemplu, un set de produse alimentare, caracteristici dietetice și modele de alimentație);
♦ disponibilitate boli concomitente(de exemplu, obezitate, hipotiroidism, diabet, leziuni renale și hepatice).
Aterogenitatea lipoproteinelor
LP-urile sunt împărțite în aterogene (VLDL, LDL și LPPP) și antiaterogene (HDL).
Potențiala aterogenitate a lipidelor din sânge este evaluată prin calcularea coeficientului de aterogenitate a colesterolului:
colesterol total - colesterol HDL
HDL colesterol
În mod normal, coeficientul aterogen al colesterolului nu depășește 3,0. Pe măsură ce această valoare crește, crește riscul de a dezvolta ateroscleroză.
TIPURI DE DISLIPOPROTEINEMIE
După origine: primare (ereditare; pot fi monogenice și poligenice) și secundare.
În funcție de modificările conținutului de lipoproteine din sânge: hiperlipoproteinemie, hipo- și alipoproteinemie, dislipoproteinemie combinată.
Diverse boli, de obicei cronice, pot duce la dezvoltarea dislipoproteinemiei secundare (Tabelul 10-2).
Tabelul 10-2. Boli care duc la dezvoltarea dislipoproteinemiei secundare
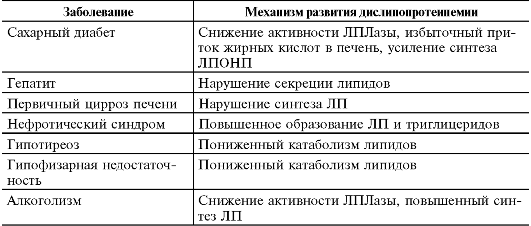 Hiperlipoproteinemie
Hiperlipoproteinemie
Hiperlipoproteinemie- afecțiuni manifestate printr-o creștere persistentă a conținutului de medicamente în plasma sanguină.
În 1967, Fredrickson și colab. a dezvoltat o clasificare a hiperlipoproteinemiei. Această clasificare a fost revizuită ulterior de specialiștii OMS (Tabelul 10-3).
Tabelul 10-3. Tipuri de hiperlipoproteinemie și conținutul diferitelor lipoproteine cu acestea
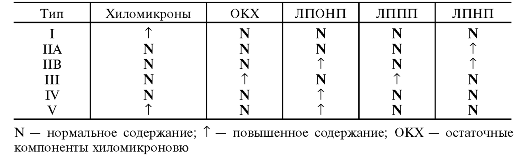 Hipoproteinemie
Hipoproteinemie
Hipoproteinemie- afectiuni manifestate printr-o scadere persistenta a nivelului de medicamente in plasma sanguina pana la absenta completa a acestora (alipoproteinemie).
Dislipoproteinemie combinată sunt caracterizate de o încălcare a raportului dintre diferitele fracții de medicament.
Ateroscleroza
Ateroscleroza- un proces patologic cronic care duce la modificări în principal în mucoasa interioară a arterelor de tip elastic și musculo-elastic datorită acumulării de exces de lipide, formarea țesut fibros, precum și un set de alte modificări ale acestora.
În ateroscleroză, arterele cel mai frecvent afectate sunt arterele coronare, carotide, renale, mezenterice, membrele inferioare, precum și aorta abdominală.
ETIOLOGIE
Cauze ateroscleroza nu a fost pe deplin elucidată. Există trei ipoteze care explică apariția aterosclerozei: lipidic, lezarea endotelială cronică și monoclonală.
Factori de risc. Sunt cunoscuți cel puțin 250 de factori care contribuie la apariția și dezvoltarea aterosclerozei. Cei mai semnificativi factori de risc includ fumatul, diabetul, hipertensiune arteriala, obezitate, boli autoimune, hipercolesterolemie, hipertrigliceridemie, hiperhomocisteinemie, inactivitate fizică, predispoziție ereditară, luarea de contraceptive orale.
PATOGENEZĂ
A evidentia etapele următoare afectarea vasculară aterosclerotică: pete și dungi lipidice, formare de aterom și fibroaterom, dezvoltarea complicațiilor (Fig. 10-1).
Pete și dungi lipidice
Endoteliul intact previne patrunderea medicamentelor in intima arterelor. Sub influența factorilor de risc, celulele endoteliale sunt deteriorate și se dezvoltă disfuncție endotelială- factor declanșator aterogeneza.
Formarea petelor și dungilor lipidice are loc în mai multe etape:
♦ Migrații în zonele intimale ale arterelor cu celule endoteliale deteriorate un numar mare monocite și limfocite T.
♦ Sinteza de către leucocite a substanțelor biologic active (factori de chimiotaxie, kinine, Pg, TNFa) și a speciilor reactive de oxigen, care este însoțită de intensificarea peroxidării lipidelor. Acești factori potențează afectarea endotelială și pătrunderea medicamentelor în intima vasculară.
♦ Activarea suplimentară a peroxidării LDL care pătrunde în stratul subendotelial cu formarea LP modificată.
♦ Captarea medicamentelor modificate de către monocite folosind „receptori scavenger” (receptori scavenger) și transformarea lor în celule de spumă- macrofage bogate în lipide.
♦ Activarea limfocitelor T și a macrofagelor la locul afectarii peretelui arterei cu dezvoltarea inflamației aseptice.
♦ Proliferarea SMC-urilor și fibroblastelor și sinteza acestora a componentelor țesutului conjunctiv cu formarea de pete și dungi lipidice în intimă.
Formarea de aterom și fibroaterom
Formarea unei plăci aterosclerotice este cauzată de mai mulți factori:
Deteriorări suplimentare ale endoteliului mediatori ai inflamației, care potențează pătrunderea LDL în intima vasculară și închiderea unui cerc vicios.
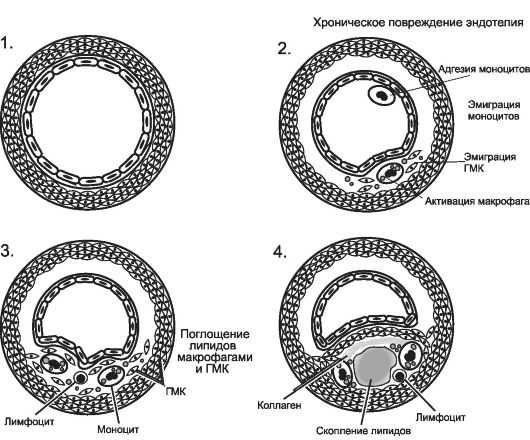 Orez. 10-1.
Modificări consecutive ale peretelui arterial deteriorat în ateroscleroză. 1 - peretele normal al arterei; 2 - aderența monocitelor și a trombocitelor la endoteliul deteriorat; 3 - migrarea monocitelor și SMC-urilor în intima, infiltrarea lipidelor; 4 - proliferarea elementelor celulare, formarea unui nucleu lipidic și formarea fibroateromului. [până la 4].
Orez. 10-1.
Modificări consecutive ale peretelui arterial deteriorat în ateroscleroză. 1 - peretele normal al arterei; 2 - aderența monocitelor și a trombocitelor la endoteliul deteriorat; 3 - migrarea monocitelor și SMC-urilor în intima, infiltrarea lipidelor; 4 - proliferarea elementelor celulare, formarea unui nucleu lipidic și formarea fibroateromului. [până la 4].
Transformare SMC în macrofage și activarea sintezei de către acestea și fibroblaste a componentelor substanței intercelulare ale țesutului conjunctiv (proteoglicani, glicozaminoglicani, colagen și fibre elastice).
Formarea miezului lipidic aterom datorită morții celulelor spumoase și eliberării de lipide libere din acestea.
♦ Aterom caracterizat prin prezența unui număr semnificativ de elemente celulare: celule de spumă, SMC-uri pe diferite etape proliferare și transformare, limfocite, granulocite, trombocite; formarea unui miez lipidic cu o cantitate mare de colesterol liber și esterii săi.
♦ Fibroaterom caracterizată prin formarea unui capac fibros peste miezul lipidic datorită sintezei componentelor țesutului conjunctiv și dezvoltării unei rețele de vase nou formate care pătrund în placă.
Dezvoltarea complicațiilor aterosclerozei
Modificare plăci de ateroscleroză conduce la dezvoltarea următoarelor procese:
♦ calcificări, aterocalcinoză - acumulare de compuși de calciu în țesutul plăcii;
♦ fisuri în învelișul fibroateromului sau ulcerațiile acestuia, care sunt însoțite de dezvoltarea unui tromb parietal cu amenințarea obstrucției arterelor sau emboliei;
♦ rupturi ale pereților microvaselor nou formate, ducând la hemoragii în peretele arterial, formarea de trombi parietali și intramurali.
Din punct de vedere clinic, complicațiile aterosclerozei se manifestă cel mai adesea ca ischemie și infarct al organelor și țesuturilor alimentate cu sânge din artera afectată.
PRINCIPII DE PREVENIRE ȘI TERAPIE A ATEROSCLEROZEI
Etiotrop. Scopul este de a elimina sau reduce efectul factorilor de risc. Exemple de măsuri: utilizarea medicamentelor hipolipemiante, corectarea tensiunii arteriale, renunțarea la fumat, aderarea la o anumită dietă.
Patogenetic. Menit să rupă „lanțul aterogenezei”. Exemple de impact: utilizarea de agenți antiplachetari și anticoagulante; utilizarea unor medicamente specifice care reduc inflamația în aterom (de exemplu, statine sau anticorpi monoclonali la TNF și alte citokine proinflamatorii).
Termenul „metabolism” înseamnă totul reacții chimice care apar în organism. Viața fără ele corpul uman devine imposibil, deoarece numai datorită unor astfel de procese există celule: cresc, contactează cu lumea exterioară, se hrănesc și se curăță. Există destul de multe tipuri de metabolism; la ele iau parte proteinele, grăsimile și aminoacizii. Și, în unele cazuri, cursul unor astfel de procese poate fi perturbat, ceea ce necesită o corecție adecvată. Să vorbim pe www.site-ul despre ce este o tulburare a metabolismului grăsimilor, luați în considerare tratamentul și simptomele acesteia, precum și remedii populare care va ajuta la rezolvarea acestei probleme.
Termenul „metabolismul grăsimilor” se referă la producerea și descompunerea grăsimilor (lipide) în organism. Procesele de descompunere a grăsimilor se desfășoară mai ales în ficat, precum și în țesutul adipos. Și eșecuri în metabolism normal lipidele pot provoca dezvoltarea aterosclerozei, a obezității, precum și a diferitelor boli endocrine (de exemplu, diabetul). După cum se știe, metabolismul grăsimilor se caracterizează printr-o reglare deosebit de complexă. Este influențată de insulină, hormoni sexuali, precum și de adrenalină, tiroxina și alți hormoni.
Despre cum se manifestă tulburarea metabolismului lipidic, ce simptome indică boala
Metabolismul grăsimilor are loc în aproape toate celulele și țesuturile corpului. Din acest motiv, simptomele tulburărilor sale sunt greu de localizat și sunt greu de împărțit în primare sau secundare.
Cel mai elementar și mai vizibil semn al tulburării este o creștere vizibilă a volumului de grăsime subcutanată, care este principalul depozit de grăsime din organism. În cazul în care procesul unei astfel de acumulări are loc cu o intensitate deosebită, medicii ridică problema obezității și o consideră o boală independentă. Obezitatea însăși se face simțită în apropiere simptome neplăcute. O astfel de încălcare provoacă o scădere capacitati fizice, provoacă dificultăți de respirație, sforăit etc. Pacienții cu această problemă experimentează foame constantă, pentru că au crescut țesut adipos necesită hrană.
Obezitatea poate provoca boli de inima, apnee in somn, infertilitate si diabet.
Încălcarea metabolismului grăsimilor în organism este însoțită de acumularea de grăsime nu numai în țesutul subcutanat, ci și în sânge. Ca urmare a unui astfel de procese patologice o persoană dezvoltă hiperlipidemie. În acest caz, testele de sânge ale pacientului arată o creștere a concentrației de colesterol, a nivelului de trigliceride și a lipoproteinelor cu densitate scăzută în plasmă.
Sângele gras este la fel de periculos ca și acumularea de grăsimi sub piele. Când cantitatea de lipide din sânge crește, particulele lor pătrund activ în pereții arterelor. Ele sunt apoi depuse pe suprafața vaselor, dând astfel naștere la plăci de ateroscleroză. Astfel de formațiuni cresc treptat și pot provoca blocarea lumenului vaselor de sânge. În anumite cazuri, pacientul poate experimenta o oprire completă a fluxului sanguin - un atac de cord sau un accident vascular cerebral.
Este de remarcat faptul că, uneori, o încălcare a metabolismului grăsimilor se manifestă printr-o lipsă de lipide. În acest caz, pacientul începe să devină epuizat și are o lipsă de vitamine liposolubile A, D, E și K. Apare și o defecțiune ciclu menstrualȘi funcțiile de reproducere. În plus, deficitul de lipide provoacă o lipsă de acizi grași nesaturați esențiali, care se face simțită prin căderea părului, eczeme, leziuni inflamatorii afectarea pielii și a rinichilor.
Despre cum se corectează tulburările de metabolism al grăsimilor, ce tratament ajută
Pacienții cu tulburări metabolice sunt sfătuiți să elimine factorii de risc; în plus, au nevoie alimente dietetice. Uneori, doar aceste mijloace de corecție conservatoare sunt suficiente pentru a optimiza starea pacientului. Cu toate acestea, o persoană cu o tulburare procesele metabolice Cel mai adesea, trebuie să respectați restricțiile alimentare pe tot parcursul vieții.
Meniul pentru astfel de pacienți ar trebui să includă cantitate semnificativă legume, fructe, precum și cereale și produse lactate cu conținut scăzut de grăsimi. Exercițiu fizic sunt selectați individual, în plus, pacienții trebuie să renunțe la fumat, la consumul de alcool și să se protejeze de stres.
Dacă asemenea măsuri nu dau efect pozitiv, medicii se conectează terapie medicamentoasă. În acest caz, se pot utiliza statine, un acid nicotinic iar derivații săi, fibrații, antioxidanții și sechestranții sunt uneori medicamentele de alegere acizi biliari. Medicamentele pot fi selectate numai de către un medic, precum și doza lor.
Tratamentul tulburărilor de metabolism al grăsimilor cu remedii populare
Medicamentele pe bază de plante pot fi utilizate pentru a trata tulburările metabolice. Luarea infuziei de ceai de fireweed dă un efect bun. Preparați treizeci de grame din această materie primă cu o jumătate de litru de apă clocotită, aduceți medicamentul la fierbere și lăsați timp de o jumătate de oră. Luați compoziția rezultată de șaptezeci de mililitri de patru ori pe zi.
De asemenea, puteți prepara patruzeci de grame de frunze de pătlagină cu două sute de mililitri de apă clocotită. Se lasă acoperit timp de o jumătate de oră, apoi se strecoară și se ia treizeci de mililitri cu aproximativ douăzeci de minute înainte de mese, de trei ori pe zi.
De asemenea, puteți combina cincisprezece grame de coada-calului cu două sute de mililitri de apă clocotită. Se lasă acoperit o jumătate de oră, apoi se strecoară. Luați cincizeci de mililitri de patru ori pe zi.
Dacă bănuiți dezvoltarea tulburărilor metabolice, ar trebui să căutați ajutorul medicului.
Tulburări ale lipidelor
Lipidele sunt substanțe cu compoziție chimică eterogenă. Corpul uman conține o varietate de lipide: acizi grași, fosfolipide, colesterol, trigliceride, steroizi etc. Necesarul uman de grăsimi variază între 80-100 g pe zi.
Funcțiile lipidelor
Structural: lipidele formează baza membranelor celulare.
de reglementare.
† Lipidele reglează permeabilitatea membranei, starea lor coloidală și fluiditatea, activitatea enzimelor dependente de lipide (de exemplu, adenilat și guanilat ciclaze, Na + , K + -ATPaza, Ca 2+ -ATPaza, citocrom oxidaza), activitatea membranei receptori (de exemplu, pentru catecolamine, acetilcolină, insulină, citokine).
† Lipidele individuale - substanțe biologic active (de exemplu, Pg, leucotriene, factor de activare a trombocitelor, hormoni steroizi) - reglează funcțiile celulelor, organelor și țesuturilor.
Alimentare cu energie. Lipidele sunt una dintre principalele surse de energie pentru mușchii striați, ficat, rinichi și o sursă suplimentară de energie pentru țesutul nervos.
De protecţie. Inclus țesut subcutanat lipidele formează un tampon
un strat care protejează țesuturile moi de stresul mecanic.
Izolator. Lipidele creează un strat izolator termic în țesuturile de suprafață ale corpului și o înveliș izolator electric în jurul fibrelor nervoase.
Forme tipice de patologie
Forme standard patologiile metabolismului lipidic sunt prezentate în Fig. 10–1.
Orez. 10–1. Forme tipice de patologie a metabolismului lipidic.
În funcție de nivelul tulburărilor metabolismului lipidic, se disting următoarele tulburări:
† Digestia și absorbția lipidelor în tractul gastrointestinal (de exemplu, ca urmare a deficienței lipazelor pancreatice, afectarea formării și excreției bilei, tulburări ale cavității și digestiei „membranare”).
† Transferul transmembranar al lipidelor din intestin în sânge și utilizarea lor de către celule (de exemplu, cu enterită, tulburări circulatorii în peretele intestinului subțire).
† Metabolizarea lipidelor în țesuturi (de exemplu, cu un defect sau deficiență de lipaze, fosfolipaze, LPLază).
În funcție de manifestările clinice, se disting obezitatea, epuizarea, dislipoproteinemia, lipodistrofia și lipidoza.
Obezitatea
Conținutul normal de țesut adipos la bărbați este de 15–20% din greutatea corporală, la femei - 20–30%.
Obezitatea este acumularea excesivă (patologică) de grăsime în organism sub formă de trigliceride. În același timp, greutatea corporală crește cu mai mult de 20-30%.
Potrivit experților OMS, în țările europene dezvoltate, de la 20 la 60% din populație este supraponderală, în Rusia - aproximativ 60%.
În sine, o creștere a masei de țesut adipos nu reprezintă un pericol pentru organism, deși îi reduce capacitățile de adaptare. Cu toate acestea, obezitatea crește riscul de boală cardiacă ischemică (de 1,5 ori), ateroscleroză (de 2 ori), hipertensiune(de 3 ori), diabet (de 4 ori), precum și unele neoplasme (de exemplu, cancer de sân, de endometru și de prostată).
Tipuri de obezitate
Principalele tipuri de obezitate sunt prezentate în Fig. 10–2.
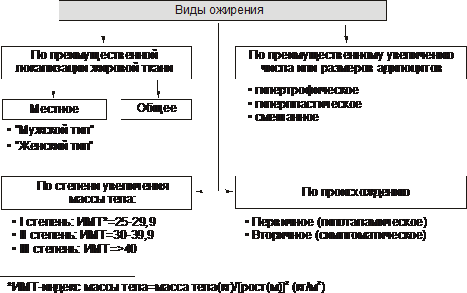
Orez. 10–2. Tipuri de obezitate. IMC - indicele de masă corporală (vezi text).
În funcție de gradul de creștere a greutății corporale, se disting trei grade de obezitate. În acest caz, se folosește conceptul de „greutate ideală a corpului”.
Sunt folosite diverse formule pentru a estima greutatea corporală ideală.
† Cel mai simplu - index Broca : 100 se scade din indicatorul de inaltime (in cm).
† Indicele de masă corporală se calculează, de asemenea, folosind următoarea formulă:
Greutatea corporală este considerată normală, cu un indice de masă corporală în intervalul 18,5-24,9. Dacă aceste valori sunt depășite, se spune că sunt supraponderali (Tabelul 10-1).
Tabelul 10–1. Nivelurile de obezitate
Notă. IMC - indicele de masă corporală
Pe baza localizării predominante a țesutului adipos, obezitatea se distinge între generală (uniformă) și locală (lipohipertrofie locală). Tipuri de obezitate locală:
† Tip feminin (gynoid) - exces de grăsime subcutanată în principal în șolduri și fese.
† Tip masculin (android) - acumulare de grăsime în zona abdominală.
Pe baza creșterii predominante a numărului sau mărimii celulelor adipoase, se disting următoarele:
† Obezitate hiperplastică (datorită creșterii predominante a numărului de adipocite). Este mai rezistent la tratament și în cazurile severe necesită o intervenție chirurgicală pentru îndepărtarea excesului de grăsime.
† Hipertrofic (datorită creșterii predominante a masei și dimensiunii adipocitelor). Se observă mai des după 30 de ani.
† Hiperplastic-hipertrofic (mixt). Este adesea detectată în copilărie.
Conform genezei, se disting obezitatea primară și formele sale secundare.
† Obezitatea primară (hipotalamică) este rezultatul unor tulburări ale sistemului de reglare a metabolismului grăsimilor (lipostat) - o boală independentă a genezei neuroendocrine.
† Obezitatea secundară (simptomatică) este o consecință a diferitelor tulburări din organism, care determină:
‡ reducerea consumului de energie (și, prin urmare, a consumului de trigliceride în țesutul adipos),
‡ activarea sintezei lipidelor - lipogeneza (observată într-o serie de boli, de exemplu, diabet, hipotiroidism, hipercortizolism).
Cauzele obezității
Cauza obezității primare este o disfuncție a sistemului adipocit-hipotalamus. Acesta este rezultatul unei deficiențe și/sau insuficiență a efectelor leptinei (prin suprimarea producției de neuropeptidă Y de către neuronii hipotalamici, ceea ce crește apetitul și foamea).
Obezitatea secundară se dezvoltă din cauza excesului de calorii și P nivelul redus al consumului de energie al organismului. Consumul de energie depinde de gradul de activitate (în primul rând fizic) și de stilul de viață al unei persoane. Activitatea fizică insuficientă este unul dintre motive importante obezitatea.
Patogenia obezității
Există mecanisme neurogenice, endocrine și metabolice ale obezității.
Variante neurogenice ale obezității
Mecanismele neurogenice (centrogenice și hipotalamice) ale obezității sunt prezentate în Fig. 10–3.
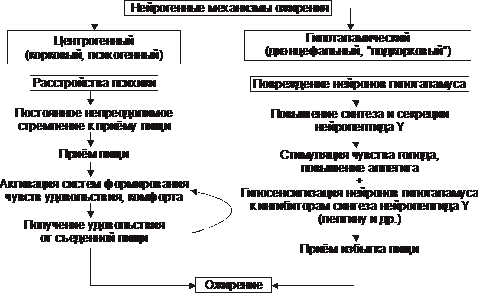
Orez. 10–3. Mecanisme neurogenice ale obezității.
† Centrogen mecanism (cortical, psihogen) - una dintre variantele tulburării de alimentație (celelalte două: anorexia nervoasă și bulimia). Motiv: diverse tulburări psihice, manifestate printr-o dorință constantă, uneori irezistibilă, de a mânca. Mecanisme posibile:
‡ activarea sistemelor serotoninergice, dopaminergice, opioidergice și a altor sisteme implicate în formarea sentimentelor de plăcere și confort;
‡ percepția alimentelor ca un stimul puternic pozitiv (dopaj), care activează și mai mult aceste sisteme - se închide cercul vicios al mecanismului centrogen al dezvoltării obezității.
† Hipotalamic mecanism (diencefalic, subcortical). Cauza sa este deteriorarea neuronilor nucleilor ventromediali și paraventriculari ai hipotalamusului (de exemplu, după o comoție cerebrală, cu encefalită, craniofaringiom, metastaze tumorale în hipotalamus). Cele mai importante legături în patogeneză:
‡ Creșterea spontană (fără un motiv identificat) a sintezei și secreției neuropeptidei Y de către neuronii nucleului ventral posterolateral al hipotalamusului.
‡ Deteriorarea sau iritația neuronilor din nucleul menționat mai sus stimulează, de asemenea, sinteza și secreția neuropeptidei Y și reduce sensibilitatea la factorii care inhibă sinteza neuropeptidei Y (în principal leptina).
§ Neuropeptida Y stimuleaza foamea si creste apetitul.
§ Leptina suprimă formarea stimulentului poftei de mâncare - neuropeptida Y.
‡ Întreruperea participării hipotalamusului la formarea senzației de foame. Această senzație se formează odată cu scăderea GPC, contracția mușchilor stomacului în timpul evacuării alimentelor și al golirii acesteia (senzație de disconfort alimentar - „sugerea în stomac”). Informațiile de la terminațiile nervoase senzitive periferice sunt integrate în nucleii nervoși ai hipotalamusului, responsabili pentru comportament alimentar.
‡ Ca urmare a proceselor de mai sus, producerea de neurotransmițători și neuropeptide care formează senzația de foame și cresc pofta de mâncare (GABA, dopamină, - endorfină, encefaline) și/sau neurotransmițători și neuropeptide care formează senzația de sațietate și inhibă alimentația. comportamentul (serotonină, norepinefrină, colecistochinină, somatostatina) este îmbunătățit).
Variante endocrine ale obezității
Mecanismele endocrine ale obezității - leptina, hipotiroidă, suprarenale și insulină - sunt prezentate în Fig. 10–4.
![]()
Orez. 10–4. Patogenia obezității.
† Mecanismul leptinei - conducând în dezvoltarea obezității primare.
‡ leptina formate în celulele adipoase. Reduce pofta de mancare si creste consumul de energie al organismului. Nivelul de leptina din sânge se corelează direct cu cantitatea de țesut adipos alb. Multe celule au receptori de leptina, inclusiv neuronii nucleului ventromedial al hipotalamusului. Leptina suprimă formarea și eliberarea neuropeptidei Y de către hipotalamus.
‡ NeuropeptidăY creează senzația de foame, crește pofta de mâncare, reduce consumul de energie al organismului. Există un fel de feedback negativ între hipotalamus și țesutul adipos: aportul alimentar în exces, însoțit de o creștere a masei de țesut adipos, duce la creșterea secreției de leptine. Acest lucru (prin inhibarea producției de neuropeptidă Y) reduce senzația de foame. Cu toate acestea, la persoanele obeze, acest mecanism de reglare poate fi afectat, de exemplu, din cauza rezistenței crescute la leptine sau a mutației genei leptinei.
‡ Lipostat. Circuitul leptină-neuropeptidă Y asigură menținerea masei de țesut adipos corporal - lipostat (sau punctul de referință al organismului în raport cu intensitatea metabolismului energetic). Pe lângă leptina, sistemul lipostat include insulină, catecolamine, serotonină, colecistochinină și endorfine.
† Mecanismul hipotiroidian obezitatea este rezultatul efectelor insuficiente ale hormonilor tiroidieni care conțin iod. Aceasta reduce intensitatea lipolizei, rata proceselor metabolice în țesuturi și costurile energetice ale organismului.
† suprarenale(glucocorticoizi, cortizol) mecanism obezitatea este activată din cauza hiperproducției de glucocorticoizi în cortexul suprarenal (de exemplu, în timpul bolii sau sindromului Itsenko ‑Cushing ). Sub influența excesului de glucocorticoizi, gluconeogeneza este activată (din această cauză se dezvoltă hiperglicemia), transportul glucozei în adipocite și glicoliza (reacțiile lipolitice sunt inhibate și trigliceridele se acumulează).
† Mecanismul insulinei Dezvoltarea obezității se dezvoltă ca urmare a activării directe a lipogenezei în țesutul adipos de către insulină.
† Alte mecanisme. Obezitatea se poate dezvolta și cu alte endocrinopatii (de exemplu, cu o deficiență a hormonului de creștere și a hormonilor gonadotrofici). Mecanismele dezvoltării obezității în aceste condiții sunt descrise în Capitolul 27, „Endocrinopatii”).
Mecanismele metabolice ale obezității
† Rezervele de carbohidrați din organism sunt relativ mici. Sunt aproximativ egale cu aportul lor zilnic cu alimente. În acest sens, a fost dezvoltat un mecanism de economisire a carbohidraților.
†Pe măsură ce proporția de grăsimi din dietă crește, rata de oxidare a carbohidraților scade. Acest lucru este evidențiat de o scădere corespunzătoare a coeficientului respirator (raportul dintre viteza de formare a CO 2 și rata de consum de O 2 ).
† Dacă acest lucru nu se întâmplă (dacă mecanismul de inhibare a glicogenolizei este perturbat în condiții concentrație mare grăsimi din sânge), este activat un mecanism care crește pofta de mâncare și crește aportul alimentar, având ca scop furnizarea cantității necesare de carbohidrați în organism.
†În aceste condiții, grăsimile se acumulează sub formă de trigliceride. Obezitatea se dezvoltă.
Epuizare
Pierderea și cașexia sunt scăderi patologice ale masei de țesut adipos sub normal. În același timp, masa musculară și a țesutului conjunctiv scade semnificativ.
Cu epuizare, deficitul de țesut adipos poate fi de 20–25% sau mai mult (cu un indice de masă corporală sub 20 kg/m2), iar cu cașexie - sub 50%.
Cauze și tipuri de epuizare și cașexie
Există cauze endogene și exogene ale epuizării.
Cauze exogene
† Postul complet sau parțial forțat sau conștient (în acest din urmă caz, cel mai adesea în scopul slăbirii).
‡ Postul complet este o condiție în care organismul nu primește hrană (de exemplu, în absența acestuia, refuzul de a mânca, incapacitatea de a mânca).
‡ Postul incomplet este o afecțiune caracterizată printr-o deficiență semnificativă a substanțelor plastice și a caloriilor din alimente (de exemplu, cu alimentație cantitativă și calitativă inadecvată, alimentație omogenă, vegetarianism).
† Alimente cu conținut scăzut de calorii, care nu completează costurile energetice ale organismului.
Cauze endogene
Depleția de origine endogenă este împărțită în primară și secundară.
† Cauzele epuizării primare (hipotalamice, diencefalice) sunt discutate în Fig. 10–5.
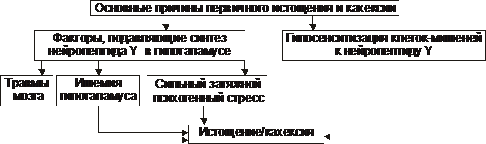
Orez. 10–5. Principalele cauze ale pierderii primare și ale cașexiei.
† Cauzele epuizării secundare (simptomatice) sunt prezentate în Fig. 10–6.
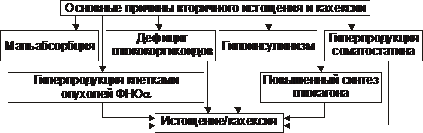
Orez. 10–6. Principalele cauze ale pierderii secundare și ale cașexiei.
Patogenia pierderii și a cașexiei
Risipirea exogenă și cașexia. Absența sau deficitul semnificativ de produse alimentare duce la dezvoltarea unui lanț de procese secvenţiale și interdependente, discutate în Fig. 10–7.
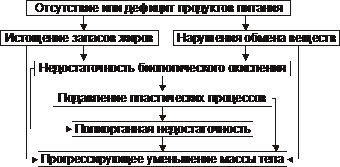
Orez. 10–7. Principalele verigi în patogeneza epuizării exogene și a cașexiei.
Forme endogene primare epuizare și cașexie. Formele hipotalamice, cahectice și anorexice au cea mai mare importanță clinică.
† Forma hipotalamică
În forma hipotalamică (diencefalică, subcorticală) de epuizare și cașexie, are loc o scădere sau încetare a sintezei și eliberării peptidei Y în sânge de către neuronii hipotalamusului, ceea ce duce la procesele secvențiale prezentate în Fig. 10–8.

Orez. 10–8. Principalele legături ale mecanismului hipotalamic de epuizare și cașexie.
† Forma de cachectină
Patogenia cachectinei sau citokinei, formei de pierdere și cașexie este discutată în Fig. 10–9.
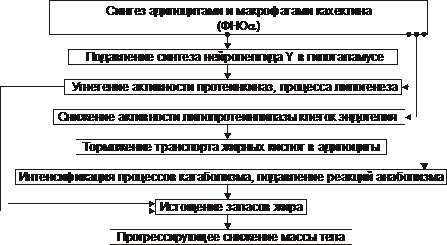
Orez. 10–9. Principalele legături ale mecanismului cachectinei de epuizare și cașexie.
† Forma anorexica
Principalele legături în patogeneza formei anorexice de epuizare și cașexie sunt prezentate în Fig. 10–10.
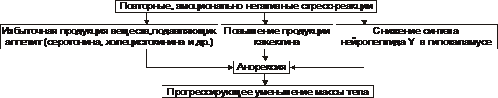
Orez. 10–10. Principalele legături ale mecanismului anorectic de epuizare și cașexie.
‡ Persoanele care sunt predispuse la dezvoltarea anorexiei au o atitudine critică față de corpul lor (percepute ca având supraponderal) determină dezvoltarea tulburărilor neuropsihiatrice. Acest lucru duce la episoade prelungite de refuz alimentar. Se observă cel mai adesea la adolescente și la fetele sub 16-18 ani.
‡ Cu reacții de stres repetate și negative din punct de vedere emoțional, se observă formarea excesivă a serotoninei și colecistokininei, care suprimă apetitul.
‡ Cursul ulterioar al procesului poate duce la implementarea efectelor neuropeptidei Y și cachectinei. Acești factori stau cel mai probabil la baza patogenezei anorexiei nervoase. Cu un curs prelungit al procesului, se dezvoltă o scădere pronunțată a greutății corporale, până la cașexie.
Forme endogene secundare epuizarea și cașexia sunt simptome importante, adesea principalele, ale altor afecțiuni și boli patologice (Fig. 10–11).

Orez. 10–11. Principalele cauze ale pierderii endogene secundare și ale cașexiei.
Lipodistrofie
Lipodistrofia este o afecțiune caracterizată prin pierderea generalizată sau locală a țesutului adipos, mai rar prin acumularea excesivă a acestuia în țesutul subcutanat. Cauzele lipodistrofiilor sunt variate și nu întotdeauna cunoscute, de la mutații ale diferitelor gene (de exemplu, lamine) până la complicații post-injectare. Există un grup mare de sindroame de lipodistrofie ereditare și congenitale, unele dintre ele sunt discutate în articolul „Lipodistrofii” (anexa „Termeni de referință” de pe CD).
Lipidoze
Lipidozele sunt o formă tipică de tulburare a metabolismului lipidic, caracterizată prin tulburări metabolice ale diferitelor lipide (de exemplu, sfingolipidoze, gangliozidoze, mucolipidoze, adrenoleucodistrofie, leucodistrofie, lipofuscinoză, cerebrozidoză) în celule (lipidoze parenchimatoase), țesuturi adipoase (lipidoze parenchimatoase), țesuturi adipoase (e). pereții vaselor arteriale (ateroscleroză), arterioscleroză). Aceste forme de lipidoze sunt descrise în acest manual (Capitolul 4 „Dezunerile celulare”, în acest capitol, precum și în articolele din Anexa „Cartea de referință a termenilor” de pe CD).
Dislipoproteinemie
Dislipoproteinemia este o afecțiune caracterizată printr-o abatere de la normă în conținutul, structura și raportul diferitelor medicamente din sânge. Tulburările metabolismului medicamentelor sunt veriga principală în patogeneza aterosclerozei, bolii ischemice ale inimii, pancreatitei și a altor boli.
Natura cursului și manifestările clinice ale dislipoproteinemiei sunt determinate de:
Proprietăți ereditare ale organismului (de exemplu, compoziția, raportul și nivelul diferitelor medicamente; caracteristicile metabolismului lor).
Factori de mediu (de exemplu, un set de produse alimentare, caracteristici dietetice și modele de alimentație).
Prezența (sau absența) bolilor concomitente (de exemplu, obezitatea, hipotiroidismul, diabetul, afectarea rinichilor și ficatului).
Caracteristicile lipoproteinelor
În plasma sanguină circulă diferite lipide. Acizii grași liberi sunt transportați de albumină și trigliceridele, colesterolul, esterii de colesteril și fosfolipidele, iar o cantitate mică de acizi grași sunt transportate ca parte a medicamentului. Aceste particule sferice constau dintr-un miez hidrofob (conține esteri de colesteril și trigliceride) și un înveliș hidrofil (conține colesterol, fosfolipide și apolipoproteine). Principalele caracteristici ale diferitelor medicamente sunt prezentate în tabel. 10–2.
Tabelul 10–2. Tipuri și proprietăți principale ale lipoproteinelor
|
Chilomicronii | |||||
|
Dimensiunea particulelor (nm) |
75–1200 | ||||
|
Densitate (g/cm 3 ) |
0,98–1,006 |
1,006–1,019 |
1,019–1,063 |
1,063–1,210 |
|
|
Compus (%): | |||||
|
Colesterolul | |||||
|
Trigliceridele | |||||
|
Fosfolipide | |||||
|
ApoLP |
B48, AI, AII, AIV, CI, CII, CIII, E |
B100, CI, CII, CIII, E |
AI, AII, AIV, CI, CII, CIII, E |
||
|
Sursă |
Intestinul subtire, lipidele alimentare |
Ficat, intestin subțire |
VLDL, LPPP |
Intestin subțire, ficat |
|
|
Aterogenitate |
Nu dovedit |
Nu dovedit |
Antiaterogen |
||
Apolipoproteine asigura păstrarea structurii ordonate a micelilor medicamentului, interacțiunea medicamentelor cu receptorii celulari și schimbul de componente între medicamente. Caracteristici detaliate apoLP și defectele lor sunt prezentate în articolul „Defecte ale apolipoproteinelor” (vezi Anexa „Referința termenilor” de pe CD).
Aterogenitatea lipoproteinelor
LP-urile sunt împărțite în aterogene și antiaterogene (Fig. 10-12).

Orez. 10–12. Tipuri de lipoproteine în funcție de aterogenitatea lor.
Efectul antiaterogen al HDL este determinat de următoarele proprietăți:
† Capacitatea de a elimina excesul de colesterol din membrana plasmatică a celulelor, inclusiv endoteliul vascular, și de a-l transfera în ficat, unde colesterolul este îndepărtat cu bilă.
† Afinitate mai mare a HDL pentru receptorii apoLP E și apoLP B comparativ cu LDL. Aceasta este determinată continut ridicat apoLP E la HDL. Ca rezultat, HDL împiedică celulele să preia particulele încărcate cu colesterol.
Evaluarea potențialului aterogen al lipidelor din sânge se realizează prin calcularea coeficientului de aterogenitate a colesterolului:
În mod normal, coeficientul aterogen al colesterolului nu depășește 3,0. Pe măsură ce această valoare crește, crește riscul de a dezvolta ateroscleroză.
Tipuri de dislipoproteinemie
Principalele tipuri de dislipoproteinemie sunt prezentate în Fig. 10–13.

Orez. 10–13. Tipuri de dislipoproteinemie.
Peste 30% din dislipoproteinemiile primare sunt forme moștenite de patologie (atât monogenice, cât și poligenice cu geneză multifactorială).
Aproximativ 70% dintre dislipoproteinemiile sunt considerate dobândite. Dislipoproteinemiile secundare (dobândite) sunt simptome ale altor boli. Ele însoțesc multe boli umane (Tabelul 10–3).
Tabelul 10–3. Cele mai frecvente procese patologice care duc la dezvoltarea dislipoproteinemiei secundare
|
Boala |
Mecanismul de dezvoltare |
|
|
Diabet |
eu, IV, V |
Scăderea activității LPLazei, excesul de flux de acizi grași în ficat, creșterea sintezei VLDL |
|
Secreția lipidelor afectată |
||
|
Ciroza hepatică primară |
Sinteza afectată a medicamentelor |
|
|
Sindrom nefrotic |
II, IV, V |
Creșterea formării de lipoproteine și trigliceride |
|
Hipotiroidism |
II, IV | |
|
Insuficiență pituitară |
Catabolismul lipidic redus |
|
|
Alcoolism cronic |
IV, V |
Scăderea activității LPLazei, creșterea sintezei lipidelor |
Diverse defecte ereditare, precum și procesele patologice dobândite și bolile duc adesea la modificări similare ale conținutului și profilului diferitelor medicamente. În acest sens, este necesară diferențierea fină a originii lor, permițând tratarea lor eficientă.
Hiperlipoproteinemie
Hiperlipoproteinemia este o afecțiune caracterizată printr-o tulburare a formării, transportului și metabolismului medicamentelor și care se manifestă printr-o creștere persistentă a conținutului de colesterol și/sau trigliceride în plasma sanguină.
Clasificare
În 1967, Fredrickson și coautorii au dezvoltat o clasificare a hiperlipoproteinemiilor (hiperlipidemii). Baza s-a bazat pe date de conținut colesterol totalși trigliceridele din plasma sanguină, precum și caracteristicile distribuției fracțiilor medicamentoase în timpul electroforezei și ultracentrifugării lor. Pe această bază, au fost identificate cinci tipuri de hiperlipoproteinemie. Această clasificare a fost revizuită ulterior de specialiștii OMS (Tabelul 10-4).
Încălcările și cauzele lor în ordine alfabetică:
tulburare de metabolism lipidic -
Întreaga linie boli cauzate de tulburare a metabolismului lipidic. Cele mai importante dintre ele sunt ateroscleroza si obezitatea. Boli a sistemului cardio-vascular, ca o consecință a aterosclerozei, ocupă primul loc în structura mortalității în lume. Una dintre cele mai frecvente manifestări ale aterosclerozei este deteriorarea vasele coronare inimile. Acumularea de colesterol în pereții vaselor de sânge duce la formarea plăcilor aterosclerotice. Acestea, crescând în dimensiune în timp, pot bloca lumenul vasului și pot interfera cu fluxul sanguin normal. Dacă, ca urmare, fluxul sanguin este întrerupt în artere coronare, atunci apare angină sau infarct miocardic. Predispoziția la ateroscleroză depinde de concentrația formelor de transport ale lipidelor din sânge - alfa-lipoproteinele plasmatice.
Ce boli cauzează tulburări ale metabolismului lipidic:
Acumularea de colesterol (CH) în peretele vascular are loc din cauza unui dezechilibru între intrarea acestuia în intima vasculară și ieșirea sa. Ca urmare a acestui dezechilibru, colesterolul se acumulează acolo. În centrele de acumulare a colesterolului se formează structuri - ateroame. Există doi factori cei mai cunoscuți care cauzează tulburări ale metabolismului lipidic.
1. În primul rând, acestea sunt modificări ale particulelor de LDL (glicozilare, peroxidare a lipidelor, hidroliza fosfolipidelor, oxidarea apo B). Prin urmare, ele sunt capturate de celule speciale - „scavengers” (în principal macrofage). Absorbția particulelor de lipoproteine de către receptorii „gunoi” are loc în mod necontrolat. Spre deosebire de endocitoza mediată de apo B/E, aceasta nu provoacă efecte reglatoare menite să reducă intrarea colesterolului în celulă, descrise mai sus. Ca urmare, macrofagele devin supraîncărcate cu lipide, își pierd funcția de absorbție a deșeurilor și se transformă în celule de spumă. Acestea din urmă sunt reținute în perete vase de sângeși începe să secrete factori de creștere care accelerează diviziunea celulară. Are loc proliferarea celulelor aterosclerotice.
2. În al doilea rând, este eliberarea ineficientă a colesterolului din endoteliu peretele vascular circulând în HDL din sânge.
Factori care influențează nivel crescut LDL la om
Sex - mai mare la bărbați decât la femeile aflate în premenopauză și mai scăzut decât la femeile în postmenopauză
- Îmbătrânirea
- Grăsimi saturateîn dietă
- Consum mare colesterolul
- Dieta saraca in alimente cu fibre grosiere
- Consumul de alcool
- Sarcina
- Obezitate
- Diabet
- Hipotiroidism
- Boala Cushing
- Uremie
- Nefroză
- Hiperlipidemie ereditară
Tulburări ale metabolismului lipidic (dislipidemie), caracterizate în primul rând prin continut crescutîn sânge colesterolul și trigliceridele sunt cei mai importanți factori risc de ateroscleroză și boli asociate ale sistemului cardiovascular. Concentrațiile plasmatice ale colesterolului total (TC) sau ale fracțiunilor acestuia se corelează strâns cu morbiditatea și mortalitatea din cauza bolii coronariene și a altor complicații ale aterosclerozei. Prin urmare, caracteristicile tulburărilor metabolismului lipidic sunt condiție prealabilă prevenire eficientă boli cardiovasculare.
Tulburările metabolismului lipidic pot fi primare sau secundare și se caracterizează doar printr-o creștere a colesterolului (hipercolesterolemie izolată), a trigliceridelor (hipertrigliceridemie izolată), a trigliceridelor și a colesterolului (hiperlipidemie mixtă).
Tulburarea primară a metabolismului lipidic este determinată de mutații unice sau multiple ale genelor corespunzătoare, în urma cărora există o supraproducție sau o utilizare afectată a trigliceridelor și Colesterolul LDL sau supraproducția și afectarea clearance-ului HDL.
Tulburarea primară a metabolismului lipidic poate fi diagnosticată la pacienții cu simptome clinice aceste încălcări, cu start prematur ateroscleroză (până la 60 de ani), la persoanele cu antecedente familiale de ateroscleroză sau cu o creștere a colesterolului seric > 240 mg/dL (> 6,2 mmol/L).
Tulburarea secundară a metabolismului lipidic apare, de regulă, în populația țărilor dezvoltate ca urmare a stil de viata sedentar viata, consumul de alimente care contin cantitati mari de colesterol, acizi grasi saturati.
Alte cauze ale tulburărilor secundare ale metabolismului lipidic pot fi:
1. Diabet zaharat.
2. Abuzul de alcool.
3. Insuficiență renală cronică.
4. Hipertiroidism.
5. Ciroza biliara primara.
6. Luarea anumitor medicamente (beta-blocante, medicamente antiretrovirale, estrogeni, progestative, glucocorticoizi).
Tulburări ereditare ale metabolismului lipidic:
Un număr mic de oameni experimentează tulburări ereditare metabolismul lipoproteinelor, manifestat prin hiper- sau hipolipoproteinemie. Ele sunt cauzate de o încălcare a sintezei, transportului sau defalcării lipoproteinelor.
În conformitate cu clasificare general acceptată, există 5 tipuri de hiperlipoproteinemie.
1. Existența tipului 1 se datorează unei activități LPL insuficiente. Ca urmare, chilomicronii sunt eliminați din fluxul sanguin foarte lent. Se acumulează în sânge, iar nivelurile de VLDL sunt, de asemenea, mai mari decât în mod normal.
2. Hiperlipoproteinemia de tip 2 se împarte în două subtipuri: 2a, caracterizată printr-un conținut ridicat de LDL din sângeși 2b (creștere a LDL și VLDL). Hiperlipoproteinemia de tip 2 se manifestă prin hipercolesterolemie ridicată, și în unele cazuri foarte mare, cu dezvoltarea aterosclerozei și boala coronariană inimile. Conținutul de triacilgliceroli din sânge este în limite normale (tip 2a) sau moderat crescut (tip 2b). Hiperlipoproteinemia de tip 2 este caracteristică boala grava- hipercolesterolemie ereditară care afectează tinerii. În cazul formei homozigote se termină fatal V La o vârstă frageda de la infarct miocardic, accidente vasculare cerebrale și alte complicații ale aterosclerozei. Hiperlipoproteinemia de tip 2 este larg răspândită.
3. În cazul hiperlipoproteinemiei de tip 3 (disbetalipoproteinemie), conversia VLDL în LDL este afectată, iar în sânge apare LDL sau VLDL flotant patologic. Conținutul de colesterol și triacilgliceroli din sânge este crescut. Acest tip este destul de rar.
4. Cu hiperlipoproteinemia de tip 4, principala modificare este o creștere a VLDL. Ca urmare, conținutul de triacilgliceroli din serul sanguin este semnificativ crescut. Combinat cu ateroscleroza vaselor coronare, obezitatea, diabetul zaharat. Se dezvoltă în principal la adulți și este foarte frecventă.
5. Hiperlipoproteinemie de tip 5 – o creștere a conținutului de ser din sânge de colesterol și VLDL, asociată cu moderată activitate scăzută lipoprotein lipaze. Concentrațiile de LDL și HDL sunt sub normal. Conținutul de triacilgliceroli din sânge este crescut, în timp ce concentrația de colesterol este în limite normale sau moderat crescută. Apare la adulți, dar răspândită nu are.
Tipizarea hiperlipoproteinemiei se efectuează în laborator pe baza studiului conținutului diferitelor clase de lipoproteine din sânge folosind metode fotometrice.
Nivelul colesterolului în HDL este mai informativ ca un predictor al leziunilor aterosclerotice ale vaselor coronare. Și mai informativ este coeficientul care reflectă raportul dintre medicamentele aterogene și cele antiaterogene.
Cu cât acest coeficient este mai mare, cu atât mai mult pericol apariția și evoluția bolii. La indivizii sănătoși, nu depășește 3-3,5 (la bărbați este mai mare decât la femei). U pacienţii cu boală cardiacă ischemică ajunge la 5-6 sau mai multe unități.
Este diabetul o boală a metabolismului lipidic?
Manifestările tulburărilor metabolismului lipidic sunt atât de pronunțate în diabet, încât diabetul este adesea numit mai mult o boala lipide decât metabolismul carbohidraților. Principalele tulburări ale metabolismului lipidelor în diabet zaharat sunt descompunerea crescută a lipidelor, creșterea formării corpilor cetonici și scăderea sintezei de acizi grași și triacilgliceroli.
U persoana sanatoasa de obicei, 50% din glucoza primită este descompusă de CO2 și H2O; aproximativ 5% este transformat în glicogen, iar restul este transformat în lipide în depozitele de grăsime. În diabet, doar 5% din glucoză este transformată în lipide, în timp ce cantitatea de glucoză descompusă în CO2 și H2O scade și ea, iar cantitatea transformată în glicogen se modifică ușor. Rezultatul unui consum redus de glucoză este o creștere a nivelului de glucoză din sânge și eliminarea acesteia în urină. Deficitul intracelular de glucoză duce la o scădere a sintezei acizilor grași.
La pacienții care nu primesc tratament, există o creștere a conținutului plasmatic de triacilgliceroli și chilomicroni, iar plasma este adesea lipemică. O creștere a nivelului acestor componente determină o scădere a lipolizei în depozitele de grăsime. Scăderea activității lipoprotein lipazei contribuie în continuare la scăderea lipolizei.
Peroxidarea lipidelor
Caracteristicile lipidelor membranele celulare este nesaturarea lor semnificativă. Acizii grași nesaturați sunt ușor supuși distrugerii peroxidului - LPO (peroxidarea lipidelor). Răspunsul membranei la deteriorare se numește, prin urmare, „stres de peroxid”.
LPO se bazează pe mecanismul radicalilor liberi.
Patologia radicalilor liberi este fumatul, cancerul, ischemia, hiperoxia, îmbătrânirea, diabetul, i.e. În aproape toate bolile, apare formarea necontrolată radicali liberi oxigen și intensificarea LPO.
Celula are sisteme pentru a se proteja de deteriorarea radicalilor liberi. Sistemul antioxidant al celulelor și țesuturilor corpului include 2 verigi: enzimatic și non-enzimatic.
Antioxidanți enzimatici:
- SOD (superoxid dismutaza) si ceruloplasmina, implicate in neutralizarea radicalilor liberi de oxigen;
- catalaza, care catalizează descompunerea peroxidului de hidrogen; sistemul glutation, care asigură catabolismul peroxizilor lipidici, nucleotidelor modificate cu peroxid și steroizilor.
Chiar și o lipsă pe termen scurt de antioxidanți neenzimatici, în special de vitamine antioxidante (tocoferol, retinol, ascorbat), duce la deteriorarea persistentă și ireversibilă a membranelor celulare.
Ce medici ar trebui să contactați dacă apare o tulburare a metabolismului lipidic:
Ați observat o tulburare a metabolismului lipidic? Doriți să aflați informații mai detaliate sau aveți nevoie de o inspecție? Puteți programați-vă la un medic– clinica Eurolaborator mereu la dispozitia ta! Cei mai buni doctori te vor examina și te vor studia semne externeși vă va ajuta să identificați boala după simptome, să vă sfătuiască și să furnizați ajutor necesar. poti si tu sunați la un medic acasă. Clinica Eurolaborator deschis pentru tine non-stop.simptomele bolilor și nu-ți dai seama că aceste boli pot pune viața în pericol. Sunt multe boli care la început nu se manifestă în corpul nostru, dar în final se dovedește că, din păcate, este prea târziu să le tratăm. Fiecare boală are propriile simptome specifice, caracteristice manifestări externe- așa-zisul simptomele bolii. Identificarea simptomelor este primul pas în diagnosticarea bolilor în general. Pentru a face acest lucru, trebuie doar să o faceți de mai multe ori pe an. fi examinat de un medic pentru a nu numai preveni boală cumplită, dar și sprijin minte sănătoasăîn organism și în organism în ansamblu.
Dacă vrei să pui o întrebare unui medic, folosește secțiunea de consultații online, poate că acolo vei găsi răspunsuri la întrebările tale și citește sfaturi de autoîngrijire. Dacă sunteți interesat de recenzii despre clinici și medici, încercați să găsiți informațiile de care aveți nevoie. Înregistrați-vă și pe portal medical Eurolaborator pentru a fi la curent cele mai recente știriși actualizări de informații de pe site, care vă vor fi trimise automat prin e-mail.
Diagrama de simptome este doar pentru scopuri educaționale. Nu vă automedicați; Pentru toate întrebările referitoare la definirea bolii și metodele de tratare a acesteia, consultați-vă medicul. EUROLAB nu este responsabil pentru consecințele cauzate de utilizarea informațiilor postate pe portal.
Dacă sunteți interesat de orice alte simptome de boli și tipuri de tulburări, sau aveți alte întrebări sau sugestii, scrieți-ne, cu siguranță vom încerca să vă ajutăm.

