Пиковая систолическая скорость кровотока норма. Ультразвуковое исследование сосудов. Исследование сосудов верхних конечностей
Физические основы ультразвука и варианты ультразвуковых методов исследования в кардиологии подробно описаны в многочисленных руководствах , к которым мы отсылаем любознательного читателя.
В настоящее время в ангиологии наибольшее распространение получили следующие методы УЗИ:
- ультразвуковая допплерография, позволяющая измерять скорость потока крови;
- ультразвуковая ангиография (В-сканирование), обеспечивающая визуализацию внутреннего просвета сосуда, измерение его диаметра и оценку состояния сосудистой стенки;
- дуплексное сканирование, объединяющее оба названных выше метода;
- спектральный анализ и цветное картирование допплеровского сигнала, поз-воляющие изучать характер и скорость потока крови в сердце и сосудах.
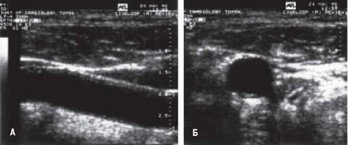
Рис. 3.21. Возрастные изменения доппле- тразвукового луча. Следует сра- рограммы периферической артерии .
зу оговориться, что допплеров-ское УЗИ (Д-УЗИ) сосудов не является методом прямой визуализации атеросклеротического поражения артерий, но по изменению скорости кровотока позволяет судить о выраженности сосудистой патологии.
В современной диагностике заболеваний сердца и сосудов применяются четыре варианта Д-УЗИ .
Доплеровское расследование при анемии плода
Поскольку существует разница в результатах между лабораториями, каждое учреждение должно определить свой «критический титр» - уровень, на котором существует значительный риск развития гидрографов. Внутрисуставные переливания продолжаются до 35 недель беременности. В идеале, эмбриональное вмешательство должно происходить до наступления гидрогеля. В результате были запрошены неинвазивные методы, которые предсказывают тяжелую анемию до наступления гидрогелей. В течение многих лет были оценены несколько сосудов, чтобы лучше предсказать тяжелую анемию.
рости и характере кровотока.
Спектральный анализ допплеровских сигналов показал различие артериального кровотока в зависимости от возраста даже у здоровых людей (рис. 3.21).
Известно, что при исследовании скорости кровотока по сосудам с помощью ультразвука эффект Допплера проявляется тем лучше, чем выше эластичность стенки сосуда, эффективное давление и сопротивление . Это выражается в виде профиля скоростей (рис. 3.21) с крутым подъемом ускорения (а). Снижение скорости движения (b) менее быстрое с инцизурой (с), дикротическим зубцом (d), постсистоличес- ким забросом (е). Эластическое сопротивление артерии обусловливает появление позитивной волны (f). Таким образом, достаточная эластичность артериальных стенок позволяет левому желудочку выбрасывать кровь в артериальное русло, даже если артериально-капиллярное сопротивление повышено. Способность артерий к эластичному сокращению обеспечивает поддержание кровотока во время диастолы. Вследствие атеросклероза эластичность артериальной стенки снижается, что ведет прежде всего к уменьшению вторичной позитивной волны (f), затем происходит сокращение заброса (е), закругление вершины и расширение основания главного комплекса допплерограммы.
В соответствии с известными физическими закономерностями стенка сосуда обладает большим акустическим сопротивлением по сравнению с окружающими тканями, следственно, она дает более яркое отражение УЗ-сигнала, чем близлежащие мягкие ткани. Просвет сосуда имеет мень-
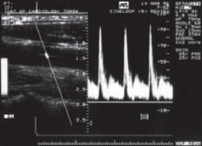 шее акустическое сопротивление, чем стенка, поэтому разница данного показателя этих структур будет достаточно большой, чтобы резко конт-растировать их изображение. Таким образом, контуры сосудов и их просвет в норме идентифицируются достаточно отчетливо, при этом стенки артерий визуализируются на экране УЗ-прибора как яркие структуры, а просвет со- Рис. 3.23. Пример дуплексного сканирования суда выглядит темным крупной артерии (общая сонная артерия) (рис. 3.22). здорового человека. Пояснение в тексте.
шее акустическое сопротивление, чем стенка, поэтому разница данного показателя этих структур будет достаточно большой, чтобы резко конт-растировать их изображение. Таким образом, контуры сосудов и их просвет в норме идентифицируются достаточно отчетливо, при этом стенки артерий визуализируются на экране УЗ-прибора как яркие структуры, а просвет со- Рис. 3.23. Пример дуплексного сканирования суда выглядит темным крупной артерии (общая сонная артерия) (рис. 3.22). здорового человека. Пояснение в тексте.
Увеличение скорости крови с анемией плода было зарегистрировано в сонных артериях, нисходящей аорте и пупочной вене. Внутрисердечные и венозные исследования Допплера не могут точно предсказать анемию 9. Аплома плода 16 и селезеночная артерия 17 также оценивались с переменным успехом. Использование угловых независимых показателей или измерений, которые требуют коррекции угла, недостаточно чувствительны для обнаружения изменений скорости, связанных с анемией 1.
Средняя мозговая артерия стала подходящим выбором при оценке плода для анемии. Однако метод получения пиковой систолической скорости в средней мозговой артерии имеет решающее значение для получения достоверных результатов. Вершину плода изображают на осевой плоскости, которая включает в себя перегородку перегородки и талами. Затем преобразователь перемещается к основанию черепа до тех пор, пока не будет визуализирован круг Виллиса. Угол сундука судна должен быть близок к нулю, а доплеровские ворота располагаются в центре сосуда непосредственно над его демаркацией из круга Уиллиса 18.
При сосудистой патологии различия в акустическом сопротивлении между просветом сосуда, его стенками и окружающими тканями уменьшаются, что ведет к снижению контрастных различий между ними.
В современной УЗ-диагностике используют приборы, работающие в В-режиме реального масштаба времени, что означает возможность получения изображения и контроля за движением органов в соответствии с естественным временным ходом. Безусловными достоинствами этих приборов, выгодно отличающими их от других аппаратов, являются: высокая разрешающая способность, возможность получения изображения в любой плоскости и под любым углом сканирования интересующего сосуда, незаменимость при изучении движущихся объектов, в частности - пульсирующих сосудов.
Следует учитывать, что при распространении УЗ-волны в различных средах происходит потеря энергии, и степень ее поглощения зависит от частоты УЗ-сигнала. Чем больше частота, тем выше степень поглощения. Поэтому в УЗ-сканировании для локации глубоко расположенных сосудов (грудная, брюшная полость, забрюшинное пространство) используют датчики с частотой 2,25-3,5 МГц. Для эхолокации поверхностных сосудов (конечности, шея) необходимы УЗ-датчики с частотой 510 МГц .
Несомненным прогрессом явилась возможность одновременно с В-сканированием выполнять Д-УЗИ кровотока в сосуде (дуплексное сканирование, УЗ-ангиография). Располагая метку, откуда будет осуще-
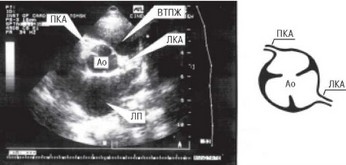
Рис. 3.24. Ультразвуковое сканирование коронарных артерий. А - эхограмма; Ао
Исследование сосудов шеи
Плод не должен быть активным или дышать во время обследования. До этого гестационного возраста ретикулоэндотелиальная система слишком незрелая, чтобы успешно уничтожить достаточное количество покрытых антителом эритроцитов, чтобы вызвать значительную анемию 24.
Физиологический механизм этого открытия еще не выяснен. Фетальная длина печени при нормальной и изоиммунизированной беременности. Ультрасонографические измерения селезенки плода в эритроцитах - аллоиммунизированная беременность. Средняя систолическая скорость центральной мозговой артерии для диагностики анемии плода: неописуемая история. Венозная, артериальная и внутриутробная кровоточивость крови в изоиммунизации эритроцитов. Влияние трансфузии внутрисосудистой трансплантации плода на внутриклеточные доплеровские формы волны плода. Острые гемодинамические изменения плода после внутриутробного переливания для лечения аллоиммунизации тяжелых эритроцитов. Внутриматочная переливание плода при гемолитической болезни. Преимущества и риск трансфузии плода в клетках после 32 недель беременности. Фетальная переливание для аллоиммунизации эритроцитов плода во время беременности. Импульсные доплеровские сигналы скорости потока до и после внутриматочной внутрисосудистой переливания для тяжелого эритробластоза фетали. Импульсные доплеровские сигналы скорости потока в предсказании гематокрита плода сильно изоиммунизированной беременности. Диагностика анемии плода с использованием допплеровского ультразвука при беременности, осложненной иммунизацией группы материнской крови. Точное предсказание фетального гемоглобина с помощью допплеровской ультрасонографии. Неинвазивные тесты для прогнозирования эмбриональной анемии при беременности, вызванной Келл-аллоиммунизированным. Допплер-сонография для прогнозирования анемии плода, вызванная массивным кровоизлиянием в фетоматери. Значение средней систолической скорости средней мозговой артерии в диагностике анемии плода после внутриутробной смерти одного монохорионного близнеца. Неинвазивный диагноз с помощью допплеровской ультрасонографии анемии плода в результате парвовирусной инфекции. Прогнозирование анемии плода при резус-болезни путем измерения систолической скорости пиковой средней церебральной артерии. Коррекция эмбриональной анемии на систолической скорости пика средней мозговой артерии. Корреляция между систолической скоростью пика средней мозговой артерии и фетальным гемоглобином после 2 предыдущих внутриматочных переливаний. Влияние эмбриональных поведенческих состояний на систолическую скорость пика средней мозговой артерии. Продольное измерение пиковой систолической скорости в средней церебральной артерии плода для мониторинга беременностей, осложненных аллоиммунизацией красных клеток: перспективное многоцентровое исследование с целью лечения. Обычное управление аллоиммунизацией эритроцитов у матери по сравнению с управлением с помощью допплеровской оценки систолической скорости средней мозговой артерии.
- Совместная группа для допплеровской оценки скорости крови у анемичных плодов.
- Фетальная скорость кровотока средней мозговой артерии в анемическом плоде.
- Сонографическая оценка плода плодовых водорослей.
- Переоценка полезности диаметра плодной вены плода в управлении изоиммунизацией.
- аорта; ВТПЖ - выносящий тракт правого желудочка; ЛП - левое предсердие; ЛКА
- левая коронарная артерия; ПКА - правая коронарная артерия. На схеме показано расположение устьев коронарных артерий в проекции створок аортального клапана.
ствляться регистрация отраженного сигнала, на любой глубине УЗ-луча под контролем изображения в В-режиме, можно выбирать любой участок сосуда, в котором необходима регистрация скорости кровотока (рис. 3.23).
Современные УЗ-приборы обладают возмож-ностью сочетать режимы В-сканирования, Д-УЗИ и цветного картирования потоков, что позволяет определять характер и выраженность нарушений кровотока в зависимости от тяжести органически изменений сосудистой стенки. Иными словами, такие приборы помогают параллельно оценивать морфологический субстрат и функциональные проявления сосудистой патологии.
УЗИ коронарных артерий в диагностике ИБС не получило широкого распространения. Между тем опубликованы многочисленные данные о возможности визуализации устьев коронарных артерий (чаще всего устье общего ствола ЛКА) с помощью двумерной эхокардиографии .
Показано, что для локации ЛКА оптимальным является апикальное расположение датчика, при котором удается визуализировать артерию на максимальном протяжении и нередко идентифицировать проксимальный отдел огибающей ветви. Препятствием для наблюдения артерии из этого доступа является выраженная степень ожирения.
Парастернальное ультразвуковое окно привлекает возможностью исследовать артерию с большим увеличением, так как отсюда она наиболее близка к датчику (рис. 3.24). У пациентов с эмфиземой легких из этого доступа ЛКА не обнаруживается в связи с уменьшением акустического окна. В этих случаях предпочтительным является субкосталь- ный доступ.
У здоровых лиц толщина стенок ЛКА составляет 1-2 мм, ширина просвета 3-6 мм. Внутренний контур артериальной стенки ровный. При визуальной сравнительной оценке плотность стенки артерии приближается к плотности прилежащего левого сегмента аорты и значительно уступает плотности переднего и заднего сегментов.
У больных ИБС выявлено увеличение плотности стенок ЛКА, обусловленное атеросклеротическим поражением .
В литературе имеются данные о возможности применения чреспи- щеводного УЗИ для визуализации коронарных артерий и изучения коронарного кровотока методом допплерографии и цветного картирования .
Несмотря на многообещающие предварительные данные, по мнению авторитетных исследователей , ограничениями метода УЗИ коронарных артерий являются ложноположительные результаты и способность выявлять только значительные поражения коронарных артерий - стенозы не менее, чем на 50%. Кроме того, вопросы специфично-
Кроме того, измерения интимной медиальной толщины связаны с повышенным риском инсульта. Эти испытания включают разнообразные группы населения в Европе и Северной Америке, чтобы помочь врачам получить доказательства, подтверждающие лучшую клиническую практику для бессимптомной болезни сонной артерии.
Ультрасонография сонной артерии - это двухэтапная или дуплексная процедура. Изображение обычно просматривается в оттенках серого, что является шкалой яркости. Иногда информация о цветовом потоке накладывается на изображение в градациях серого. В артерии помещается зондирующий курсор, и генерируется сигнал, представляющий скорость кровотока. Сигнал имеет пики и отливы, которые соответствуют систолическому и диастолическому кровотоку.
- Обработка изображений осуществляется с помощью метода яркостного режима.
- По соглашению цвет пульсирующей артерии красный.
- Это называется цветной доплеровской визуализацией.
- Это позволяет измерять скорость кровотока.
- Сигнал визуальный и слуховой.
- Пики и отливы создают спектр.
Б
А
1
2
3
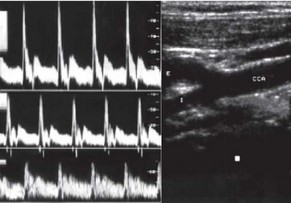
Рис. 3.25. Пример дуплексного сканирования сонной артерии на уровне бифуркации у здорового человека. А - продольное В-сканирование; Б - допплерограммы кровотока в общей (1), наружной (2) и внутренней (3) сонных артериях.
Метод импульсного эха - используется для изображения судна. Исходный сигнал генерируется в компьютере, передается через датчик на шейку пациента, а затем отскакивает от различных границ ткани. Направление импульса и время, прошедшее до возвращения сигнала определяют положение границы ткани. Изменения эхогенности бляшки, измеренные количественным индексом ультразвукового исследования с помощью компьютера, могут быть маркером нестабильности бляшек, а также индикатором зубного налета ремоделирование, тем самым обеспечивая средства для мониторинга препаратов против атеросклероза, таких как статины. Объект, который очень мало подбирается из импульса, такого как жидкость в кисте, является гипоэхогенным. Объект, который подбирает большую часть сигнала, например, сильно кальцинированный бляшка, является гиперэхогенной.
- Датчик обнаруживает сигнал возврата.
- Эхогенность объекта на изображении определяет его яркость.
сти и чувствительности методов УЗИ в выявлении коронарных стенозов нельзя считать окончательно решенными.
Развитие ультразвуковой технологии и катетерной техники привело к появлению метода внутрисосудистой ультразвуковой визуализации, который позволяет проводить качественную (субъективную) оценку биологических структур в зоне интереса, количественно анализировать акустические параметры (амплитуду, частоту, угол рассеяния отраженного сигнала, акустическую плотность и неоднородность тканей), характеризующие изучаемый объект: сосудистую стенку, атероматозные и тромботические наложения .
У больных ИБС внутрикоронарное УЗИ дает возможность качественно и количественно определять выраженность стеноза, морфологическую структуру стенки артерии и атеросклеротической бляшки, а также оценивать функциональные свойства (эластичность, ригидность) коронарной артерии .
Однако в настоящее время этот метод, по-видимому, следует отнести к категории экстравагантных, и в ближайшие годы он едва ли станет доступен для широкого применения в клинике.
УЗИ брахиоцефальных артерий сейчас принадлежит основное значение в диагностике цереброваскулярной патологии, обусловленной ате-
Изменения скорости в спектральном анализе отражают изменения в гемодинамике. . Доплеровское явление. Используется для оценки скорости крови при прохождении через зонд. Как и в случае технологии импульсного эха, импульс испускается от преобразователя с определенной частотой. Когда пульс попадает в движущуюся кровь, он возвращается обратно к зонду; однако его частота изменяется.
- Изменение частоты известно как допплеровский сдвиг.
- Этот сдвиг коррелирует с изменениями скорости кровотока.
- Это называется зависимостью от угла.
dT
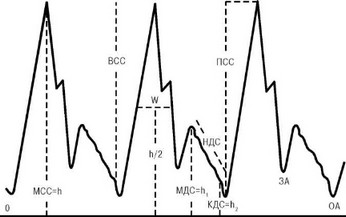
Рис. 3.26. Основные элементы допплерограммы общей сонной артерии . Пояснение в тексте.
ро-склерозом, тромбозом и эмболиями, неспецифическим аортоарте- риитом, врожденными сосудистыми аномалиями. Считается, что с помощью УЗИ можно установить локализацию и протяженность поражения примерно с той же точностью, как и при артериографии .
Исследование проводят в положении больного лежа на спине с откинутой назад головой, для чего под лопатки может быть подложен валик.
Датчик устанавливают в области яремной вырезки и отклоняют кзади. Линия сканирования проходит во фронтальной плоскости. При этом на экране УЗ-монитора видна дуга аорты с отходящими от нее основными ветвями: левой общей сонной и подключичными артериями. Для исследования сосудов шеи УЗ-датчик располагают поочередно на обеих боковых поверхностях в области грудинно-ключично-сосцевидных мышц. Линия сканирования примерно совпадает с сагиттальной плоскостью. Здесь обычно видны общие сонные артерии и их бифуркации.
На экране эхолокатора общая сонная артерия (ОСА) прослеживается на всем протяжении со светлыми, ровными, хорошо различимыми стенками. Отчетливо видна синхронная с сердечными сокращениями пульсация. Кроме основного ствола ОСА, хорошо дифференцируются
наружная и внутренняя сонные артерии (ВСА), в которых при Д-УЗИ регистрируются характерные спектры артериального кровотока (рис. 3.25).
Особенность кровотока по брахиоцефальным артериям у здоровых людей состоит в том, что ни в одной из фаз сердечного цикла он не достигает нуля, поэтому на допплерограмме ОСА различают следующие элементы (рис. 3.26):
Подобно свету, радиации и слышимому звуку, ультразвук - это волна. Среда представляет собой канал, через который проходит волна. Примерами сред являются воздух, вода и ткань. Частота измеряется в циклах в секунду, называемая герц. Цикл представляет собой один оборот длины волны.
Исследование сосудов нижних конечностей
Поэтому он измеряется в мегагерцах. Поэтому он измеряется в килогерцах. Иногда используется термин пространственная длительность импульса. Он равен числу циклов в импульсе, умноженном на длину волны. Когда ультразвук проходит через ткань, часть сигнала теряется через рассеяние, отражение и поглощение.
- МСС - максимальная систолическая скорость (h);
- ВСС - возрастание систолической скорости;
- МДС - максимальная диастолическая скорость (hj);
- КДС - конечная диастолическая скорость (h2);
- НДС - наклон диастолической скорости;
- ПСС - прирост систолической скорости;
- ЗА - закрытие аорты;
- ОА - открытие аорты;
- dT - время от открытия аорты до максимума ПСС;
- СУ - систолическое ускорение (СУ = ПСС: dT);
- ИЦС - индекс циркулярного сопротивления (ВСС / МСС);
- W- ширина кривой на уровне половины МСС.
В спектральном анализе допплерограммы для определения стенози- рования сонных артерий выделяют три основных признака: изменение пиковой систолической частоты, величина спектрального расширения допплеровского сигнала, форма огибающей спектрограммы.
С внедрением методов В-сканирования и дуплексного исследования появилась возможность документально подтверждать эволюцию атеро-
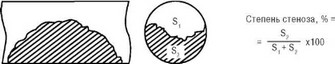
Рис. 3.27. Схема определения степени стенозирования артерии по данным ультразвукового В-сканирования. Пояснение в тексте.
склеротической бляшки от момента ее появления до развития стеноза или окклюзии артерии.
В одном из наших исследований в скринирующем режиме было выполнено 2300 ультразвуковых ангиографий сонных артерий у пациентов с различными сердечно-сосудистыми заболеваниями, но при отсутствии отчетливых клинических проявлений хронической цереброваскулярной недостаточности (ХЦВН). Среди всех обследованных наиболее частой (84%) патологией была ИБС.
Отдельную группу составили 54 больных с атеросклеротическим поражением брахиоцефальных артерий и клиническими признаками ХЦВН II-IV степени. Пациентам этой группы, кроме УЗИ сонных артерий, были выполнены восходящая церебральная ангиография и операция каротидной эндар- терэктомии с последующим макро- и микроскопическим анализом биопсийного операционного материала (профессор И.В.Суходоло).
В работе использовали эхо- камеры SSD-280 (фирма “Aloka”, Япония), “Ultramark-9 HDI” (фирма ATL, США) и высокочастотный (7,5 МГц) линейный зонд. Двумерное сканирование сонных артерий выполняли в продольной и поперечной проекциях с переднебоковой поверхности шеи при максимальном отведении голо-
Качественная оценка допплеровского спектра
Поэтому, чем выше частота машины, тем больше затухание, и тем меньше может отображаться на большем расстоянии от зонда. С другой стороны, более высокие частоты означают более короткие длины волн и лучшие разрешения. Поэтому существует компромисс в регулировании частот.
Поток крови может быть ламинарным, нарушенным, турбулентным или пробковым. Когда стеноз отсутствует, кровоток является ламинарным. Поток крови ровный, с самым быстрым потоком в середине и самым медленным по краям сосуда. Когда присутствует небольшая степень стеноза, кровоток становится нарушенным и теряет ламинарное качество. Даже в нормальных условиях такой поток можно наблюдать вокруг каротидной колбы. При еще большем стенозе поток может стать турбулентным.
вы. Для количественной оценки амплитуды, частоты и интенсивности отраженного сигнала от стробируемого объекта применяли встроенную в прибор программу гистометрического анализа.
У больных ИБС атеросклеротическое поражение сонных артерий выявлено в каждом четвертом случае. Чаще всего (83,3%) бляшки локализовались в верхней трети и бифуркации ОСА. Асимметричное поражение наблюдалось в четыре раза реже, чем двустороннее и “многоэтажное”. Причем последний вид поражения у больных ХЦВН установлен в 85,2%. У 8 больных ИБС обнаружено бессимптомное одностороннее сте- нозирование ВСА более 75% просвета сосуда. Здесь же надо заметить, что и у больных с синдромом ХЦВН не удалось проследить параллелизма между степенью стенозирования каротидных артерий и тяжестью неврологического дефицита. Это подтверждает литературные данные о том, что в 15-20 % случаев даже полная односторонняя окклюзия ВСА может протекать бессимптомно .
При сопоставлении частоты выявления каротидных стенозов с помощью УЗИ и рентгеноконтрастной ангиографии корреляционный анализ показал высокое совпадение (r=0,789; рlt;0,01) результатов обоих методов. Однако, по нашему мнению, применение двухосевого УЗИ позволяет более точно определять степень стенозиро- вания артерий. Это связано с тем, что при измерении диаметра сосуда в одной продольной проекции истинная величина стеноза искажается, в особенности при эксцентрических бляшках, тогда как поперечное УЗ-
сканирование дает возможность определять площадь сечения артерии и степень ее стеноза (рис. 3.27).
В ходе исследования каротидных стенозов наше внимание привлекла неоднородность интенсивности отражения сигнала, что могло отражать особенности морфологической структуры атероматозных наложений. Первоначально среди всех УЗ-находок были выделены две разновидности бляшек
Количественные допплеросонографические параметры артериального кровотока
Число Рейнольдса определяет уровень, на котором происходит турбулентный поток. Это известно как закон Пуазейля. Таким образом, при нормальной гемодинамике, когда длина сосуда возрастает или увеличивается вязкость жидкости, происходит и сопротивление. По мере увеличения радиуса сосуда сопротивление значительно уменьшается.
В стенотическом сосуде объемный поток остается постоянным. В правиле непрерывности указывается, что объемный поток остается постоянным независимо от степени сужения. Поэтому, когда диаметр сосуда уменьшается, скорость крови увеличивается, чтобы поддерживать объемный расход.
- плотные (“твердые”) и неплотные (“мягкие”).
Вторая категория бляшек отличалась зна
чительной (30-40 Дб) интенсивностью отраженного сигнала, гистомет- рический анализ которого превышал уровень интенсивности сигнала от сосудистой стенки. Эти бляшки были отнесены к плотным, или гомогенным.
Гистометрическое разложение отраженной УЗ-волны позволяет оценивать консистенцию бляшки по максимальной амплитуде интенсивности эхо-сигнала, а ее структуру (однородность, неоднородность) - по частоте встречаемости максимального уровня во всем спектре сигнала (рис. 3.28).
Сопоставление гистометрического анализа В-сканирования атеросклеротических бляшек и результатов гистоморфологического исследования операционного материала, полученного после каротидной эндар- терэктомии (54 больных), позволило выделить вполне определенные эхоморфоструктурные критерии классификации атеросклероза. По массивности включения в бляшку грубых кальцинозных и фиброзных конгломератов, наличию казеозного некроза и набухания, которые нашли свое отражение в данных УЗИ, все бляшки были разделены на 3 типа:
- 1-й тип - “мягкие”, рыхлые бляшки с низкой акустической плотностью и амплитудой эхо-сигнала в диапазоне от 8 до 18 Дб (рис. 3.28.а);
- 2-й тип - гетерогенные бляшки с широким диапазоном амплитудных характеристик интенсивности эхо-сигнала (рис. 3.28.б);
- 3-й тип - плотные, гомогенные бляшки с высокой частотой амплитуд гистограммы в полосе интенсивности эхо-сигнала от 19 до 35-40 Дб рис. 3.28.в);
Не лишены любопытства наши наблюдения локализации атеросклеротических бляшек разных типов в каротидном бассейне (рис. 3.29). Так, бляшки 1-го типа в 90% случаев располагались в нижней и средней третях ОСА, в ряде наблюдений циркулярно суживая просвет сосуда на протяжении до 2 см. Бляшки гетерогенной структуры (2-го типа) встречались чаще (83 %) в верхней трети и в области бифуркации ОСА. Атероматозные наложения 3-го (гомогенного) структурного типа в 94% наблюдений локализовались в области бифуркации и в устьях ВСА; такие бляшки в 34% случаев имели концентрическую форму с выступающими в просвет сосуда фрагментами, в 8% - неправильную раковинообразную форму, наиболее вероятно, вследствие изъязвления поверхности бляшки. Среди всех больных с выявленным атеросклерозом сонных артерий у 12% выявлено сочетание бляшек разных структурных типов в одном сосуде и “многоэтажное” поражение ОСА и ВСА.
Важно отметить, что, не найдя прямой зависимости между степенью стенозирова- ния сонных артерий и тяжестью клинических проявлений ХЦВН, мы обнаружили связь между структурными типами атеросклеротического поражения сосудов и особенностями клинической симптоматики. Так, у 173 больных со стенозами ВСА менее 75% при 3-м (плотном, гомогенном) структурном типе бляшек неврологический дефицит наблюдался лишь в 5% случаев, тогда как наличие рыхлых и гетерогенных бляшек у 64% больных сопровождалось неврологическими нарушениями различной тяжести (канд.мед.наук
М.П.Плотников).
С учетом изложенного, при оценке атеросклеротического поражения сонных артерий с помощью В-ангиосканирова- ния, нам представляется целесообразным определять не только степень стенозирования сосудов, но и интенсивность эхо-сигнала, которая характеризует структурные особенности атероматозных наложений, что, в свою очередь, подтверждено почти полным совпадением результатов УЗИ с данными гистоморфологического исследования.
Как было указано выше, в настоящее время дуплексное сканирование сонных артерий (см. рис. 3.22) является главным методом диагностики ка-
ротидных стенозов. Стандартизованное дуплексное УЗИ лежит в основе многоцентровых международных исследований, таких, как “Asymptomatic Carotid Stenosis and Risk of Stroke” (ACSRS) и “Asymptomatic Carotid Surgery Trial” (ACST), в которых мы принимали участие. По мнению некоторых исследователей , по своей диагностической значимости дуплексное УЗИ превосходит ангиографию даже при предоперационном обследовании больных с каротидным атеросклерозом. Вот, что пишет профессор П.Р.Ф.Белл из Великобритании: “ В нашей практике ангиография не выполняется, если только к этому нет специальных показаний, мы полагаемся исключительно на характер поражения по данным дуплексного сканирования. Ангиография назначается, если при дуплексном сканировании имеется проксимальный или дистальный обрыв изображения, и она не производится всем больным. У нас не было проблем при соблюдении данного правила более чем в 300 наблюдениях каротидных эндартерэктомий” .
Дуплексное сканирование позволяет хорошо визуализировать ате- ро-склеротическую бляшку и определять характерные изменения кровотока в области стеноза (рис. 3.30).
При стенозе ВСА на допплерограммах выявляют следующие наиболее важные изменения:
- участок артерии с повышенной скоростью кровотока в области сужения просвета сосуда атеросклеротической бляшкой (рис. 3.30.б);
- участок артерии с турбулент-ным током крови, выражающимся в типичном наложении допплеровских высокочастотных сигналов (связанных с повышением скорости потока) и низкочастотных сигналов (обусловленных вибрацией стенок сосуда) (рис. 3.30.в);
- снижение скорости кровотока в ВСА на 30% и больше по сравнению с контрлатеральной артерией;
- уменьшение диастолической составляющей скорости кровотока в ОСА по сравнению с контрлатеральной артерией.
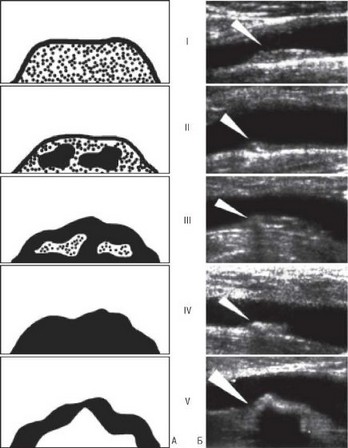
Рис. 3.31. Ультразвуковая классификация атеросклеротических бляшек в сонных артериях. А - схематическое изображение эхоморфоструктуры бляшек; Б - ультразвуковое изображение бляшек (указаны стрелками). Остальные пояснения в тексте.
В современной зарубежной литературе для объединения подобных атеросклеротических поражений сонных артерий определено такое понятие, как “эмбологенный потенциал бляшки с нестабильной морфологической структурой” .
Современные УЗ-приборы 4-5-го поколения оснащены специальными программами компьютерной обработки изображения, позволяющими с высокой точностью измерять акустические параметры эхо-сигнала, что в свою очередь, дает возможность детально анализировать структурные характеристики изучаемого объекта, в частности - морфологические особенности атеросклеротических бляшек .
На основании результатов УЗИ предложены различные классификации каротидных атеросклеротических бляшек. Например, их делят на гомогенные и гетерогенные , выделяют также мягкие, плотные и кальцинированные бляшки. Более прогрессивной представляется классификация, описанная в 1993 г. и нашедшая свое применение в международном многоцентровом исследовании по протоколу ACSRS. В этой
 классификации выделено 5 эхо-типов атеросклеротических бляшек каротидной локализации (рис. 3.31).
классификации выделено 5 эхо-типов атеросклеротических бляшек каротидной локализации (рис. 3.31).
Тип I: однородные эхонегативные (мягкие) бляшки с наличием (или без) эхопозитивной (плотной) покрышки;
Тип II: преимущественно эхонегативные бляшки с более чем 50%- ными эхопозитивными компонентами;
Тип III: преимущественно эхопозитивные бляшки с более чем 50%-ными эхонегативными включениями;
Тип IV: однородные эхопозитивные (плотные) бляшки;
Тип V: бляшки, которые невозможно классифицировать в связи с тем, что обширная кальцификация создает интенсивную акустическую тень.
При клиническом сопоставлении выявлено, что эхопозитивные, плотные фиброзированные бляшки с толстой фиброзной покрышкой чаще
Таблица 3.1.
Соотношение лодыжечно-брахиального индекса (ЛБИ) с тяжестью клинических проявлений артериальной недостаточности нижних конечностей .
Величина ЛБИ, усл.ед. Клинический признак
1,2±0,1 норма
0,6±0,2 перемежающаяся хромота
0,3±0,1 ишемическая боль в покое
- 1 ±0,1 угрожающий некроз тканей

встречаются у асимптомных больных и рассматриваются как бляшки со стабильной морфоструктурой. Бляшки эхонегативные, мягкие, с богатым отложением липидов или с кровоизлияниями, много чаще обнаруживались у больных с симптомами ХЦВН, были связаны с высокой частотой мозговых инсультов .
Эта классификация признана более надежной в динамическом наблюдении за больными с каротидными стенозами по сравнению с объективным неврологическим исследованием, так как предложенные градации атеросклеротических бляшек позволяют лучше идентифицировать каротидные поражения с высоким риском ишемического инсульта .
В заключение остается коротко упомянуть о том, что на сегодняшний день единственным реальным средством устранения стеноза и профилактики инсульта остается операция каротидной эндартерэктомии, одним из аспектов которой является проблема рестенозов. При этом показано, что в течение двух лет после операции рестеноз обычно связан с гиперплазией эндотелия и гладкомышечных клеток интимы, а в более поздние сроки - с новообразующейся атеросклеротической бляшкой . В свя-
В
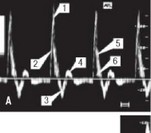
Рис. 3.33. Пример ультразвуковой спектрограммы бедренной (А), подко-ленной (Б) и задней большеберцовой (В) артерий здорового человека.
- - систолический пик; волны спектро-граммы прямого (2), обратного (3) и отраженного (4) кровотока; 5 - полоса частот огибающей спектрограммы; 6 - систолическое “окно".
зи этим, вполне очевидно, что в длительном послеоперационном наблюдении за такими пациентами методом выбора является качественное дуплексное УЗИ сонных артерий.
УЗИ брюшной аорты и магистральных артерий нижних конечностей позволяет определять уровень сегментарной окклюзии, тяжесть сте- нозирующего поражения сосудов и выраженность нарушений регионарного кровообращения у больных ОАНК.
В ангиохирургической практике наиболее распространенной является УЗ-допплерогра- фия (флуометрия), которая дает возможность оценить пульсовой кровоток, систолическое давление (рис. 3.32) и скорость кровотока по артериям. При ОААНК важным диагностическим показателем является уровень регионарного систолического давления в разных сегментах конеч-ностей по сравнению с величиной АД в плечевой артерии.
Исследование выполняют при горизонтальном положении больного. Манжету сфигмома- нометра шириной 18 см накладывают на исследуемый участок конечности (бедро, голень); УЗ-датчик устанавливают в проекции артерии под углом 45° в сторону притока крови; появление первого сигнала при выпускании воздуха из манжеты указывает величину систолического АД в данном сегменте. Аналогично измеряют давление в плечевых артериях, после чего вычисляют индекс регионарного систолического давления, как отношение давления в сегменте ноги к величине давления в брахиальной артерии. У здоровых людей этот индекс, как правило, превышает 1,0.
У больных ОААНК при ишемии II степени индекс давления на бедре колеблется от 0,9 до
- 8. Лодыжечно-брахиальный индекс (ЛБИ) понижается примерно до 0,7. При ишемии III степени ЛБИ снижается до 0,5. При ишемии
- степени ЛБИ падает до 0,3 и ниже . Иными словами, при окклюзирующем поражении Рис. 3.34. артерий нижних конечностей снижение ЛБИ
брюш-HoiA аорты (АО) Графическая регистрация Д-УЗИ позволя-
здорового человека в
продольной (А) и
поперечной (Б)
проекциях.
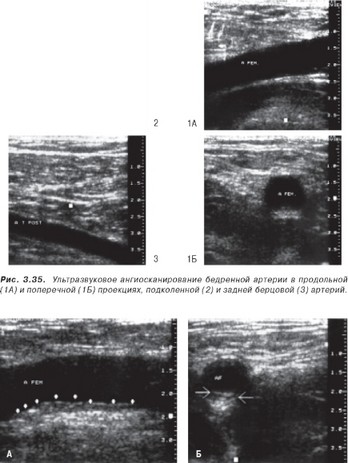
Рис. 3.36. Ультразвуковое изображение атеросклеротической бляшки (указана стрелками) в бедренной артерии при продольном (А) и поперечном (Б) сканировании.
ет оценивать качественные и количественные характеристики кровотока в сосудах конечностей (рис. 3.21, 3.33). Качественная характеристика включает оценку огибающей спектрограммы, величину спектрального расширения. В норме имеются 3 волны спектрограммы: прямого, обратного и отраженного кровотока; узкая полоса частот располагается вдоль огибающей спектрограммы, под систолическим пиком формируется “окно” (рис. 3.33).
![]() При окклюзии аортоподвздошного сегмента на спектрограмме бедренной артерии регистрируется нарушение формы огибающей, исчезновение обратного и отраженного кровотока, увеличение времени подъема кривой и снижение пиковой систолической частоты. Такие же изменения наблюдаются в кровотоке по подколенной артерии у больных с окклюзией бедренного сегмента.
При окклюзии аортоподвздошного сегмента на спектрограмме бедренной артерии регистрируется нарушение формы огибающей, исчезновение обратного и отраженного кровотока, увеличение времени подъема кривой и снижение пиковой систолической частоты. Такие же изменения наблюдаются в кровотоке по подколенной артерии у больных с окклюзией бедренного сегмента.
При стенозе подвздошной, бедренной артерии на спектрограммах с дистальных сосудов отмечаются притупление вершины, исчезновение волны обратного кровотока, снижение пиковой систолической частоты
Метод В-сканирования дает возможность визуальной оценки атеросклеротического поражения брюшной аорты и ее магистральных ветвей.
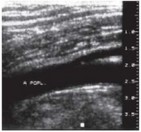
По литературным данным, использование УЗ-ангиоскани- рования позволяет получить изображение аорты у всех здоровых лиц. Сканирование в продольной плоскости, так же как и в поперечной, дает воз- Рис. 3.37. узи общей бедренной (А), можность изучать аорту на мак-
подколен-ной (Б) и задней большеберцовой симальном протяжении. При
(В) артерий здорового человека в режиме этом аорта имеет вид трубчатой
дуплексного сканирования.
структуры, постепенно суживающейся в дистальном направлении. В норме у стенок аорты гладкий, ровный контур, их толщина не превышает 3 мм. Стенка аорты значительно толще стенки, расположенной рядом нижней полой вены. В обеих плоскостях сканирования просвет аорты (диаметром 2,0-2,4 см) однороден, не содержит никаких включений и отраженных сигналов, имеет темный цвет (рис. 3.34). Отличительной особенностью аорты является отчетливо видимая при В-ска- нировании пульсация на всем протяжении аорты, совпадающая с сердечными сокращениями.
При поперечном сканировании в области бифуркации аорты по обе стороны позвоночника можно различить два небольших, диаметром 1,11,2 см, округлых пульсирующих образования - общие подвздошные артерии.
Подвздошные артерии как справа, так и слева, прослеживаются на протяжении 6-8 см в дистальном направлении от бифуркации аорты. Они имеют вид трубчатых структур с ровными, гладкими контурами внутрен-
1
2
А
Б
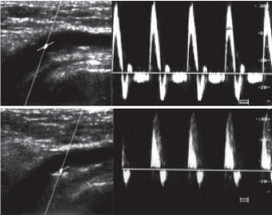
Рис. 3.38. Дуплексное сканирование нестенозирующего атеросклероза бедренной артерии.
- - метка установлена в центральной части просвета сосуда. Амплитуда и конфигурация спектрограммы кровотока (А) не отличается от нормы (см. рис. 3.33.А).
- - метка установлена над бляшкой. На допплерограмме (Б) регистрируется уменьшение скорости и турбулентный характер кровотока: снижение систолического пика, расширение спектра частот, исчезновение “окна" и волны отраженного кровотока.
ней поверхности стенок и отчетливо видимую пульсацию. Диаметр общих подвздошных артерий равен 1,1±0,1 см, а наружных подвздошных
- 0,9±0,1 см .
Пораженные атеросклерозом стенки периферических артерий имеют неровные контуры (рис. 3.36). Отражающая способность их различна: максимальный эхосигнал дают кальцинированные бляшки, остальные участки стенки имеют меньшую интенсивность отражения, однако она всегда выше, чем у стенок непораженного сосуда.
В местах стенозирования артерий, как правило, хорошо видны участки кальциноза стенки, которые отличаются более высокой эхоплотно- стью. Однако в отличие от полной окклюзии всегда сохранен просвет сосуда.
При стенозах наблюдается феномен исчезновения пульсации стенок артерии. Локальные стенозы обусловливают трудноразличимое исчезновение пульсации на небольшом участке артерии. В случае протяженного стеноза хорошо заметно снижение пульсации при приближении к зоне стеноза
Для исследования брюшной аорты, чревной, мезентериальных и почечных артерий используем конвексный датчик 2.5-5 МГц.
Нажимайте на картинки, чтобы увеличить.
 |
|
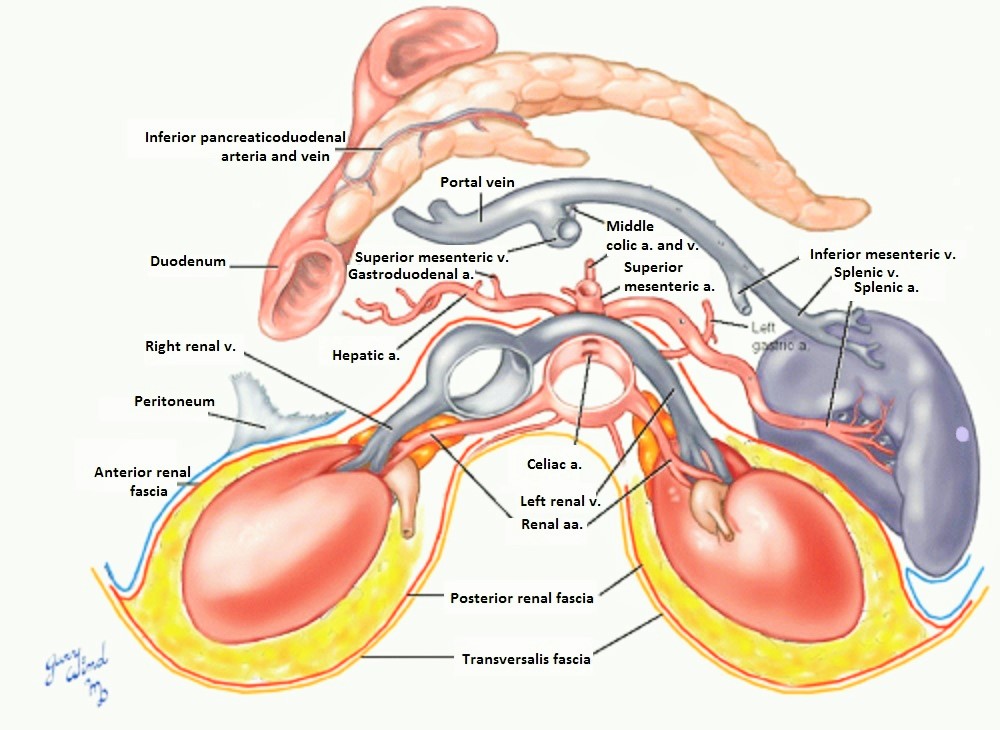
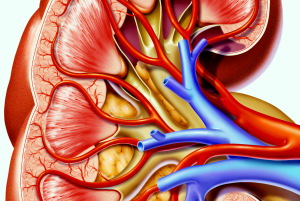
| Фото. Почечные артерии отходят от брюшной аорты чуть ниже верхней брыжеечной артерии — на уровне II поясничного позвонка. Кпереди от почечной артерией располагается почечная вена, в воротах почки оба сосуды находятся кпереди от почечной лоханки. Правая почечная артерия — это единственный крупный сосуд, который проходит позади нижней полой вены. Левая почечная вена проходит через «пинцет» между аортой и верхней брыжеечной артерией. Часто встречается кольцевидная левая почечная вена, когда одна ветвь располагается впереди, а другая — позади аорты. | |
Сначала оценим размеры почки, толщину паренхимы, состояние чашечно-лоханочного комплекса. Далее проследим аорту от чревного ствола до бифуркации при в режимах серой шкалы и ЦДК. При наличии атеросклеротических бляшек в аорте, вероятен стеноз устьев почечной артерии, особенно у пожилых или больных сахарным диабетом. Если возможно, найдите почечные артерии на поперечном срезе аорты при сканировании через переднюю стенку живота, двигая датчик от верхней брыжеечной артерии вдоль аорты. Правую почечную артерию найти проще, чем левую. Проследим ее ход от аорты до ворот почки, где она делится на сегментарные ветви. Левую почечную артерию лучше видно в положении на боку. Тщательно осмотрите брюшную аорту и почки, чтобы выявить добавочные ветви почечных артерий из нижних отделов аорты или подвздошных артерий.
 |
 |
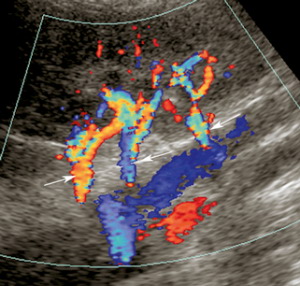 |
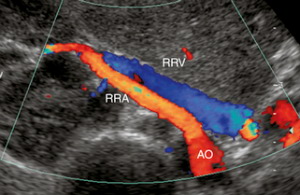
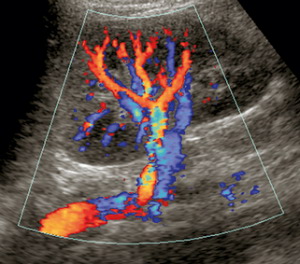
| Фото. А — При ЦДК видно, что от аорты (АО) отходит правая почечная артерия (RRА) и направляется к воротам почки; спереди от правой почечной артерии располагается правая почечная вена (RRV). Акустическим окном служит паренхима печени. Б — При ЦДК в положении на правом боку акустическим окном служит левая почка — хорошо видно как левая почечная артерия и вена в воротах почки делятся на сегментарные и междолевые сосуды. В — Несколько добавочных почечных артерий (стрелки) идут к левой почке. | ||
 |
 |
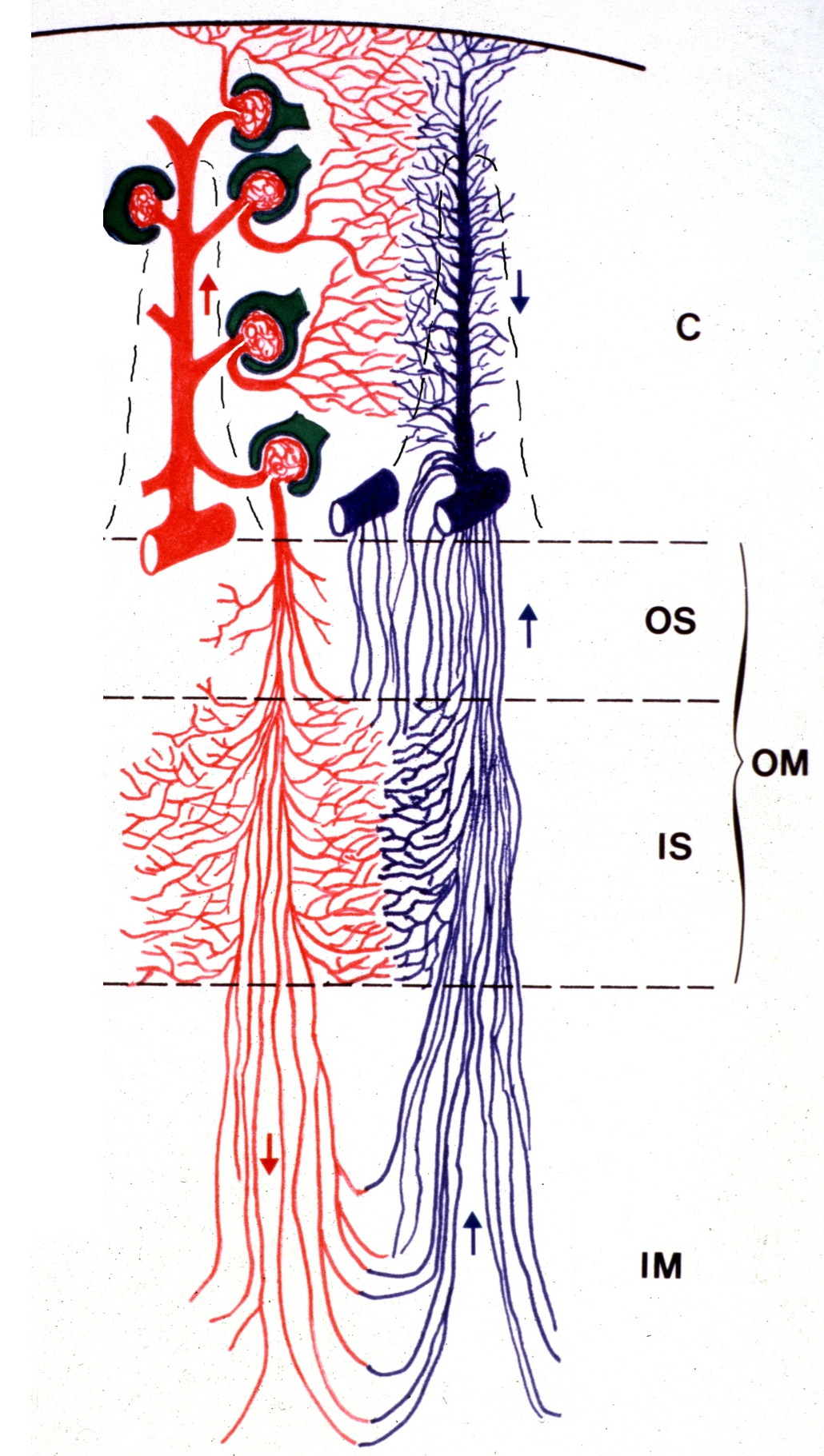 |
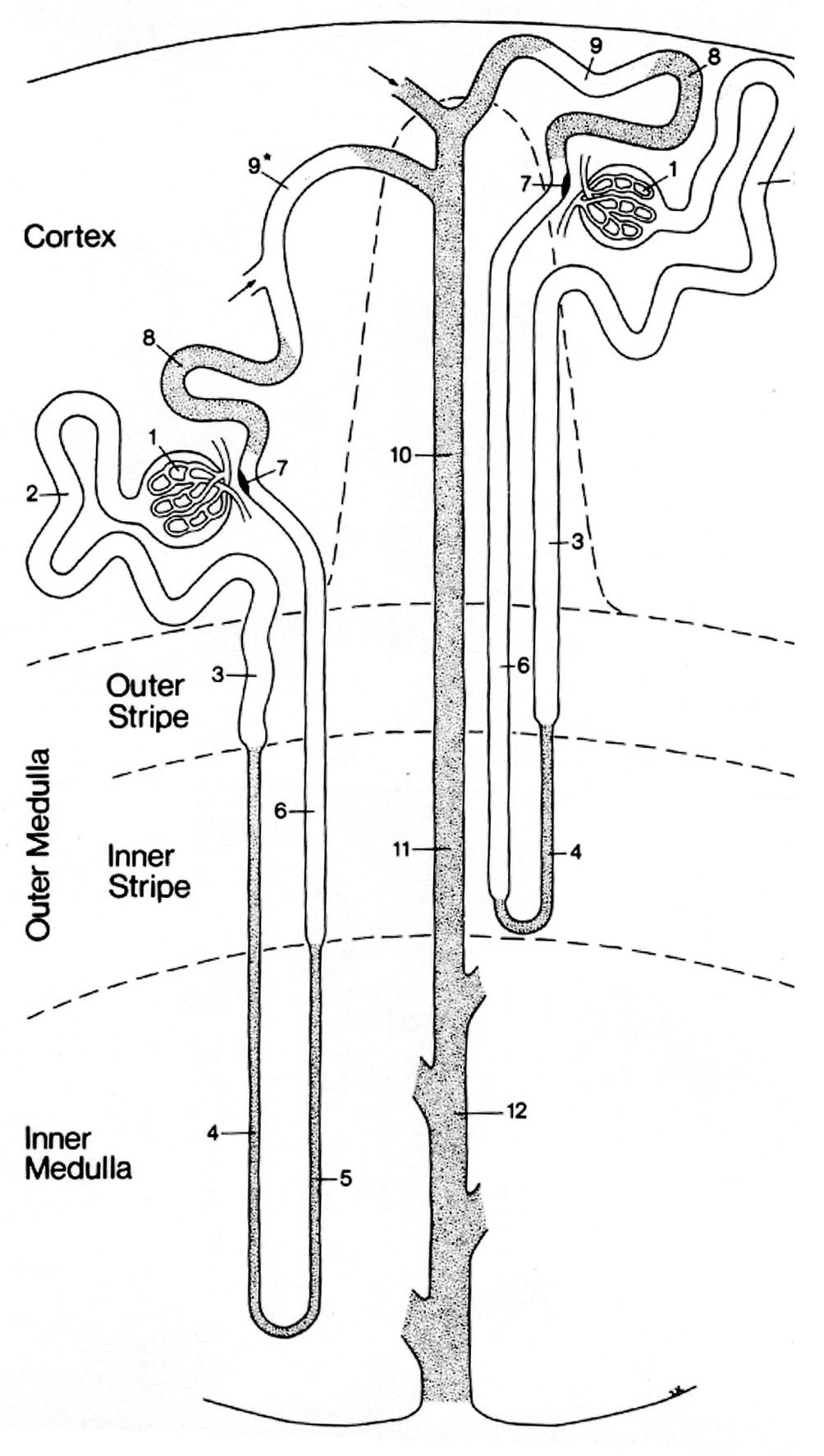
| Фото. А — В воротах почки главная почечная артерия делится на пять сегментарных: задняя, верхушечная, верхняя, средняя и нижняя. Сегментарные артерии проходят через синус и разделяются на междолевые артерии, которые располагаются между пирамидами в паренхиме почки. Междолевые артерии продолжаются в дугообразные (аа. arcuatae) → междольковые (аа. interlobular) → приносящие артериолы клубочков (vas afferens) → капиллярные клубочки (glomeruli). Кровь от клубочка оттекает в выносящие артерии, из которых формируются прямые венулы (venulae rectae) и междольковые вены (venae interlobulares). Междольковые вены и прямые венулы образуют дуговые вены (vv. arcuatae). Затем кровь поступает в междолевые (vv.interlobares) → сегментарные (vv. segmentares) → почечные вены (v. renales) → нижнюю полую вену. | ||
Следует оценить почечную артерию при выходе из аорты, в проксимальном, среднем и дистальном сегменте, а так же верхушечную, среднюю и нижнюю сегментарные артерий. Как минимум, в семи точках с обеих сторон проводим спектральный анализ доплеровской кривой. О бращайте внимание на высокоскоростной поток и турбулентность, так как они могут быть связаны со стенозом.
Важно!!! Угол между плоскостью сканирования и сосудом должен быть от 30° до 60°.
Оцениваем пиковую систолическую (PSV) и конечно-диастолическую (EDV) скорости кровотока, а также время ускорения (Ao AT). Пиковая систолическая (PSV) и конечная диастолическая (EDV) скорости определяются на вершине высочайшего систолического пика и в конце диастолы, соответственно. Время ускорения (Ao AT) определяется от начала систолического движения до высочайшего систолического пика. Систолическое ускорение (Ao Accel) определяется путем деления пикового систолического изменения скорости кровотока на время ускорения. Индекс резистентности (RI) = (пиковая систолическая скорость кровотока — скорость кровотока в конце диастолы) / пиковая систолическая скорость кровотока.
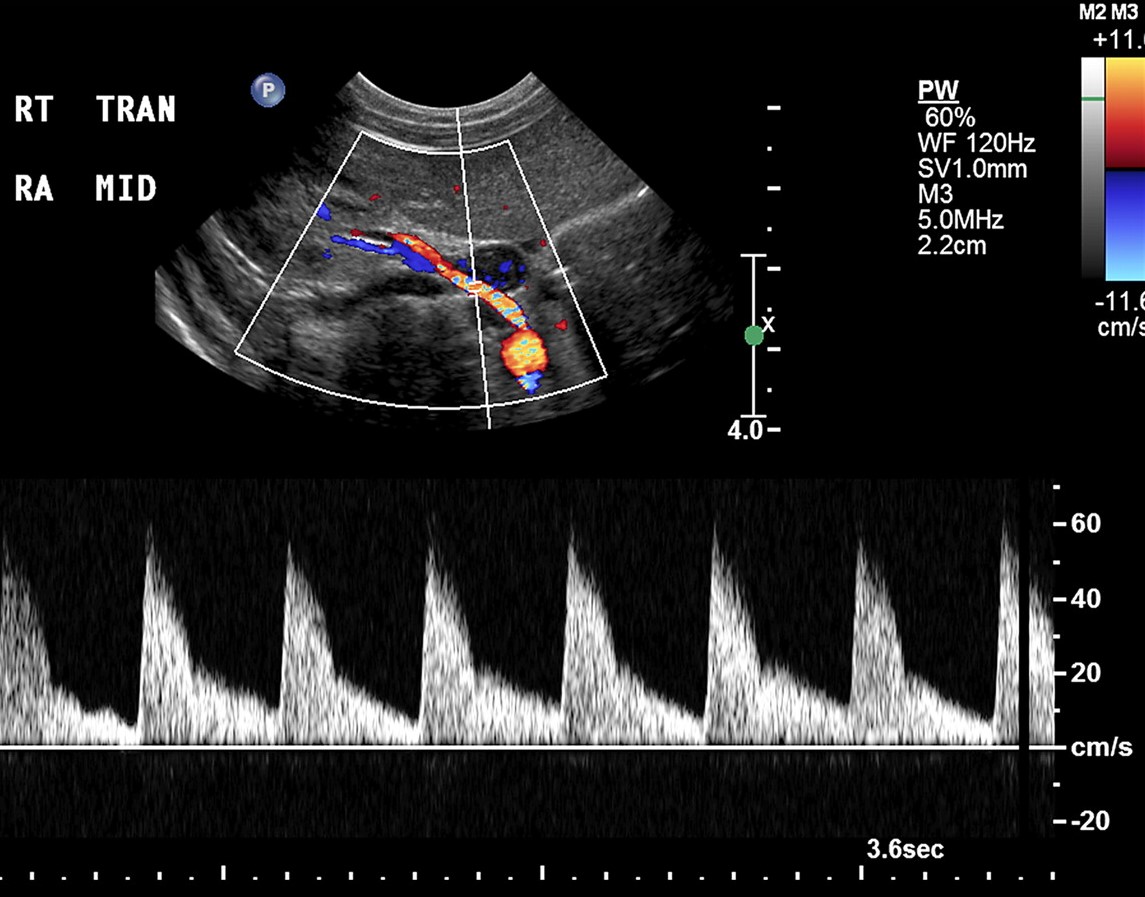
Нормальный спектр почечных артерий и сосудов паренхимы почек имеет выраженный систолический пик с антеградным диастолическим потоком на протяжении всего сердечного цикла. В норме у взрослых пиковая систолическая скорость (PSV) в почечной артерии 100-180 см/с, конечно-диастолическая скорость (EDV) — 25-50 см/с; RI на главной почечной артерии в области ворот почки должен быть менее 0.7, а на междолевых артериях 0.34-0.74, разница RI правой и левой почки не превышает 0,05.
 |
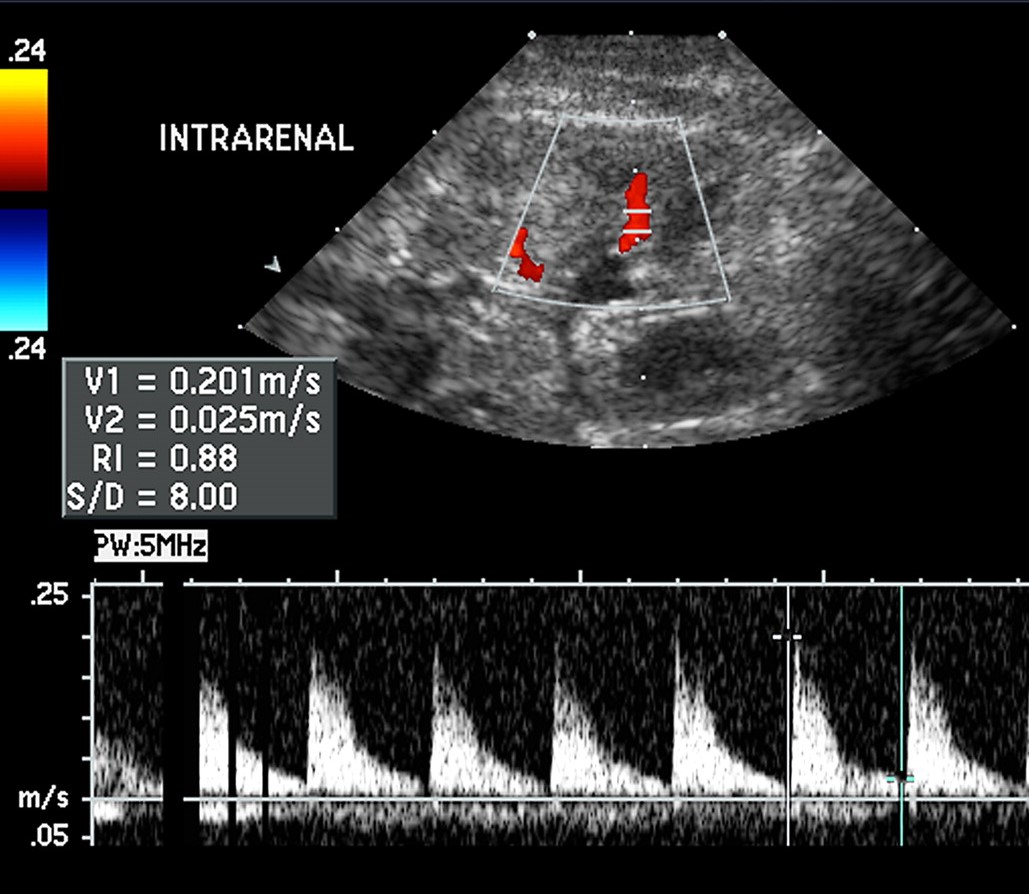 |
| Фото. A — Спектр от средней части правой почечной артерии у 2-дневной девочки демонстрирует выраженный систолический пик с антеградным потоком по всей диастоле. B — Спектр от внутрипочечной артерии у недоношенной 26-дневной девочки показывает относительно высокое сопротивление (RI 0,88), которое считается нормальным для недоношенных новорожденных. | |
Гемодинамически значимый стеноз почечной артерии, как правило, определяется при уменьшении диаметра на 50-60%. Критерии для диагностики гемодинамически значимого стеноза почечной артерии:
- Пиковая систолическая скорость в почечной артерии 180-200 см/сек или более;
- Соотношение пика систолы в почечной артерии и пика систолы в аорте на уровне почечной артерии (RAR) превышает 3.3;
Важно!!! Молодые пациенты без стеноза могут иметь высокие (выше 180 см/сек) значения систолического пика аорты и ее ветвей. Пожилые пациенты с тяжелой сердечной недостаточностью и плохим сердечным выбросом могут иметь низкий систолический пик даже в области стеноза. Соотношение пика систолы в почечной артерии и пика систолы в аорте на уровне почечной артерии позволяет нивелировать эти особенности.
- При стенозе почечной артерии кровоток в дистальных отделах (внутрипочечные сосуды) затухает — “tardus-parvus” эффект. Tardus означает медленно или поздно, а parvus мелко или мало. Tardus указывает, что систолическое ускорение медленное и время для достижения пиковой систолической скорости увеличивается. Parvus указывает на то, что систолический пик имеет низкую высоту, что означает медленную скорость потока. Индекс ускорения менее 300 см/сек 2 или время разгона свыше 0,07 секунд считается ненормальным и указывает на стеноз почечной артерии в 60% случаев. Некоторые авторы используют ускорение 0,10 или 0,12 секунды как отсечку для значимых стенозов, что повышает специфичность.
- Соотношение пиковой систолической скорости почечной и междолевой артерий (RIR) не должно превышать 5.
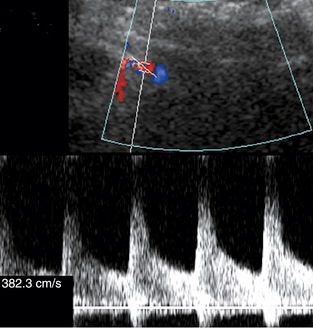
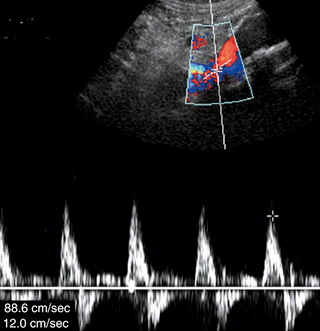
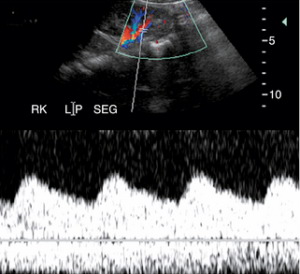
| Фото. Стеноз правой почечной артерии при доплерографии. А — Повышена пиковая систолическая скорость почечной артерии — 382,3 см/сек. Б — Пиковая систолическая скорость аорты на уровне почечных артерий — 88.6 см/сек. Почечно-аортальное соотношение составляет 4,3, что указывает на значимый стеноз почечной артерии. В — На внутрипочечных сегментарных артериях имеется демпфирование сигнала — характерна кривая tardus-parvus. Обратите внимание на округлый контур раннего систолического пика и продолжительное систолическое время разгона. | ||
 |
 |
 |
Важно!!! Стеноз почечной артерии можно заподозрить по косвенным признакам — затухание допплеровского сигнал в сегментарных или междолевых артериях. Оценка внутрипочечного кровотока — это легкий, точный и быстрый способ выявления почечного стеноза.
Но нельзя использовать единственно этот метод. Форма кривых при доплере внутрипочечных артерий зависит от эластичности сосудов, резистентности микроциркуляторного русла, а также от входящего тока крови. У пациентов с изменениями в мелких сосудах почек, например, при диабетической нефропатии, феномен затухания сигнала во внутрипочечных сосудах даже при высоком уровне стеноза почечной артерии может быть уничтожен. Наоборот, затухающие внутрипочечные волны можно увидеть в отсутствии значимого стеноза почечной артерии у больных с аортальным стенозом или окклюзией аорты.
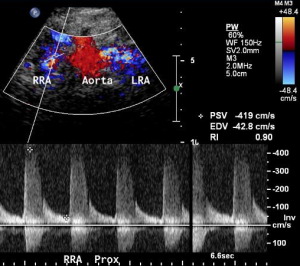
| Фото. А — Стеноз почечной артерии слева: пиковая систолическая скорость — 419 см/сек, конечная диастолическая скорость — 42,8 см/сек, индекс резистентности — 0,9. Б — Пиковая систолическая скорость в левой почечной артерии 282 см/сек, что указывает на стеноз. Обратите внимание (рисунок В), доплер внутрипочечных сосудов на вид нормальный. Стеноз был подтвержден при магнитно-резонансной ангиографии. | ||
 |
 |
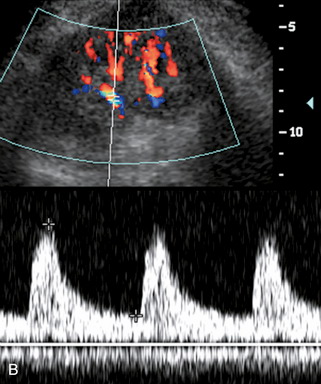 |
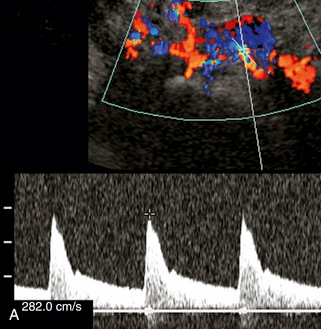
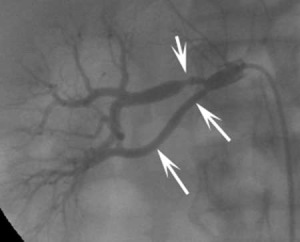
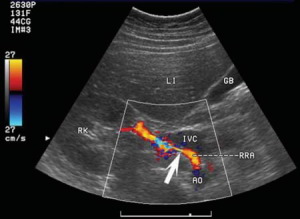
| Фото. Выраженный стеноз правой почечной артерии у молодого мужчины: А — На ангиограмме выраженный стеноз в среднем сегменте правой главной почечной артерии (толстая стрелка) и добавочная артерия (тонкие стрелки). Б — Пиковая систолическая скорость на почечной артерии всего 111 см/сек — спектральный доплер не видит стеноза. В — На цветном доплере заметно сужение правой почечной артерии (стрелка). AO — аорта; GB — желчный пузырь; IVC — нижняя полая вена; LI — печень; РК — правая почка; RRA — правая почечная артерия. | ||
 |
 |
 |
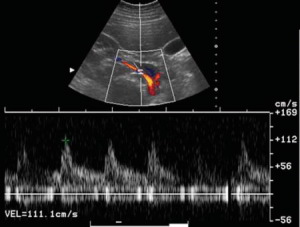
| Фото. Выраженный стеноз среднего сегмента правой почечной артерии у пожилой женщины. А — Пиковая систолическая скорость (PSV) на почечной артерии 438 см/сек, почечно-аортальное соотношение 5,1 (438/86). Б — Спектральный анализ междолевой артерии показывает типичные для стеноза изменения: низкая PSV — 14 см/сек; время систолического ускорения 0,18 секунды, IR 0,43, соотношение почечная/междолевая артерии (RIR) 438/14=31,3. В — На ангиографии стеноз в среднем сегменте правой почечной артерии подтвержден. | ||
 |
 |
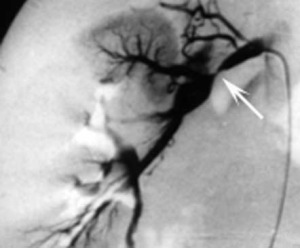 |
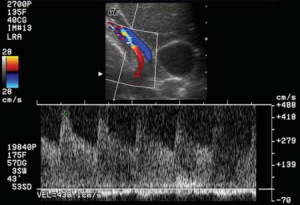
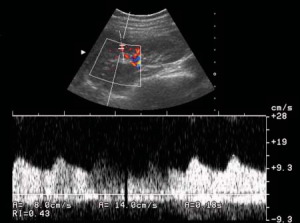
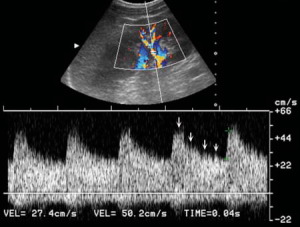
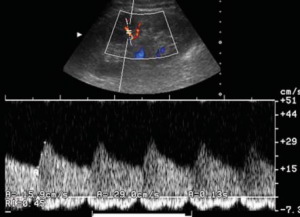
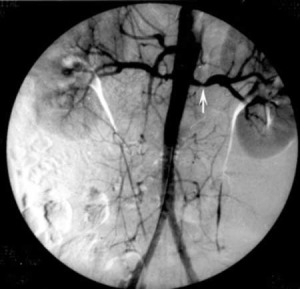
| Фото. При спектральной доплерографии почек у пожилого мужчины выявили изменения на уровне внутрипочечных артерий: A — Спектральный анализ сегментарной артерии показывает турбулентный и хаотичным характер тока крови — всплески сигнала по контуру (стрелки), но время систолического ускорения не изменено — 0,04 секунды. B — На междолевой артерии поток крови ламинарный — гладкий контур, но время систолического ускорения увеличено — 0,13 секунды. C — Ангиография показывает выраженный стеноз среднего сегмента левой почечной артерии. | ||
 |
 |
 |

