علائم درمان هتروتوپی ماده خاکستری هتروتوپی زیر قشری: لیسنسفالی
کلید واژه ها:صرع، دیسپلازی کانونی قشر مغز، هتروتوپی ماده خاکستری، کورتیکوگرافی
هدفبررسی نتایج درمان جراحی صرع در بیماران مبتلا به اختلال در مهاجرت نورون ها در قشر مغز.
مواد و روش ها: بر روی 4 بیمار 20 تا 37 ساله (2 مرد و 2 زن) مبتلا به صرع ناشی از اختلالات رشدی مختلف قشر مغز جراحی شده است.
نتایجهمه بیماران در تصویر بالینی به مدت 6 تا 22 سال قبل از بستری شدن در بیمارستان دچار تشنج نسبی با جنرالیزاسیون ثانویه بودند. MRI مغز در سه بیمار دیسپلازی کانونی قشر مغز و در یک بیمار هتروتوپی اطراف بطنی منتشر ماده خاکستری مغز را نشان داد. سه بیمار مبتلا به FCD تحت کاشت الکترودهای کورتیکوگرافی برای تعیین ناحیه قشر مسئول ایجاد تشنج قرار گرفتند. بیماران مبتلا به FCD تحت تاپکتومی ضایعات با کورتیکوگرافی حین عمل، بیمار مبتلا به هتروتوپی اطراف بطنی تحت لوبکتومی لوب فرونتال راست قرار گرفتند. عوارض عفونی و عصبی پس از مداخلات مشاهده نشد. بررسی مورفولوژیکی آمادهسازیها FCD نوع تیلور را در 2 بیمار، FCD نوع غیر تیلور را در یک بیمار، و هتروتوپی ماده خاکستری اطراف بطنی را در یک بیمار نشان داد. پس از 12 ماه در دوره پس از عمل، در سه بیمار مبتلا به FCD، نتیجه درمان جراحی به عنوان کلاس IA بر اساس مقیاس انگل (رهایی کامل از تشنج)، در بیمار مبتلا به هتروتوپی ماده خاکستری - II بر اساس مقیاس انگل ارزیابی شد. (کاهش دفعات تشنج تا 50 درصد)
نتیجه گیری. در بیماران مبتلا به صرع مقاوم به دارو، لازم است نقش اتیوپاتوژنتیک احتمالی اختلالات در مهاجرت نورون های قشر مغز در نظر گرفته شود. درمان جراحی ممکن است گزینه ای برای دستیابی به بهبودی بالینی پایدار و سازگاری اجتماعی بیماران باشد.
شیزنسفالی یک ناهنجاری در ساختار قشر مغز است. این به دلیل نقض رشد مغز در هفته 2-5 بارداری رخ می دهد. این بیماری با اختلال در مهاجرت نورون ها به قشر مغز در طول تشکیل شبکه های عصبی مغز همراه است.
محتوا:
اسکیزنسفالی چیست؟
به دلیل تغذیه ناکافی عروقی یا عدم وجود آن، بخشی از بافت مغز تشکیل نمی شود. شیزنسفالی فرآیند تخریب بافت نیست، بلکه نتیجه توسعه نیافتگی آن است (یک نقص خطی در بافت مغز که با عدم وجود سلول های ماده خاکستری مشخص می شود).
سن متوسط شروع علائم 4 سال (محدوده 3-4 هفته تا 12 سال) است.
اسکیزنسفالی دو نوع است.
شکاف بسته - 1 نوع.با یک بخش خطی یک طرفه یا دو طرفه از قشر مغز با ساختار ناقص مشخص می شود. دیواره های شکاف بسته می شوند، بطن ها با فضای زیر عنکبوتیه ارتباط برقرار می کنند. حفره شکاف یک شیار کوچک است که با اپیتلیوم اپاندیمی و مننژهای عنکبوتیه پوشیده شده است. با مایع مغزی نخاعی پر نمی شود، بنابراین تشخیص آسیب شناسی در دوره قبل از تولد در نورسونوگرافی غیرممکن است.
شکاف باز (باز) - نوع 2.در یک یا هر دو طرف دیده می شود. دیواره های نقص توسط یک لومن پر از CSF از یکدیگر جدا می شوند. طول آن: از دیواره بطن ها تا فضای زیر عنکبوتیه. در سونوگرافی، اسکیزنسفالی باز با افزایش بطن ها تشخیص داده می شود.
علائم
اسکیزنسفالی بسته بیش از 50 درصد از همه موارد تشخیص داده شده را تشکیل می دهد. در 30 درصد موارد، بیماری با هیدروسفالی پیشرونده ترکیب می شود که با شانت بطنی از بین می رود.تعداد و شدت علائم بستگی به نوع اسکیزنسفالی دارد: یک طرفه یا دو طرفه، به محلی شدن نقص قشر مغز.
یک جانبهشکاف باعث فلج، فلج جزئی یا کامل در یک طرف بدن می شود. اکثر بچه ها وقتی بزرگ می شوند، توانایی های ذهنی متوسطی دارند، سطح توانایی های بدنی نزدیک به نرمال است.
علائم اسکیزنسفالی بسته یک طرفه در اکثر بیماران به چنین اختلالات رشدی محدود می شود: عدم ابتکار عمل، عقب ماندن از کودکان همسن از نظر ذهنی و جسمی (بدیهی است در طول بازی های مشترک)، اختلالات درک گفتار متوسط. اختلال در هماهنگی حرکات در سمت بدن مقابل ناحیه آسیب دیده مشاهده می شود.
دو طرفهشکاف ها علائم شدیدتری دارند: تاخیر در رشد جسمی و ذهنی، مشکلات در یادگیری زبان و آموزش دروس پایه در مدرسه. به دلیل اتصالات ناقص بین مغز و نخاع، محدودیت عملکرد حرکتی امکان پذیر است. ناهماهنگی دوطرفه با اسکیزنسفالی دو طرفه (دوطرفه) حتی با اندازه کوچک شکاف ها امکان پذیر است.
سایر علائم شیزنزفالیا:
- تون عضلانی کم؛
- هیدروسفالی (انباشت مایع در بطن های مغز)؛
- میکروسفالی (سر کوچکتر از حد طبیعی)، گاهی اوقات ماکروسفالی (به دلیل هیدروسفالی)؛
- تشنج های مکرر
دور سر نوزاد زیر یک سال مبتلا به هیدروسفالی به جای 40 سانتی متر طبیعی در 3 ماهگی و 47 سانتی متر در سال به 50 تا 75 سانتی متر افزایش می یابد.
همه کودکان مبتلا به اسکیزنسفالی با صرع کانونی تشخیص داده می شوند.(منطقه به وضوح تعریف شده از epiactivity).
انواع تشنج:
- تشنج های کانونی پیچیده - تاری هوشیاری، چرخش سر، تثبیت بی حرکت نگاه، میوکلونوس (انقباض عضلات تشنجی) اندام تحتانی. معمولا فقط در یک طرف بدن دیده می شود.
- تشنج های پیچیده با تعمیم ثانویه (پیش از تشنج اورا یا کانونی).
- تشنج های ساده
تشنجهای میوکلونیک (انقباضات ریتمیک گروههای عضلانی که حرکات غیرارادی را تحریک میکنند) و تشنجهای تونیک (آرامش غیرمنتظره عضلانی) کمتر شایع هستند. آنها می توانند 4-8 بار در ماه یا کمتر عود کنند، گاهی اوقات فقط چند بار در طول زندگی رخ می دهند.
فراوانی و شدت حملات صرعبه نوع شیزنسفالی بستگی ندارد، بلکه به وجود بخش هایی از دیسپلازی قشر مغز (ساختار غیر طبیعی قشر مغز) بستگی دارد.
در 100٪ موارد، شیزنسفالی با نقض عملکردهای بالاتر قشر مغز مشخص می شود:بینایی، شنوایی، حساسیت (بو، لمس، مزه) با شدت های مختلف. اختلالات حرکتی با لوکالیشن پیشانی شکاف ها آشکارتر می شود.
اسکیزنسفالی به ندرت یک آسیب شناسی مستقل است. معمولا شناسایی می شود در ترکیب با گروهی از ناهنجاری ها، همچنین در نتیجه نقض فرآیندهای انتوژنز (توسعه بدن) در دوران بارداری ایجاد شده است:
- دیسژنزیس(توسعه نیافتگی) یا عدم وجود جسم پینه ای؛
- بطن کولومگالی(بزرگ شدن بطن ها با نقض خروج مایع مغزی نخاعی)؛
- هیپوپلازی مخچه(مسئول عملکردهای حرکتی و هماهنگی)؛
- پلی میکروژیریا(پیچش های اضافی زیاد، ترتیب نادرست لایه های قشر مغز)؛
- هتروتوپی ماده خاکستری(انباشت غیر طبیعی و محلی سازی نادرست)؛
- اتساع(جابه جایی) یا نقص دیوار، توسعه نیافتگی شاخ بطن های مغز.
تصویر بالینی اسکیزنسفالی با پیامدهای نقص مغز تکمیل می شود:
- شکل هیدروسفالی سر (پیشانی غیرطبیعی بالا، قسمت فوقانی بزرگ شده جمجمه، برآمدگی های فوقانی به شدت مشخص شده و به سمت جلو منتقل شده، الگوی وریدی به شدت برجسته روی پیشانی)؛
- نقض عصب عضلات که حرکت کره چشم، عضلات داخلی چشم و پلک ها را تضمین می کند.
- حالات غیر طبیعی صورت یا عدم وجود آن به دلیل عصب دهی نامناسب عضلات صورت.
- فلج پیازی (اختلال در گفتار، بلع، ناتوانی در کنترل (حرکت) عضلات صورت)؛
- افزایش تون عضلانی؛
- تتراپارزی اسپاستیک (پارزی تمام اندام ها، عدم تقارن و اختلال در تون عضلانی)؛
- عدم وجود یا نقض رفلکس های بدون قید و شرط؛
گاهی اوقات علائم عصبی اسکیزنسفالی کمتر از آن چیزی است که پزشکان در ابتدا از MRI شک می کنند.
چه چیزی باعث اسکیزنسفالی می شود؟
علت دقیق اسکیزنسفالی مشخص نشده است. اکثر محققان نظریه های مرتبط با اختلالات ژنتیکی و عروقی را مطرح می کنند.
جهش در ژن های هومئوباکس مسئول رشد و مهاجرت نوروبلاست ها (پیش ساز نورون ها) در بسیاری از کودکان مبتلا به اسکیزنسفالی، اما نه همه آنها، دیده می شود. تئوری ژنتیکی وقوع توسط موارد اسکیزنسفالی در خواهر و برادر پشتیبانی می شود.
توسعه بیماری ممکن است تحت تأثیر قرار گیرد عفونت ها (به عنوان مثال، سیتومگالوویروس) و داروها .
چه فرآیندهایی باعث ظهور فضا در ماده خاکستری می شود؟
برخی دیگر نظر متفاوتی دارند: شکاف در ماده خاکستری در نتیجه ایجاد می شود انسداد عروق . انسداد یا عدم وجود شریان های کاروتید داخلی یا میانی مغز منجر به سکته مغزی ایسکمیک و متعاقباً نکروز مغزی می شود.
تشخیص
معاینه و درمان علامتی در بخش روانی-عصبی انجام می شود.پزشکان از روش های تشخیص ابزاری زیر استفاده می کنند:
- تصویربرداری رزونانس مغناطیسی.
- توموگرافی کامپیوتری اشعه ایکس.
- الکتروانسفالوگرافی با آزمایش هایی با باز و بسته کردن چشم ها، تحریک نوری و هیپرونتیلاسیون تکمیل می شود (از کودک خواسته می شود دم و بازدم سریع و عمیق انجام دهد).
در تمام کودکان مبتلا به اسکیزنسفالی، EEG کندی در فعالیت پس زمینه و همچنین یکی از دو تغییر را نشان می دهد:
- فعالیت صرع موضعی در مناطق فرونتوتمپورال.
- فعالیت صرعی در همه جا بدون تمرکز خاص.
به دلیل وجود هیدروسفالی، اسکیزنسفالی باز مشابه است پورانسفالی اما در حالت دوم، شکاف با اپیتلیال پوشانده نمی شود، بلکه با بافت همبند یا گلیال (کمکی) پوشیده می شود. ممکن است این بیماری با آن اشتباه گرفته شود هولوپروسسفالی (عدم تقسیم کامل یا جزئی مغز جلویی به نیمکره ها).
سی تی به ندرت در تشخیص اسکیزنسفالی استفاده می شود، زیرا MRI تصویر کامل تری از آسیب شناسی ارائه می دهد.

با کمک تصویربرداری رزونانس مغناطیسی، اختلالات همزمان رشد مغز شناسایی می شود:
- هتروتوپی ماده خاکستری (گره هایی در ماده خاکستری زیر پوشش بطن ها)؛
- هیپوپلازی عصب بینایی (تعداد کافی آکسون، واحدهای ساختاری نورون ها)؛
- آژنز سپتوم پلوسیدوم در محلی سازی فرونتال اسکیزنسفالی.
- دیسپلازی سپتو-اپتیک (اختلالات رشدی غده هیپوفیز، سپتوم پلوسیدوم، عصب بینایی).
رفتار
درمان علامتی اسکیزنسفالی ارائه می شود.
تتراپارزی، همی پارزی، تشنج، اسپاسم عضلانی، عقب ماندگی روانی حرکتی، با تحریک الکتریکی یا میکروپلاریزاسیون مغز درمان می شود، روان درمانی، داروهای ضد صرع، درمان بوتولینوم (مسدود کردن انتقال سیگنال های ناخواسته از اعصاب به عضلات)، درمان ارتوپدی استفاده می شود.
بیماران مبتلا به اسکیزنسفالی خفیف پس از شروع درمان با داروهای ضد صرع عود را تجربه نمی کنند.
چه پزشکانی غیر از متخصص مغز و اعصاب و جراح مغز و اعصاب به کودک کمک خواهند کرد؟
پزشکان در حداقل 3 تخصص می توانند به بهبود کیفیت زندگی کمک کنند:
- فیزیوتراپیستدرمان را برای بهبود پیش آگهی توسعه مهارت های حرکتی، یعنی: توانایی نشستن و ایستادن (در موارد شدید) تجویز می کند. کودکانی که علائم خفیف دارند ممکن است از تمریناتی برای تقویت عضلات بازوها و پاهای خود بهره مند شوند.
- خدمات کاردرمانگراگر کودک نتواند کارهایی را انجام دهد که نیاز به مهارت های حرکتی خوب دارد: غذا خوردن، لباس پوشیدن به تنهایی. کاردرمانی زندگی کامل و انجام عملکردها را در خانه، مهدکودک، مدرسه در دسترس قرار می دهد.
- متخصص گفتار درمانیمهارت های صحبت کردن و بلع را بهبود بخشد.
پیش آگهی چیست؟
اسکیزنسفالی پیش آگهی غالباً مطلوبی برای زندگی دارد. در صورت ارائه به موقع اقدامات احیا و / یا توانبخشی و درمان بعدی، بهبودی رخ می دهد. مشکلات مربوط به فعالیت حرکتی مادام العمر ادامه خواهد داشت، خطر عقب ماندگی ذهنی وجود دارد، اما اکثر بیماران می توانند به طور کامل در جامعه زندگی کنند.علاوه بر صرع، هیدروسفالی مشکل اصلی بیماران مبتلا به اسکیزنسفالی است. با افزایش مداوم مایعات از یک طرف، جابجایی بطن ها و فشرده سازی بافت های اطراف، از جمله بصل النخاع (فعالیت قلب و عملکرد تنفسی را تنظیم می کند) وجود دارد. هیدروسفالی متوسط از نظر دارویی درمان میشود، اما همیشه پزشکان نمیتوانند گزینههایی غیر از جراحی بای پس ارائه دهند.
داستان یک بیمار کوچک: پسری 2 ساله.
مادر - 25 ساله، پدر - 29 ساله، اولین بارداری، سلامت رضایت بخش، عدم وجود عوامل مضر محیطی در محل سکونت و محل کار.
هیدروسفالی برای اولین بار توسط سونوگرافی در هفته 34 پیشنهاد شد. از کلینیک منطقه، بیمار به مرکز پری ناتال منطقه ارجاع شد.
اندازه جنین در جنین سنجی با سن حاملگی مطابقت داشت. هنگام بررسی مغز در نیمکره راست، حفره ای با محتویات مایع مشاهده شد. گلومرول های عروقی موجود در آن باعث شد تا مطمئن شویم که علت تشکیل آن کیست نیست. به غیر از دایره باز ویلیس، هیچ تغییر دیگری یافت نشد.
تشخیص بالینی انجام شد: اسکیزنسفالی نوع 2 (با شکاف باز). بعد از 5 هفته یک فرزند پسر به دنیا آمد. وزن: 3450 گرم، 7 امتیاز در مقیاس آپگار. بلافاصله پس از تولد، NSG انجام شد، تشخیص تایید شد. مادر و کودک روز چهارم از بیمارستان مرخص شدند.
2 سال گذشت. کودک در رشد روانی حرکتی (ایستا، مهارت های حرکتی، واکنش های حسی، گفتار، تعامل اجتماعی)، توانایی های حرکتی محدود است. سندرم تشنجی و کاهش رفلکس های نخاعی وجود دارد.
وجود ناهنجاری های جمجمه ای، که به صورت بصری قابل مشاهده است، دارای ارزش پیش آگهی منفی است: میکروسفالی، شکل سر هیدروسفالی. انحرافات مشابهی می تواند در کودک مبتلا به اسکیزنسفالی باز ایجاد شود.
یک پیش آگهی مطلوب برای زندگی به کودک مبتلا به اسکیزنسفالی بسته داده می شود. برعکس، شکاف های باز در ماده خاکستری منجر به تاخیر در رشد ذهنی یا روانی گفتاری (ZPR یا ZPRR)، اختلالات حرکتی می شود.
سابقه یک بیمار بالغ: 20 سال.
رسیدگی به شکایات تورتیکولی (صدا و زنگ در گوش)، تشنج های صرع با اتوماسیون های گفتاری (تلفظ کنترل نشده کلمات)، تشنج های تونیک-کلونیک. حملات صرع منجر به از دست دادن هوشیاری می شود.
از لحظه تولد تا بستری شدن در بیمارستان پس از آخرین تشنج که در کلاس در دانشگاه اتفاق افتاد، تشخیص اسکیزنسفالی فرض نشد.
گزارش مختصردر هنگام تولد، هیچ ناهنجاری مشاهده نشد، تاخیر رشد در 9 ماهگی شروع شد، سمت راست به طور ناگهانی اطاعت نکرد. پس از تماس با یک متخصص مغز و اعصاب اطفال، آنها MRI و سی تی اسکن انجام دادند که تشخیص آن فلج مغزی بود (بعداً مشخص شد که تشخیص نادرست بوده است). یک دوره داروهای وازواکتیو و متابولیک عصبی تجویز شد، اگرچه هیچ نشانه مربوطه وجود نداشت.
اولین تشنج صرع در سن 8 سالگی رخ داد. پس از آن، تشنج با هاله شنوایی و تشنج شدید، اما بدون از دست دادن هوشیاری مشاهده شد. داروهای زیادی از جمله داروهای ضد صرع تجویز شد، اما بیماری پیشرفت کرد.
اخیراً حملات چند روز قبل یا در ابتدای قاعدگی شروع شده است. برای درمان صرع یک دوره دپاکین همراه با لامیکتال تجویز شد. تعداد تشنج ها کاهش پیدا کرد، اما اگر شروع می شد، چندین بار در روز تشنج داشت.
نتایج تشخیص هنگام تماس با بیمارستان بالینی منطقه ای. EEG تغییرات متوسطی را در فعالیت بیوالکتریکی، ریتم آلفای نامنظم، تظاهرات در ناحیه زمانی نیمکره چپ نشان داد. تصویر MRI مشخصه اسکیزنسفالی است.
عیوب ظاهری:استرابیسم واگرا، عدم تقارن ناحیه نازولبیال، کام گوتیک (بالا و باریک، کمانی)، شکل قوس های دندانی شکسته، ایکتیوز (پوست خشک و پوسته پوسته) در ساق پا، دست و پای راست 2 و 2.5 کوتاه شده است. سانتی متر.
مشکلات عصبی:آستیگماتیسم (تاری جزئی خطوط تصویر، تاری دید)، در سمت راست بدن افزایش رفلکس تاندون (گرفتگی عضلات در حین کشش)، پاراپارزی (کاهش فعالیت عضلانی)، کاهش حساسیت وجود دارد. ناپایدار در وضعیت رومبرگ (مستقیم با بازوهای دراز شده). پلی نوروپاتی (کاهش حساسیت در بازوهای زیر آرنج، حساسیت مفرط در پاهای زیر زانو).
پیش آگهی بدبینانه برای کودکان مبتلا به صرع مقاوم به دارو (یعنی با تشنج هایی که با دارو قابل کنترل نیستند) داده می شود. وجود بیماری های همراه کیفیت زندگی را بدتر می کند و فرصت های موجود را کاهش می دهد.
یک پیامد کشنده با عفونت های حاد (از جمله آنهایی که مزمن شده اند)، اختلالات متابولیک، سمیت شدید و نارسایی اندام های متعدد ممکن است.
هتروتوپی زیر اپاندیمی(هتروتوپی اطراف بطنی) شایع ترین شکل هتروتوپی ماده خاکستری (SG) است که با گره های SG که مستقیماً در زیر اپاندیم بطن های جانبی قرار دارند مشخص می شود. بر اساس مورفولوژی می توان به موارد زیر تقسیم کرد:
- کانونی یک طرفه
- کانونی دو طرفه
- منتشر دوطرفه: نوار مواج SW اطراف بطن ها.
همهگیرشناسی
اکثر موارد پراکنده هستند، برخی از آنها مغلوب مرتبط با X هستند (Xq28). زنان دارای اختلال شناختی نسبتاً خفیفی هستند که متعاقباً به صرع مبتلا می شوند. در مورد پسران، سقط خود به خودی معمولاً به دلیل ناهنجاری های سیستم قلبی عروقی رخ می دهد. بازماندگان به شدت ناتوان هستند.
تصویر بالینی
اغلب، هتروتوپی ساب اپاندیمی با صرع و تاخیر رشد همراه است.
آسيب شناسي
مانند انواع دیگر هتروتوپی ها، این نوع نیز نتیجه نقض مهاجرت عصبی است. در برخی موارد، علت ایجاد هتروتوپی ساب اپاندیمی نقض تکثیر سلولی است.
گره های ماده خاکستری از خوشه هایی از نورون ها و سلول های گلیال تشکیل شده اند. جالب است بدانید که آنها اغلب در سمت راست یافت می شوند، احتمالاً به دلیل مهاجرت بعدی نوروبلاست ها از سمت راست.
موارد مرتبط با X نشان دهنده جهش در ژن فیلامین-1 است، پروتئینی که اکتین داخل سلولی را به هم متصل می کند. علاوه بر این، فیلامین 1 نیز نقش مهمی در رشد عروق دارد.
تشخیص
MRI روش انتخابی است، اگرچه هتروتوپی اطراف بطنی در CT و سونوگرافی دیده می شود (اگر اندازه بسیار بزرگ باشد).
سونوگرافی
ندولهای SW ساب اپاندیمی معمولاً در مقایسه با ماده سفید معمولی هیپراکویک هستند و همچنین ممکن است به داخل لومن بطن بیرون بزنند (موجهای بطنی).
سی تی
در CT، هتروتوپی ساب اپاندیمی به عنوان یک ناحیه غیر کلسیفیه از بافت ظاهر می شود که ماده حاجب، از نظر چگالی مشابه با ماده خاکستری طبیعی، در اطراف بطن های جانبی تجمع نمی کند.
ام آر آی
ام آر آی قبل از زایمان
در اواخر بارداری، تشخیص هتروتوپی ساب اپاندیمی نسبتاً واضح است. قبل از هفته 26 بارداری، وجود یک ماتریکس ژرمینال اطراف بطنی تله انسفالیک طبیعی، تشخیص حرکت جنین را دشوار می کند.
ام آر آی پس از زایمان
گره های کوچکی از ماده خاکستری در لایه اپاندیمی مشاهده می شوند و خطوط بطن ها را مخدوش می کنند. اغلب، محلی سازی در ناحیه مثلث و شاخ پس سری است. سایر نواحی مغز طبیعی به نظر می رسند.
گرههای ماده خاکستری در تمام توالیها، از جمله توالیهای پس از کنتراست، که در آنها، مانند ماده خاکستری معمولی، ماده کنتراست را جمع نمیکنند، مشاهده میشوند.
تشخیص های افتراقی
- هنجار
- هسته های دم دار
- تالاموس
- آستروسیتومای سلول غول پیکر ساب اپاندیمال
- تجمع کنتراست مشخصی دارد
- در نزدیکی سوراخ مونرو قرار گرفته است
- گره های ساب اپاندیمی در توبروس اسکلروزیس
- معمولاً کلسیفیه (به جز در اوایل دوران کودکی)
- سیگنال T2 بالاتر از سیگنال ماده خاکستری
- خونریزی زیر اپاندیال در سونوگرافی و ام آر آی قبل از زایمان
- اگرچه تصویر ممکن است مشابه باشد، مطالعه کنترل در مورد خونریزی، تکامل تغییرات را تعیین می کند
این نتیجه اختلال در شکل گیری ساختارهای مغزی فردی یا مغز به عنوان یک کل است که در دوره قبل از تولد رخ می دهد. آنها اغلب علائم بالینی غیراختصاصی دارند: سندرم عمدتاً صرع، عقب ماندگی ذهنی و ذهنی. شدت کلینیک مستقیماً با میزان آسیب مغزی مرتبط است. آنها از طریق سونوگرافی زنان و زایمان، پس از تولد - با استفاده از EEG، نورسونوگرافی و MRI مغز تشخیص داده می شوند. درمان علامتی: ضد صرع، کم آبی، متابولیک، اصلاح کننده روانی.
ICD-10
Q00 Q01 Q02 Q04

اطلاعات کلی
ناهنجاری در رشد مغز - نقایص، شامل تغییرات غیر طبیعی در ساختار تشریحی ساختارهای مغزی. شدت علائم عصبی همراه با ناهنجاری های مغزی به طور قابل توجهی متفاوت است. در موارد شدید، ناهنجاریها علت مرگ جنین قبل از تولد هستند، آنها تا 75 درصد از مرگهای داخل رحمی را تشکیل میدهند. علاوه بر این، ناهنجاری های شدید مغزی باعث حدود 40 درصد مرگ و میر نوزادان می شود. زمان بروز علائم بالینی ممکن است متفاوت باشد. در بیشتر موارد، ناهنجاری های مغزی در ماه های اول پس از تولد کودک ظاهر می شود. اما، از آنجایی که شکل گیری مغز تا سن 8 سالگی طول می کشد، تعدادی از نقایص از نظر بالینی پس از سال اول زندگی ظاهر می شوند. در بیش از نیمی از موارد، ناهنجاری های مغزی با ناهنجاری های اندام های جسمی ترکیب می شود. تشخیص پیش از تولد ناهنجاریهای مغزی یک وظیفه فوری زنان و زایمان عملی است و تشخیص و درمان پس از تولد آنها از موضوعات اولویتدار نورولوژی، نوزادان، اطفال و جراحی مغز و اعصاب مدرن است.

دلایل
مهمترین علت نارسایی رشد داخل رحمی، تأثیر بر بدن زن باردار و جنین، عوامل مضر مختلفی است که اثر تراتوژنیک دارند. بروز ناهنجاری در نتیجه توارث تک ژنی تنها در 1% موارد رخ می دهد. تاثیرگذارترین علت نقص مغزی را یک عامل برون زا می دانند. بسیاری از ترکیبات شیمیایی فعال، آلودگی رادیواکتیو و برخی عوامل بیولوژیکی اثر تراتوژنیک دارند. در اینجا مشکل آلودگی محیط زیست انسان که باعث ورود مواد شیمیایی سمی به بدن زن باردار می شود، اهمیت چندانی ندارد.
اثرات سمی جنینی مختلف ممکن است با سبک زندگی خود زن باردار مرتبط باشد: به عنوان مثال، سیگار کشیدن، اعتیاد به الکل، اعتیاد به مواد مخدر. اختلالات متابولیک در خانم باردار مانند دیابت شیرین، پرکاری تیروئید و غیره نیز می تواند باعث ناهنجاری های مغزی جنین شود. بسیاری از داروهایی که یک زن می تواند در مراحل اولیه بارداری، بدون آگاهی از فرآیندهای در حال وقوع در بدنش، مصرف کند، اثر تراتوژنیک نیز دارد. یک اثر تراتوژنیک قوی توسط عفونت های حامله توسط یک زن باردار یا عفونت های داخل رحمی جنین اعمال می شود. خطرناک ترین آنها سیتومگالی، لیستریوز، سرخجه، توکسوپلاسموز هستند.
پاتوژنز
ساختن سیستم عصبی جنین به معنای واقعی کلمه از هفته اول بارداری شروع می شود. در حال حاضر در روز 23 بارداری، تشکیل لوله عصبی به پایان می رسد، که ادغام ناقص انتهای قدامی آن ناهنجاری های جدی مغزی را به دنبال دارد. تقریباً در روز 28 بارداری ، وزیکول قدامی مغزی تشکیل می شود که متعاقباً به 2 قسمت جانبی تقسیم می شود که اساس نیمکره های مغزی را تشکیل می دهند. علاوه بر این، قشر مغز، پیچش های آن، جسم پینه ای، ساختارهای پایه و غیره تشکیل می شوند.
تمایز نوروبلاست ها (سلول های عصبی زاینده) منجر به تشکیل نورون هایی می شود که ماده خاکستری را تشکیل می دهند و سلول های گلیال که ماده سفید را تشکیل می دهند. ماده خاکستری مسئول فرآیندهای بالاتر فعالیت عصبی است. در ماده سفید، مسیرهای مختلفی وجود دارد که ساختارهای مغزی را به یک مکانیسم عملکردی واحد متصل می کند. نوزادی که در ترم متولد می شود به اندازه یک بزرگسال دارای تعداد نورون است. اما رشد مغز او به ویژه در 3 ماه اول به شدت ادامه دارد. زندگی افزایش سلول های گلیال، انشعاب فرآیندهای عصبی و میلین شدن آنها وجود دارد.
شکست می تواند در مراحل مختلف شکل گیری مغز رخ دهد. اگر در 6 ماه اول رخ دهد. حاملگی می تواند منجر به کاهش تعداد نورون های تشکیل شده، اختلالات مختلف در تمایز و هیپوپلازی قسمت های مختلف مغز شود. در تاریخ بعدی، آسیب و مرگ یک ماده مغزی که به طور معمول تشکیل شده است ممکن است رخ دهد.
انواع ناهنجاری های مغزی
آنسفالی- فقدان مغز و آکرانی (فقدان استخوان جمجمه). محل مغز توسط رشد بافت همبند و حفره های کیستیک اشغال شده است. ممکن است پوشیده از چرم یا برهنه باشد. آسیب شناسی با زندگی ناسازگار است.
انسفالوسل- افتادگی بافت ها و غشاهای مغز از طریق نقص در استخوان های جمجمه به دلیل بسته نشدن آن. به عنوان یک قاعده، در امتداد خط وسط تشکیل می شود، اما همچنین می تواند نامتقارن باشد. یک آنسفالوسل کوچک ممکن است شبیه سفالوهماتوما باشد. در چنین مواردی، اشعه ایکس از جمجمه به تعیین تشخیص کمک می کند. پیش آگهی بستگی به اندازه و محتوای آنسفالوسل دارد. با بیرون زدگی کوچک و وجود بافت عصبی نابجا در حفره آن، برداشتن آنسفالوسل با جراحی موثر است.
میکروسفالی- کاهش حجم و جرم مغز، به دلیل تاخیر در رشد آن. با فراوانی 1 مورد در هر 5 هزار نوزاد رخ می دهد. همراه با کاهش دور سر و نسبت نامتناسب جمجمه صورت / مغز با غلبه جمجمه اول. میکروسفالی حدود 11 درصد از تمام موارد عقب ماندگی ذهنی را تشکیل می دهد. با میکروسفالی شدید، سفاهت ممکن است. اغلب نه تنها ZPR، بلکه تاخیر در رشد فیزیکی نیز وجود دارد.
ماکروسفالی- افزایش حجم مغز و جرم آن. بسیار کمتر از میکروسفالی شایع است. ماکروسفالی معمولا با اختلال در معماری مغز، هتروتوپی ماده سفید کانونی ترکیب می شود. تظاهرات بالینی اصلی عقب ماندگی ذهنی است. ممکن است سندرم تشنجی وجود داشته باشد. ماکروسفالی نسبی با افزایش تنها در یکی از نیمکره ها وجود دارد. به عنوان یک قاعده، با عدم تقارن قسمت مغزی جمجمه همراه است.
دیسپلازی کیستیک مغزی- مشخصه آن حفره های کیستیک متعدد مغز است که معمولاً به سیستم بطنی متصل است. کیست ها می توانند از نظر اندازه متفاوت باشند. گاهی اوقات فقط در یک نیمکره موضعی می شود. کیست های مغزی متعدد با صرع که به درمان ضد تشنج مقاوم است، ظاهر می شوند. کیست های منفرد، بسته به اندازه، ممکن است یک دوره تحت بالینی داشته باشند یا با فشار خون داخل جمجمه همراه باشند. تحلیل تدریجی آنها اغلب ذکر شده است.
هولوپروسسفالی- عدم جدایی نیمکره ها، در نتیجه آنها توسط یک نیمکره منفرد نشان داده می شوند. بطن های جانبی به یک حفره منفرد تبدیل می شوند. همراه با دیسپلازی شدید جمجمه صورت و نقایص جسمی. مرده زایی یا مرگ در روز اول یادداشت می شود.
دیسپلازی کورتیکال کانونی(FKD) - حضور در قشر مغز مناطق پاتولوژیک با نورون های غول پیکر و آستروسیت های غیر طبیعی. محل مورد علاقه - نواحی زمانی و پیشانی مغز. یکی از ویژگی های بارز تشنج های صرع در PKD وجود حمله های کوتاه مدت پیچیده با تعمیم سریع است که در مرحله اولیه آنها با پدیده های حرکتی نمایشی به شکل حرکات، لگدمال کردن در یک مکان و غیره همراه است.
هتروتوپی- تجمع نورون ها، در مرحله مهاجرت نورون ها، در راه خود به سمت قشر به تأخیر افتاده است. هتروتوپیون ها می توانند تک و چندتایی باشند، شکل گره ای و روبانی داشته باشند. تفاوت اصلی آنها با اسکلروز توبروس عدم توانایی در تجمع کنتراست است. این ناهنجاری ها در رشد مغز با اپی سندرم و الیگوفرنی آشکار می شوند که شدت آن به طور مستقیم با تعداد و اندازه هتروتوپیون ها ارتباط دارد. با هتروتوپی انفرادی، تشنج های صرع معمولاً بعد از 10 سالگی ظاهر می شوند.
تشخیص
ناهنجاری های شدید مغزی اغلب با معاینه بصری قابل تشخیص است. در موارد دیگر، ZPR، افت فشار خون عضلانی در دوره نوزادی، وقوع سندرم تشنج در کودکان سال اول زندگی امکان مشکوک شدن به ناهنجاری مغزی را فراهم می کند. در صورتی که هیچ سابقه ای در مورد ترومای تولد نوزاد، هیپوکسی جنین یا خفگی نوزاد وجود نداشته باشد، می توان ماهیت تروماتیک یا هیپوکسیک آسیب مغزی را رد کرد. تشخیص قبل از تولد ناهنجاری های جنینی با غربالگری اولتراسوند در دوران بارداری انجام می شود. سونوگرافی در سه ماهه اول بارداری می تواند از تولد کودکی با ناهنجاری شدید مغزی جلوگیری کند.
یکی از روش های تشخیص نقایص مغزی در نوزادان، نورسونوگرافی از طریق فونتانل است. داده های بسیار دقیق تری در کودکان در هر سنی و در بزرگسالان با استفاده از MRI مغز به دست می آید. MRI به شما امکان می دهد ماهیت و محل ناهنجاری، اندازه کیست ها، هتروتوپی ها و سایر نواحی غیر طبیعی را تعیین کنید تا تشخیص افتراقی را با ضایعات مغزی هیپوکسیک، تروماتیک، تومور، عفونی انجام دهید. تشخیص سندرم تشنج و انتخاب درمان ضد تشنج با استفاده از EEG و همچنین نظارت تصویری EEG طولانی مدت انجام می شود. در صورت وجود موارد خانوادگی ناهنجاری های مغزی، ممکن است مشورت با یک متخصص ژنتیک با تحقیقات تبارشناسی و تجزیه و تحلیل DNA مفید باشد. به منظور شناسایی ناهنجاری های ترکیبی، معاینه اندام های جسمی انجام می شود: سونوگرافی قلب، سونوگرافی حفره شکمی، رادیوگرافی اندام های قفسه سینه، سونوگرافی کلیه ها و غیره.
درمان ناهنجاری های مغزی
درمان ناهنجاری های مغزی عمدتاً علامتی است و توسط متخصص مغز و اعصاب اطفال، متخصص نوزادان، متخصص اطفال، متخصص صرع انجام می شود. در صورت وجود سندرم تشنجی، درمان ضد تشنج (کاربامازپین، لوتیراستام، والپروات، نیترازپام، لاموتریژین و غیره) انجام می شود. از آنجایی که صرع در کودکان همراه با ناهنجاری های رشد مغز معمولاً به تک درمانی ضد تشنج مقاوم است، ترکیبی از 2 دارو تجویز می شود (مثلاً لوتیراستام با لاموتریژین). با هیدروسفالی، درمان کم آبی انجام می شود، طبق نشانه ها، به جراحی بای پس متوسل می شود. به منظور بهبود متابولیسم بافتهای مغزی با عملکرد طبیعی، که تا حدودی نقص مادرزادی موجود را جبران میکند، میتوان یک دوره درمان نورومتابولیک را با تجویز گلیسین، ویتامینهای گرم انجام داد. ب و غیره داروهای نوتروپیک فقط در صورت عدم وجود اپی سندرم در درمان استفاده می شوند.
با ناهنجاریهای مغزی متوسط و نسبتاً خفیف، توصیه میشود یک حمایت روانشناختی جامع از کودک، آموزش کودکان بزرگتر در مدارس تخصصی انجام شود. این روش ها به القای مهارت های سلف سرویس، کاهش شدت الیگوفرنی و در صورت امکان سازگاری اجتماعی کودکان مبتلا به ناهنجاری های مغزی کمک می کند.
پیش بینی و پیشگیری
پیش آگهی تا حد زیادی با شدت ناهنجاری مغزی تعیین می شود. یک علامت نامطلوب، شروع زودتر صرع و مقاومت آن در برابر درمان مداوم است. وجود آسیب شناسی جسمی مادرزادی همزمان پیش آگهی را پیچیده می کند. یک اقدام پیشگیرانه موثر، حذف اثرات جنینی و تراتوژنیک بر روی یک زن در دوران بارداری است. هنگام برنامه ریزی برای بارداری، والدین آینده باید عادت های بد را کنار بگذارند، تحت مشاوره ژنتیک قرار بگیرند و از نظر عفونت های مزمن معاینه شوند.

بخش های مورفولوژیکی اصلی مغز
- مغز جلویی (نهایی) از دو نیمکره مغزی تشکیل شده است.
- دی انسفالون شامل تالاموس، اپیتالاموس، هیپوتالاموس، غده هیپوفیز است که در دیانسفالون گنجانده نشده است، اما به یک غده جداگانه جدا شده است.
- مغز میانی از پاهای مغز و سقف کوادریژمینا تشکیل شده است. تپه های بالایی سقف کوادریژمینا مرکز بینایی زیر قشری و تپه های پایینی مرکز زیر قشری شنوایی هستند.
- مغز عقبی از پل و مخچه تشکیل شده است.
- مدولا محل اتصال بصل النخاع به طناب نخاعی، فورامن مگنوم است.
مغز میانی، مغز عقبی و بصل النخاع در یک ساقه مغز ترکیب می شوند.

ساختار داخلی نیمکره های مغزی.
- ماده خاکستری
- ماده سفید
ماده خاکستری از قشر مغز تشکیل شده است که نیمکره های مغز را به طور کامل می پوشاند. ماده سفید در زیر ماده خاکستری مغز قرار دارد. با این حال، مناطقی با ماده خاکستری نیز در ماده سفید وجود دارد - خوشه هایی از سلول های عصبی. به آنها هسته (هسته) می گویند. به طور معمول، مرز مشخصی بین ماده سفید و خاکستری وجود دارد. تمایز ماده سفید و خاکستری در CT امکان پذیر است، اما در MRI تمایز بهتری دارد.

دیسپلازی قشر مغز
در دیسپلازی قشر مغز، مرزهای بین ماده سفید و خاکستری تار می شود. در چنین حالتی، باید از وارونگی بازیابی توالی T1 نیز استفاده شود. در این تصاویر، مرزها به جز نواحی دیسپلازی قشری قابل مشاهده خواهند بود.

حمله قلبی
با ادم سیتوتوکسیک که در اولین دقایق انفارکتوس مغزی ایجاد می شود، تمایز بین ماده سفید و خاکستری نیز از بین می رود که نشانه اولیه CT انفارکتوس مغزی است.







نیمکره های بزرگ مغز
نیمکره های مغز توسط یک فرآیند بزرگ فالسیفرم از هم جدا می شوند. در هر نیمکره 4 لوب وجود دارد:
- لب قدامی مغز.
- لوب جداری
- لوب پس سری
لوب فرونتال با استفاده از یک شیار مرکزی یا رالند از جداری جدا می شود که در بخش های محوری و ساژیتال کاملاً قابل مشاهده است.
لوب فرونتال توسط یک شیار جانبی از لوب تمپورال جدا می شود که هم در قسمت های ساژیتال و محوری و هم در قسمت های فرونتال به خوبی قابل مشاهده است.
لوب جداری با شیار جداری-پس سری به همین نام از لوب اکسیپیتال جدا می شود. این خط هنوز حوضچه های کاروتید و بازیلار را از هم جدا می کند.
برخی از نویسندگان جزیره ای را در یک شیار جداگانه اختصاص می دهند که ناحیه بزرگی از قشر است که جزیره را از بالا می پوشاند و از جانبی آن را تشکیل می دهد (لاتین pars opercularis) و از بخشی از لوب های پیشانی، گیجگاهی و جداری مجاور تشکیل می شود. .
مرزها را به اشتراک بگذارید


مرزها را به اشتراک بگذارید
مرزهای لوب فرونتال و جداری.
امگا -?
شیار مرکزی
علامت سبیل- شکنج پست مرکزی
شکنج سینگوله – شکنج پست مرکزی
برای تعیین صحیح مرز لوب فرونتال و جداری ابتدا شیار مرکزی را پیدا می کنیم. علامت در این شیار حک شده است امگا -? در مقاطع محوری
علامت سبیل عمود بر خط وسط و تصویری که مربوط به شیار پست مرکزی است نیز کمک می کند. شیار مرکزی به ترتیب در جلوی شکنج پست مرکزی قرار دارد.
شیار کمربند.
در بخش های ساژیتال، باید جسم پینه ای را در بالای آن پیدا کنید، یک شیار سینگوله وجود دارد که از عقب و به سمت بالا به سمت شیار پست مرکزی ادامه می یابد، که از آن شیار مرکزی یا رولاند در جلو قرار دارد.

لب قدامی مغز
لوب پیشانی بزرگ است و یکی از شکنج های اصلی شکنج پیش مرکزی است که مرکز حرکت قشر مغز است. در لوب فرونتال، شکنج فوقانی، میانی و تحتانی نیز مشخص می شود. پیچیدگی های ذکر شده از بالا به پایین و به موازات یکدیگر می روند.
در سطح تحتانی لوب فرونتال شکنج مستقیم و مداری قرار دارد که بین آنها مجاری بویایی و پیازها قرار دارند. این نواحی در اثر ضربه آسیب دیده اند.

آسیب تروماتیک به لوب فرونتال
در این بیمار، آسیب متقارن به بخشهای پایه هر دو لوب فرونتال را مشاهده میکنیم که مربوط به تغییرات پس از ضربه است.

منطقه بروکا
همچنین یک منطقه مهم ناحیه بروکا است که در قسمت های انتهایی شکنج فرونتال تحتانی قرار دارد. محلی سازی آن هنگام برنامه ریزی مداخلات جراحی مغز و اعصاب مهم است. پیدا کردن این منطقه آسان است، با یادآوری نماد مک دونالد.

انفارکتوس با درگیری در فرآیند پاتولوژیک ناحیه بروکا
این بیمار به دلیل انسداد شاخه M2 قدامی MCA چپ دچار انفارکتوس حاد شده است. آسیب به لوب فرونتال با درگیری در روند پاتولوژیک ناحیه بروکا.

لوب جداری
در پشت شیار مرکزی شکنج پست مرکزی قرار دارد که به عنوان یک تحلیلگر قشر مغزی حساسیت عمومی و حس عمقی عمل می کند.
در پشت لوبول های جداری فوقانی و تحتانی قرار دارند.
در لوبول جداری فوقانی، هسته آنالایزر پوست مسئول استریوگنوزیا است - توانایی تشخیص اشیا با لمس.
در لوبول پاریتال پایین یک تحلیلگر حرکتی مسئول آپراکسی وجود دارد - حرکات هدفمند و ارادی.
stereognosia- توانایی تشخیص اشیا با لمس.
آپراکسی- نقض اقدامات خودسرانه

آتروفی پرکونئوس
آتروفی پراکونئوس یکی از علائم اولیه بیماری آلزایمر حتی قبل از آتروفی قشر لوب های تمپورال و هیپوکامپ است.
پراکونئوس بخشی از لوب جداری در سطح داخلی هر دو نیمکره مغز است که در بالا و جلوی جسم پینه ای قرار دارد.

لوب تمپورال
در لوب تمپورال ترشح می کند
شکنج تمپورال برتر
شکنج گیجگاهی میانی
شکنج گیجگاهی تحتانی. این سه پیچ به موازات یکدیگر هستند و در یک صفحه افقی قرار دارند.
پیچش های Geschl روی سطح شکنج زمانی فوقانی قرار دارند. آنها مرکز قشری شنوایی هستند.
شکنج پاراهیپوکامپ در سطح تحتانی لوب های تمپورال در نواحی داخلی قرار دارد. قلاب به همراه هیپوکامپ مسئول حس بویایی هستند. هنگامی که هیپوکامپ آسیب می بیند، در وهله اول حافظه دچار اختلال می شود.
منطقه ورنیکه ناحیه ورنیکه در قسمت های انتهایی شکنج گیجگاهی فوقانی قرار دارد. این یک منطقه گفتار حسی است.

لوب پس سری
در لوب های پس سری، شیارها و پیچ های نامنظم مشخص می شوند، اما ثابت ترین آنها شیار خار واقع در سطح داخلی لوب پس سری است. در اطراف شیار خار 17، 18 و 19 میدان برادمن وجود دارد که مرکز بینایی قشری است.

انسداد PCA
این بیمار از نظر بالینی اختلال بینایی به دلیل آسیب به لوب اکسیپیتال را مشاهده کرده است که علت آن حمله قلبی (انسداد PCA) بوده است.
ماده خاکستری زیر قشری







ماده خاکستری زیر قشری
ماده خاکستری زیر قشری شامل:
- تالاموس
- هسته های پایه
- هسته دمی
- هسته عدسی، که در آن پوسته و توپ رنگ پریده جدا شده است.
- پوسته
کپسول داخلی از قسمت قدامی ران، زانو و خلفی ران تشکیل شده است.
چگونه ران عقبی را پیدا کنیم؟
بین تالاموس و هسته عدسی ما یک کانون فوق شدید پیدا می کنیم که یک دستگاه هرمی است. از این فوکوس شدید، خطی به سمت زانو می کشیم که برآمدگی استخوان ران خلفی کپسول داخلی خواهد بود.
نکته - زانوی پشتی را با توپ رنگ پریده اشتباه نگیرید.
هنگام طبقه بندی خونریزی های داخل مغزی در ماده خاکستری زیر قشری، بسته به محل قرارگیری در رابطه با کپسول داخلی، خونریزی ها به موارد زیر تقسیم می شوند:
- جانبی
- داخلی
- مختلط
ماده سفید
الیاف کمسیورال که نیمکره ها را به هم متصل می کنند.
جسم پینه ای (بزرگترین کامیسور)
کمیسور قدامی
کمسیور خلفی (کمیسیور فورنیکس)

کمیسور قدامی
کمیسور قدامی در زیر منقار جسم پینه ای در پشت صفحه انتهایی قرار دارد و برخی از قسمت های مغز بویایی را به هم متصل می کند: شکنج هیپوکامپ، قلاب های چپ و راست لوب های تمپورال.
کمسیور خلفی
کمیسور خلفی متعلق به اپیتالاموس است، در ریشه اپی فیز قرار دارد و قسمت های مربوطه مغز میانی و دیانسفالون را به هم متصل می کند.
ارزش عملی:
خط bicommissural در صفحه ساژیتال برای ارزیابی جسم پینه ای استفاده می شود. خط bicommissural از طریق لبه بالایی کامیسور قدامی و لبه پایینی کمیسور خلفی کشیده می شود.

جسم پینه ای
جسم پینه ای شامل موارد زیر است:
تنه یا بدن (قدامی و خلفی)
هر بخش بخش هم جانبی مغز را به هم متصل می کند.
تشکیل جسم پینه ای.
جسم پینه ای به ترتیب خاصی رشد می کند:
از زانو، سپس بدن، غلتک و در انتها منقار رشد می کند.
میلیناسیون جسم پینه ای از قسمت های خلفی به قدامی انجام می شود.
این دانش به محدود کردن تشخیص افتراقی در پاتولوژی های جسم پینه کمک می کند.

دیسژنز و آتروفی جسم پینه ای
با دیسژنیز جسم پینه ای، زانو و قسمت های قدامی جسم پینه ای به خوبی شکل می گیرند، اما برجستگی و منقار وجود ندارد. این آسیب شناسی مادرزادی است. آسیب شناسی در سمت چپ نشان داده شده است.
با آتروفی جسم پینه ای، بخش های خلفی جسم پینه ای (بخش خلفی بدن و غلتک) به خوبی شکل می گیرند، اما اندازه منقار، زانو و قسمت قدامی بدن کاهش می یابد. این تغییرات اکتسابی است.
بسیاری از بیماری ها بر جسم پینه ای تأثیر می گذارند، بنابراین وجود ضایعات برای یک بیماری خاص پاتوژنومیک نیست.

بیماری مارکیافوا-بیگنامی
بیماری مارچیافوا-بیگنامی (دژنراسیون مرکزی جسم پینه ای، سندرم مارکیافاوا، میلینولیز اکستراپونتین).
در افرادی که از الکل سوء استفاده می کنند رخ می دهد. در این افراد، MRI ضایعه برآمدگی و قسمت های خلفی تنه (بدن) جسم پینه ای را نشان می دهد.
در مراحل مزمن بیماری Marchiafava-Bignami، جسم پینه ای به شکل یک ساندویچ تجسم می شود که در آن لایه های بالایی و پایینی جسم پینه ای حفظ می شود، اما با نکروز لایه های میانی.
ماده سفید
ماده سفید:
- دور بطنی
- مقاطع عمیق (مراکز نیمهووال)
- الیاف U
ماده سفید اطراف بطن در مجاورت بطن های جانبی مغز قرار دارد.
فیبرهای U قشر شکنجی مجاور یا ماده سفید زیر قشری را به هم متصل می کنند.
بخش های عمیق ماده سفید بین ماده سفید اطراف بطنی و زیر قشری قرار دارند.
ضایعات در ماده سفید:
ضایعات ماده سفید بر اساس محل طبقه بندی می شوند:
- دور بطنی
- کنار قشر
- زیر قشری
- ضایعات در ماده سفید عمیق

ضایعات دور بطنی
دور بطنی (تک یا چندتایی، کوچک یا بزرگ، ادغام با یکدیگر)

ضایعات Juxtacortical
کنار هم - تقریبا این کانون ها در فیبرهای u موضعی هستند و مستقیماً در مجاورت ماده خاکستری قرار دارند، یعنی لایه ای از ماده سفید بین ضایعه و ماده خاکستری وجود ندارد.
از نظر شکل، این کانون ها متفاوت هستند، چگونه می توان شکل فیبرهای یو را تکرار کرد، همچنین می توانند شکل گرد و نامنظم باشند. این محلی سازی برای ام اس پاتوژنومیک است.

ضایعات زیر قشری
کانون های ساب کورتیکال کانون هایی هستند که در نزدیکی قشر مغز قرار دارند، اما در عین حال لایه ای از ماده سفید بین کانون و قشر وجود دارد.

کانون ها در ماده سفید عمیق
این کانون ها در بیماری های مختلف مغز یافت می شوند.




بطن های مغز
بطن های جانبی از موارد زیر تشکیل شده اند:
- شاخ های قدامی ( پیشانی )
- شاخ های خلفی (اکسیپیتال).
- شاخ های پایینی (زمانی).
بطن های جانبی توسط سوراخ جفتی مونرو به بطن سوم متصل می شوند.
بطن سوم به دلیل وجود پاکت ها شکلی نامنظم دارد. دهانه بطن سوم مربوط به کمیسور بین تالاموسی است.
بطن سوم توسط یک قنات سیلوین به بطن چهارم متصل می شود. از بطن چهارم، CSF از طریق سوراخ جفتی Luschka و دیافراگم جفت نشده Mogendi وارد مخازن پایه می شود.
هنگام ارزیابی بطن ها، ارزش توجه به شاخ های بطنی را دارد، زیرا در بیماری های دژنراتیو مانند بیماری آلزایمر، آتروفی هیپوکامپ با گسترش شاخ های تمپورال همراه است. در حالت FLAIR، سیگنال از شاخ های خلفی (پس سری) افزایش می یابد که طبیعی است و همچنین عدم تقارن شاخ ها.
بطن سوم.
بطن سوم در خط وسط بین توبرکل های بینایی قرار دارد. از طریق دهانه های مونرو به بطن های جانبی و از طریق قنات مغز به بطن چهارم متصل می شود.
پاکت های بطن سوم:
- فوق کیاسماتیک
- ناامید کننده
- سوپراپینال
- پینه آل
به طور معمول این جیب ها دارای گوشه های تیز هستند اما با افزایش فشار، جیب ها باز می شوند.
بطن چهارم مغز.
بطن چهارم حفره مغز عقب است و با کمک سوراخ های جفتی لوشکا و سوراخ جفت نشده مگندی به مخازن پایه متصل می شود.

شبکه های عروقی
شبکه مشیمیه تولید کننده CSF در تمام بطن های مغز قرار دارد، بنابراین کلسیفیکاسیون شبکه مشیمیه، که بیشتر در شاخ های خلفی بطن های جانبی مشاهده می شود، در هر دو بطن سوم و چهارم قابل مشاهده است.

توبروس اسکلروزیس
کلسیفیکاسیون شبکه های مشیمیه، که هنجار است، نباید با شرایط پاتولوژیک اشتباه شود. به عنوان مثال، با کلسیفیکاسیون بطن های جانبی - غده های اطراف بطنی در اسکلروز توبروس.

ماده خاکستری هتروتوپیک
مهم است که به یاد داشته باشید که تنها ماده خاکستری که با بطن های جانبی هم مرز است، هسته های دمی هستند که دارای خطوط صاف و یکدست هستند. ساختارهای ماده خاکستری اضافی که کانتور بطن های جانبی را تغییر می دهند، تغییرات پاتولوژیک مشخصه هتروتوپی ماده خاکستری هستند.

انواع ساختار بطن ها
- حفره سپتوم شفاف که در اکثر نوزادان مشاهده می شود (به مرور زمان بسته می شود) و مانند یک شکل مثلثی بین بدنه های بطن جانبی قدامی به نظر می رسد. این حفره هرگز از سوراخ مونرو عبور نمی کند.
- حفره بادبان میانی یکی از دیواره های حفره که سقف بطن سوم را تشکیل می دهد.
- حفره Verge یک حفره گسترده بین بدنه های بطن های جانبی است.

کیست کلوئیدی
انواع ساختاری باید از کیست کلوئیدی متمایز شود، که تقریباً در تمام توالیهای پالس با شدت سیگنال مایع مغزی نخاعی متفاوت است. پس از معرفی یک ماده حاجب، کیست های کلوئیدی کنتراست را جمع نمی کنند، که مربوط به یک فرآیند خوش خیم است.

هنجار MRI - بخش ساژیتال میانه. CSF - مخازن.
الف - مخزن صفحه انتهایی
ب - CASTERN OF CHIASMA
ج - مخزن بین ساقه ای
د - مخزن بای پس
ه - مخزن چهار ضلعی
و - مخزن سیسترنو مخچه
ز - مخزن سیسترنو مخچه Prepontine pontocerebellaris
H - کاسترنای جانبی مغزی
I - TANK MAGNA
تصویر از دکتر Coenraad J. Hattingh
قوطی های مغز
از بطن چهارم مغز، مایع مغزی نخاعی با کمک سوراخ های جفتی لوشکا و سوراخ جفت نشده مگندی وارد مخازن پایه می شود.
نام مخازن بر اساس محلی سازی:
در صفحه ساژیتال:
- مخزن سوپراسلار
- مخزن پل که شریان اصلی از آن عبور می کند.
- آب انبار چهار تپه
- مخزن بزرگ یا پایه مغز
در صفحه محوری:
- مخزن بین ساقه ای
- مخزن بای پس مخزن بین ساقه ای و چهار قلویی را به هم متصل می کند. همچنین، بال ها از مخزن بای پس متمایز می شوند: راست و چپ.


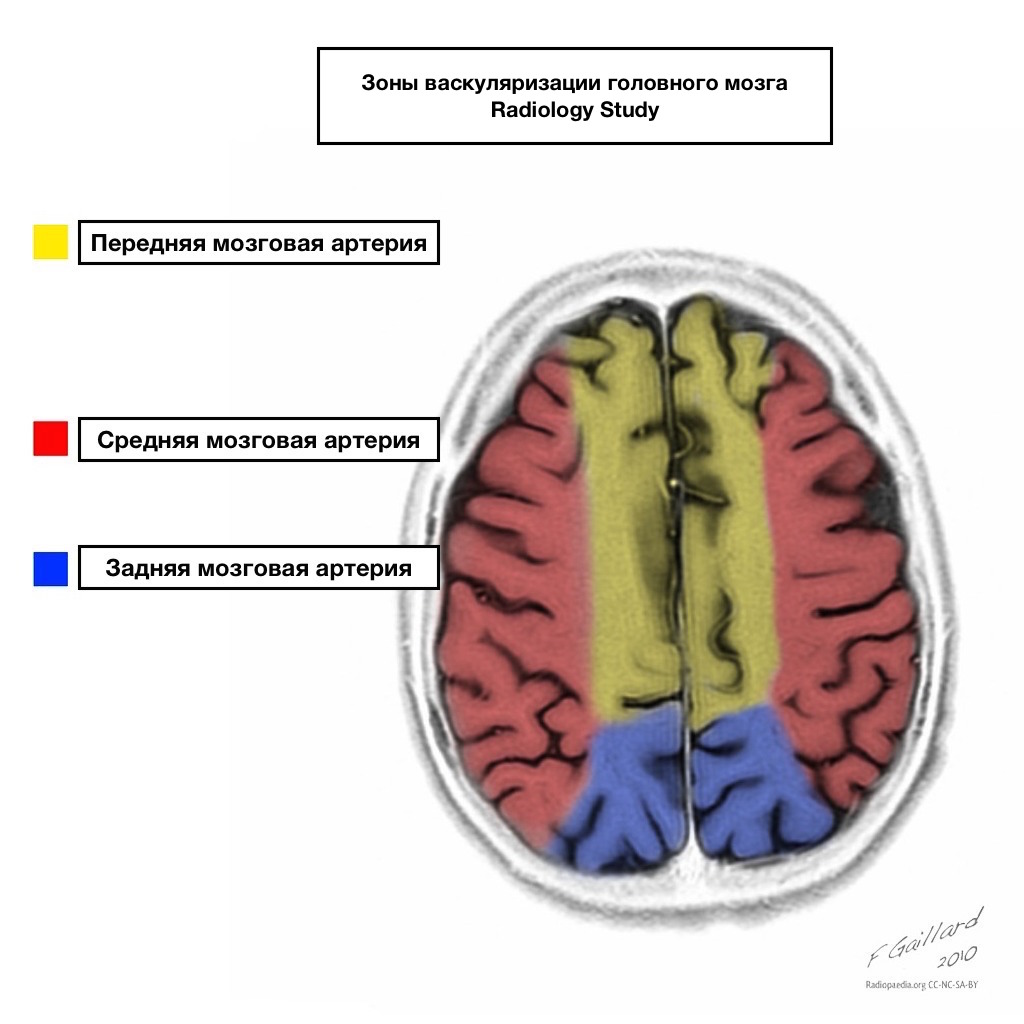







حوضچه های تامین خون مرزهای مشخصی دارند.

نواحی خون رسانی مجاور
مناطق خونرسانی مجاور در تقاطع مناطق خونرسانی:
شریان مغزی قدامی
شریان مغزی میانی
شریان مغزی خلفی.
اغلب، انفارکتوس در این مناطق ماهیت همودینامیک دارد، یعنی زمانی که فشار خون کاهش می یابد رخ می دهد.

پوسته های مغز
مغز با سه غشا پوشیده شده است.
- پوسته نرم به طور محکم به مغز متصل است، به تمام شکاف ها و شیارها می رود و رگ های خونی در آن قرار دارند. در نقاط خاصی به بطن های مغز نفوذ کرده و شبکه مشیمیه را تشکیل می دهد.
- غشای عنکبوتیه یا عنکبوتیه روی شیارها قرار دارد و از یک شکنج به شکنج دیگر گسترش می یابد.
- پوسته سخت از داخل حفرههای جمجمه را خط میکشد، محکم به آنها میچسبد و سینوسهای وریدی و فرآیندهایی را تشکیل میدهد که ساختارهای جداگانه مغز را از یکدیگر جدا میکند.
به طور معمول، غشای مغز در ام آر آی قابل مشاهده نیست، اما پس از معرفی ماده حاجب، ماده ی سخت شامه کنتراست می شود.

تغییرات در مننژهای نرم.
در کارسینوماتوز لپتومننژیال، در تصاویر بدون کنتراست T1 و T2، سیگنال مننژها افزایش یافته و پس از معرفی کنتراست، دید را بهبود می بخشد.

مننژیت
تغییرات در مننژها نیز اغلب در تغییرات التهابی، به عنوان مثال، در لپتومننژیت سلی مشاهده می شود.

تغییر دورا
با هیپوتانسیون داخل جمجمه ای تغییر در سخت شامه رخ می دهد. با این آسیب شناسی، ماده سخت غلیظ دیده می شود و کنتراست را به شدت انباشته می کند. معیارهای اضافی در تشخیص افزایش اندازه غده هیپوفیز، افتادگی لوزه های مخچه به سوراخ سوراخ است.

تغییرات در سخت شامه نیز در کارسینوماتوز پاکیمننژیال رخ می دهد که با ضخیم شدن سخت شامه همراه با تجمع شدید ماده حاجب و ادم وازوژنیک قسمت های مجاور لوب فرونتال ظاهر می شود.

فضاهای پوسته
فضاهای پوسته فضاهای بین پوسته های مغز هستند.
- فضای زیر عنکبوتیه فضای بین پیا ماتر و عنکبوتیه است. به طور معمول، باید شدت مایع مغزی نخاعی را داشته باشد.
- فضای ساب دورال فضای بین عنکبوتیه و سخت شامه است.
- فضای اپیدورال فضای بین دورا و استخوانهای جمجمه است که معمولاً با جوش خوردن سختشکم به استخوانهای جمجمه قابل مشاهده نیست.

تغییر در فضای زیر عنکبوتیه
تغییر در فضای زیر عنکبوتیه
باریک شدن. این تغییرات در طول قرار گرفتن در معرض حجمی (تومور، انفارکتوس) رخ می دهد.
افزونه. این تغییرات در دوره پس از سانحه، پس از حمله قلبی یا در طول آتروفی رخ می دهد.



خونریزی های پوسته ای
با خونریزی های پوسته، ما می توانیم پوسته ها را کاملاً شناسایی کنیم.
انواع خونریزی پوسته ای:
خونریزی اپیدورال معمولاً به صورت عدسی دیده می شود و از بخیه ها خارج نمی شود، اما ممکن است از سینوس های مغز عبور کند که با خونریزی های ساب دورال که هرگز از سینوس های مغز عبور نمی کنند متفاوت است.
خونریزی ساب دورال. شایع ترین علت پارگی وریدهای سطحی در نتیجه جابجایی مغز در هنگام ضربه است. اگر در این حالت غشای ساب عنکبوتیه نیز پاره شود، در این صورت مایع مغزی نخاعی وارد فضای ساب دورال می شود.
خونریزی زیر عنکبوتیه. افزایش سیگنال از مایع مغزی نخاعی در حالت FLAIR تشخیص داده می شود. شایع ترین علت خونریزی زیر عنکبوتیه، پارگی آنوریسم است، زیرا شریان های تغذیه کننده مغز در فضای زیر عنکبوتیه قرار دارند.

در فرآیندهای پاتولوژیک در پوسته ها از واژه لوب استفاده نمی شود، بلکه از عبارت ناحیه استفاده می شود. به عنوان مثال، این بیمار مننژیوم فرونتال دارد.

