प्रणालीगत अमाइलॉइडोसिस: निदान, विभेदक निदान, उपचार। नैदानिक पाठ्यक्रम और इसकी मुख्य अभिव्यक्तियाँ
अमाइलॉइडोसिस- एक चयापचय विकार की विशेषता वाली बीमारी, जिसके परिणामस्वरूप शरीर के लिए एक नया पदार्थ (एमाइलॉयड) बनता है, जो अंगों में जमा होता है और उनके कार्यों को बाधित करता है।
अमाइलॉइड एक जटिल ग्लाइकोप्रोटीन है जिसमें फाइब्रिलर और गोलाकार प्रोटीन पॉलीसेकेराइड के साथ निकटता से जुड़े होते हैं। अमाइलॉइड फाइब्रिल पॉलीपेप्टाइड प्रोटीन से बना होता है; फाइब्रिलर प्रोटीन के अलावा, अमाइलॉइड में एक और प्रोटीन भी होता है - तथाकथित पी-घटक, जो एमिलॉइड के सभी रूपों के लिए समान है। माना जाता है कि पी घटक अमाइलॉइड फाइब्रिल से जुड़ा एक सामान्य सीरम प्रोटीन है।
अमाइलॉइडोसिस किसी भी बीमारी की जटिलता के रूप में हो सकता है या एक स्वतंत्र प्रक्रिया के रूप में विकसित हो सकता है।
वर्तमान में, एटियलजि के आधार पर, अमाइलॉइडोसिस के कई रूप हैं जिनकी अमाइलॉइड फाइब्रिल की अपनी जैव रासायनिक संरचना है।
प्राथमिक (अज्ञातहेतुक) अमाइलॉइडोसिस बिना किसी स्पष्ट कारण के विकसित होता है और विभिन्न अंगों (हृदय, गुर्दे, आंतों, यकृत, तंत्रिका तंत्र) को प्रभावित करता है। प्राथमिक अमाइलॉइडोसिस का जैव रासायनिक रूप एएल-फॉर्म है, ऐसे अमाइलॉइड का अग्रदूत आईजी और इम्युनोग्लोबुलिन प्रकाश श्रृंखलाएं हैं। अमाइलॉइड की संरचना और आंतरिक अंगों को नुकसान की प्रकृति के अनुसार, मल्टीपल मायलोमा में अमाइलॉइडोसिस प्राथमिक (अज्ञातहेतुक) अमाइलॉइड खुराक के करीब है, जिसे वर्तमान में एक अलग समूह में विभाजित किया गया है।
वंशानुगत (आनुवंशिक) अमाइलॉइडोसिस गुर्दे के एक प्रमुख घाव, गुर्दे और तंत्रिका तंत्र को नुकसान के संयोजन से प्रकट होता है। हमारे देश में, वंशानुगत अमाइलॉइडोसिस आमतौर पर एक आवधिक बीमारी से जुड़ा होता है जो एक ऑटोसोमल प्रमुख तरीके से फैलता है। इस बीमारी में, अमाइलॉइडोसिस ही एकमात्र अभिव्यक्ति हो सकती है। वंशानुगत अमाइलॉइडोसिस का जैव रासायनिक रूप AF है (अमाइलॉइड अग्रदूत प्रीलब्यूमिन है)। आवधिक बीमारी के मामले में, जैव रासायनिक रूप एए है (पूर्ववर्ती एसएए प्रोटीन है)।
अधिग्रहित (माध्यमिक) अमाइलॉइडोसिस सबसे अधिक बार होता है और रुमेटीइड गठिया, बेचटेरू रोग, तपेदिक, पुरानी दमन में विकसित होता है - ऑस्टियोमाइलाइटिस, ब्रोन्किइक्टेसिस, क्रोनिक फेफड़े का फोड़ा, कम अक्सर अल्सरेटिव कोलाइटिस, सोरायसिस, लिम्फोग्रानुलोमैटोसिस, सिफलिस, गुर्दे के ट्यूमर, फेफड़े और अन्य में। माध्यमिक अमाइलॉइडोसिस का जैव रासायनिक रूप एए है (इसका सीरम अग्रदूत हेपेटोसाइट्स द्वारा संश्लेषित एसएए प्रोटीन है)।
सेनील अमाइलॉइडोसिस मस्तिष्क, अग्न्याशय और हृदय में पाए जाने वाले प्रोटीन चयापचय के अनैच्छिक विकारों का परिणाम है। जैव रासायनिक सूत्र AS है (पूर्ववर्ती prealbumin है)।
स्थानीय अमाइलॉइडोसिस बिना किसी स्पष्ट कारण के विकसित होता है, इसका जैव रासायनिक सूत्र AE है (अग्रदूत अज्ञात है)।
रोगजनन।केवल रोगजनन के अलग-अलग लिंक सर्वविदित हैं (योजना 22)। यह इस योजना से है कि जीन उत्परिवर्तन के प्रभाव में, साथ ही बाहरी कारकों के प्रभाव में, प्रतिरक्षा में परिवर्तन होता है - यह घट जाता है
टी-लिम्फोसाइटों की संख्या। इससे लिम्फोसाइटों के बी-सिस्टम पर उनके नियंत्रण प्रभाव में कमी आती है। नतीजतन, सामान्य इम्युनोग्लोबुलिन ले जाने वाली बी कोशिकाओं की संख्या कम हो जाती है और एमाइलॉयड फाइब्रिल अग्रदूतों को संश्लेषित करने वाली बी कोशिकाओं की संख्या बढ़ जाती है। अमाइलॉइडोब्लास्ट अधिक मात्रा में फाइब्रिलर प्रोटीन का उत्पादन करते हैं, जो बड़ी मात्रा में अमाइलॉइड के संश्लेषण का कारण बनता है।
हालांकि, अमाइलॉइडोक्लास्ट्स के आनुवंशिक दोष के कारण, जो उनकी एंजाइमिक गतिविधि में कमी में योगदान देता है, पर्याप्त अमाइलॉइड पुनर्जीवन नहीं होता है। नतीजतन, ऊतकों और अंगों में अमाइलॉइड का बढ़ा हुआ जमाव होता है [मुखिन एन.ए., 1981]।
मल्टीपल मायलोमा में, प्लाज्मा कोशिकाओं द्वारा पैराप्रोटीन के बढ़े हुए उत्पादन के परिणामस्वरूप अमाइलॉइडोसिस विकसित होता है, जिसका उपयोग अमाइलॉइड बनाने के लिए किया जाता है। अमाइलॉइडोसिस के विभिन्न रूपों में अमाइलॉइड की संरचना भिन्न होती है, जो अमाइलॉइड तंतुओं के प्रोटीन की संरचना से निर्धारित होती है।
मायोकार्डियम, परिधीय नसों (मुख्य रूप से अमाइलॉइडोसिस के अज्ञातहेतुक रूप में मनाया जाता है) को नुकसान के साथ, अमाइलॉइड संयोजी ऊतक के कोलेजन फाइबर के आसपास जमा होता है। घावों में जालीदार तंतुओं के आसपास अमाइलॉइड का जमाव देखा जाता है
गुर्दे, आंत, यकृत, अधिवृक्क ग्रंथियां, अग्न्याशय (वंशानुगत और माध्यमिक अमाइलॉइडोसिस के साथ)। हालांकि, पेरिकोलेजेनस और पेरिरेटिकुलर अमाइलॉइड जमा का संयोजन संभव है, जो विभिन्न अंगों और प्रणालियों के संयुक्त घाव प्रदान करता है।
ऊतकों में अमाइलॉइड के जमाव के साथ, काम करने वाले तत्वों, कार्डियोमायोसाइट्स, हेपेटोसाइट्स, तंत्रिका तंतुओं और वृक्क ग्लोमेरुली की संख्या कम हो जाती है, जो बाद में अंग विफलता के विकास की ओर ले जाती है।
तो, हृदय में, अमाइलॉइड एंडोकार्डियम के नीचे, मायोकार्डियम के स्ट्रोमा और वाहिकाओं में और एपिकार्डियम में नसों के साथ जमा होता है। इसी समय, हृदय आकार में तेजी से बढ़ता है, और कार्डियोमायोसाइट्स की संख्या तेजी से घटती है। यह सब मायोकार्डियम और दिल की विफलता के संकुचन समारोह में कमी के साथ-साथ चालन और हृदय ताल की गड़बड़ी की ओर जाता है। मस्तिष्क में सेनील एमिलॉयडोसिस के साथ, एमिलॉयड कॉर्टेक्स, जहाजों और झिल्ली के तथाकथित सेनील प्लेक में पाया जाता है। त्वचा में, अमाइलॉइड पैपिला और संवहनी दीवारों में जमा हो जाता है, जिससे एपिडर्मिस का तेज शोष होता है। यकृत में, अमाइलॉइड साइनसॉइडल वाहिकाओं के तारकीय रेटिकुलोएन्डोथेलियोसाइट्स के बीच, वाहिकाओं, नलिकाओं की दीवारों में और पोर्टल पथ के संयोजी ऊतक में जमा होता है। जैसे ही अमाइलॉइड जमा होता है, यकृत कोशिकाएं शोष करती हैं।
गुर्दे में, अमाइलॉइड ग्लोमेरुलर केशिकाओं और नेफ्रॉन के नलिकाओं की झिल्ली में, मेसेंजियम, केशिका छोरों और धमनी के साथ जमा होता है। जैसे ही अमाइलॉइड जमा होता है, अधिकांश नेफ्रॉन शोष, मर जाते हैं, या संयोजी ऊतक द्वारा प्रतिस्थापित किए जाते हैं - एक अमाइलॉइड-सिकुड़ा हुआ गुर्दा प्रकट होता है। इस प्रक्रिया को निम्नलिखित आरेख के रूप में दर्शाया जा सकता है:
प्रोटीनुरिया -> नेफ्रोटिक सिंड्रोम -> गुर्दे की विफलता।
तदनुसार, नैदानिक तस्वीर में तीन चरणों को प्रतिष्ठित किया जाता है: 1) प्रारंभिक (प्रोटीन्यूरिक); 2) तैनात (नेफ्रोटिक); 3) टर्मिनल (एज़ोटेमिक)।
नैदानिक तस्वीर।अमाइलॉइडोसिस की अभिव्यक्तियाँ विविध हैं और इसके द्वारा निर्धारित की जाती हैं: 1) किसी विशेष अंग में अमाइलॉइड का स्थानीयकरण; 2) अंग में अमाइलॉइड जमा की गंभीरता की डिग्री; 3) मुख्य बीमारी जिसके खिलाफ अमाइलॉइड विकसित हुआ (अमाइलॉइडोसिस के द्वितीयक रूप के साथ)।
निदान में कठिनाइयाँ उत्पन्न हो सकती हैं, इस तथ्य के कारण कि रोग की नैदानिक अभिव्यक्तियाँ केवल एक निश्चित मात्रा में जमा अमाइलॉइड के साथ ध्यान देने योग्य होंगी। इस संबंध में, एक "अव्यक्त" अवधि अमाइलॉइड के जमाव के क्षण से लेकर किसी अंग या प्रणाली के बिगड़ा हुआ कामकाज के लक्षणों की उपस्थिति तक अपरिहार्य है।
गुर्दे की क्षति के मामले में नैदानिक तस्वीर विशेष रूप से उज्ज्वल है, एमिलॉयड जमा का सबसे आम स्थानीयकरण।
प्रारंभिक चरण में नैदानिक खोज के पहले चरण में, व्यावहारिक रूप से अमाइलॉइडोसिस द्वारा गुर्दे की क्षति का संकेत देने वाली कोई जानकारी प्राप्त नहीं की जा सकती है। रोगियों की शिकायतें अंतर्निहित बीमारी (द्वितीयक अमाइलॉइडोसिस के साथ) से जुड़ी होती हैं।
इतिहास में एक विशेष बीमारी (फुफ्फुसीय तपेदिक, अस्थिमज्जा का प्रदाह, संधिशोथ, आदि), इसके पाठ्यक्रम और चिकित्सा की उपस्थिति के बारे में जानकारी है। अपने आप में, यह जानकारी गुर्दे के अमाइलॉइडोसिस का निदान करने की अनुमति नहीं देती है, लेकिन इस संभावना पर डॉक्टर का ध्यान आकर्षित करती है।
अमाइलॉइडोसिस के उन्नत चरण में, रोगी नेफ्रोटिक सिंड्रोम के विकास के कारण, मूत्र की मात्रा में कमी, अलग-अलग प्रसार और गंभीरता के साथ-साथ कमजोरी, भूख की कमी और प्रदर्शन में कमी की शिकायत करते हैं। उनके साथ, माध्यमिक अमाइलॉइडोसिस में, अंतर्निहित बीमारी की अभिव्यक्ति के बारे में शिकायतें हैं।
अंतिम चरण में, पुरानी गुर्दे की विफलता के विकास के कारण शिकायतें होती हैं: भूख में कमी, मतली, उल्टी (अपच संबंधी विकार), सिरदर्द, नींद की गड़बड़ी (तंत्रिका तंत्र विकार), त्वचा की खुजली।
नैदानिक खोज के चरण II में, प्रारंभिक अवस्था में केवल अंतर्निहित बीमारी (द्वितीयक अमाइलॉइडोसिस के साथ) की विशेषता वाले लक्षणों का पता लगाया जा सकता है।
पर उच्च चरणप्रकट करें: 1) विभिन्न स्थानीयकरण और अभिव्यंजना के हाइपोस्टेसिस; शरीर में महत्वपूर्ण द्रव प्रतिधारण के साथ, हाइड्रोथोरैक्स, हाइड्रोपेरिकार्डियम, क्षणिक जलोदर दिखाई दे सकता है; 2) धमनी उच्च रक्तचाप (एमाइलॉयडोसिस वाले 12-20% रोगियों में होता है), बाएं वेंट्रिकल का फैलाव और अतिवृद्धि; 3) ऊतकों में अमाइलॉइड के जमाव के कारण यकृत और प्लीहा में वृद्धि (यकृत और प्लीहा घने, दर्द रहित, नुकीले किनारे वाले होते हैं); 4) अंतर्निहित बीमारी के लक्षण (माध्यमिक अमाइलॉइडोसिस के साथ)।
पर टर्मिनल चरणलक्षण गुर्दे की विफलता की गंभीरता से निर्धारित होते हैं: 1) डिस्ट्रोफिक सिंड्रोम (त्वचा और श्लेष्म झिल्ली में परिवर्तन); 2) सीरस-आर्टिकुलर सिंड्रोम (ऑस्टियोआर्थ्रोपैथी, सेकेंडरी गाउट, ड्राई पेरिकार्डिटिस, फुफ्फुस); 3) धमनी उच्च रक्तचाप।
अमाइलॉइडोसिस के लिए नैदानिक खोज के चरण III में, निदान करने के लिए सबसे महत्वपूर्ण जानकारी प्राप्त की जाती है, जिसे निम्नानुसार समूहीकृत किया जा सकता है: 1) मूत्र सिंड्रोम; 2) प्रोटीन और लिपिड चयापचय का उल्लंघन; 3) अमाइलॉइड द्रव्यमान के जमाव का पता लगाना।
मूत्र संबंधी सिंड्रोम: 1) प्रोटीनमेह - अमाइलॉइडोसिस का सबसे महत्वपूर्ण लक्षण, अपने सभी रूपों में विकसित होता है, लेकिन ज्यादातर माध्यमिक अमाइलॉइडोसिस में। प्रोटीनुरिया आमतौर पर महत्वपूर्ण होता है, प्रति दिन 2-20 ग्राम प्रोटीन निकलता है, जिसका मुख्य भाग एल्ब्यूमिन होता है। कम मात्रा में, ग्लोब्युलिन उत्सर्जित होते हैं, मूत्र में सीरम अमाइलॉइड अग्रदूत (एसएए प्रोटीन) का उत्सर्जन संभव है। अंतिम चरण में, प्रोटीनुरिया बना रहता है। मूत्र में, a- और विशेष रूप से y-ग्लाइकोप्रोटीन का पता लगाया जा सकता है।
प्रोटीनुरिया की डिग्री के अनुसार, हाइलिन और कम बार दानेदार कास्ट पाए जाते हैं। अक्सर, माइक्रोहेमेटुरिया या ल्यूकोसाइटुरिया का निदान किया जाता है, लेकिन इसकी गंभीरता प्रोटीनुरिया की डिग्री के अनुरूप नहीं होती है (जैसा कि ग्लोमेरुलोनेफ्राइटिस के साथ देखा जाता है)। अमाइलॉइडोसिस में लिपिड चयापचय विकारों की डिग्री मूत्र तलछट में द्विअर्थी क्रिस्टल की उपस्थिति के साथ लिपोइडुरिया से मेल खाती है।
प्रोटीन और लिपिड चयापचय विकार: 1) हाइपोप्रोटीनेमिया हाइपोएल्ब्यूमिनमिया और हाइपर के साथ संयोजन में-<Х2- и гипергаммаглобулинемией; 2) гиперхолестеринемия, гипертриглицеридемия, гипербеталипопротеиде-мия. Выраженная диспротеинемия и нарушения липидного обмена приводят к значительному увеличению СОЭ и изменению осадочных проб (тимоловая, сулемовая и др.).
निदान के लिए महत्वपूर्ण है अंगों और ऊतकों में अमाइलॉइड द्रव्यमान का पता लगाना:जिगर में (50% मामलों में), प्लीहा (पंचर बायोप्सी के साथ), मसूड़ों और मलाशय की श्लेष्मा झिल्ली।
प्रारंभिक चरण (प्रोटीन्यूरिक) में, मसूड़ों के श्लेष्म झिल्ली की बायोप्सी अक्सर नकारात्मक परिणाम देती है, और मलाशय - एक सकारात्मक परिणाम; पहले मामले में उन्नत चरण (नेफ्रोटिक) में, परिणाम आधे रोगियों में सकारात्मक होते हैं, और दूसरे में - और भी अधिक बार।
अंत में, क्रोनिक रीनल फेल्योर में, आधे से अधिक मामलों में मसूड़े के ऊतकों का बायोप्सी डेटा सकारात्मक होता है, और लगभग सभी मामलों में रेक्टल म्यूकोसा का। इसलिए, उन्नत प्रक्रिया के लिए मसूड़े के म्यूकोसा की बायोप्सी की सिफारिश की जानी चाहिए, और अमाइलॉइडोसिस के किसी भी स्तर पर रेक्टल बायोप्सी की सिफारिश की जानी चाहिए।
यदि अज्ञातहेतुक अमाइलॉइडोसिस का संदेह है (हृदय, परिधीय नसों, कम अक्सर - गुर्दे को नुकसान के साथ होता है), तो सबसे पहले गम म्यूकोसा की बायोप्सी करने की सलाह दी जाती है, और माध्यमिक (अधिग्रहित) एमाइलॉयडोसिस और इसके मामले में वंशानुगत रूप (गुर्दे को प्रमुख क्षति के साथ होते हैं) - श्लेष्म झिल्ली मलाशय की बायोप्सी।
कई अन्य अध्ययन मदद करते हैं: 1) उस बीमारी के निदान को स्पष्ट करें, जिसके खिलाफ अमाइलॉइडोसिस विकसित हुआ; 2) गुर्दे की कार्यात्मक स्थिति का आकलन करें (रीबर्ग परीक्षण, ज़िमनिट्स्की परीक्षण, रक्त क्रिएटिनिन स्तर)।
प्रवाह। गुर्दे की अमाइलॉइडोसिस की नैदानिक तस्वीर में ऐसी विशेषताएं हैं जो इसे एक अलग मूल के गुर्दे की क्षति से अलग करती हैं: 1) नेफ्रोटिक सिंड्रोम धीरे-धीरे विकसित होता है और अक्सर प्रोटीनूरिया के एक लंबे चरण के बाद, एक निरंतर पाठ्यक्रम की विशेषता होती है, एडिमा अक्सर विभिन्न मूत्रवर्धक के लिए प्रतिरोधी होती है। सीजीएन के साथ, नेफ्रोटिक सिंड्रोम, एक नियम के रूप में, पहले से ही रोग की शुरुआत में होता है और अक्सर भविष्य में पुनरावृत्ति होता है; 2) धमनी उच्च रक्तचाप शायद ही कभी मनाया जाता है, यहां तक कि पुरानी गुर्दे की विफलता के चरण में भी; 3) प्राथमिक अमाइलॉइडोसिस में, पुरानी गुर्दे की विफलता माध्यमिक अमाइलॉइडोसिस या सीजीएन के विपरीत अधिक सौम्य रूप से आगे बढ़ती है (अमाइलॉइडोसिस के माध्यमिक रूपों की तुलना में ग्लोमेरुलर क्षति की कम गंभीरता के कारण); 4) माध्यमिक अमाइलॉइडोसिस का कोर्स काफी हद तक अंतर्निहित बीमारी पर निर्भर करता है, जिसके लगातार तेज होने से एमाइलॉयडोसिस की एक महत्वपूर्ण प्रगति संभव है।
जटिलताएं। 2-5% मामलों में अमाइलॉइडोसिस के साथ विकसित होता है:
1) गुर्दे की शिरा घनास्त्रता (माध्यमिक अमाइलॉइडोसिस के साथ), जो प्रकट होता है
हेमट्यूरिया और काठ का क्षेत्र में दर्द, प्रोटीन में वृद्धि
रिया और मूत्राधिक्य में गिरावट;
2) परस्पर संक्रमण;
3) फाइब्रिनस-प्यूरुलेंट पेरिटोनिटिस, जिसकी उपस्थिति के साथ है
जलोदर में तेज वृद्धि होती है।
निदान।अमाइलॉइडोसिस की नैदानिक अभिव्यक्तियाँ निरर्थक हैं। प्रत्येक लक्षण (एडिमा, प्रोटीनुरिया, धमनी उच्च रक्तचाप) गुर्दे की विभिन्न बीमारियों में हो सकता है। अमाइलॉइडोसिस के विश्वसनीय निदान के लिए एकमात्र तरीका एक अंग (गुर्दे, यकृत, मलाशय के श्लेष्म या मसूड़ों) की बायोप्सी है, लेकिन यह हमेशा संभव नहीं होता है। इसलिए, ज्यादातर मामलों में रोग प्रक्रिया की नैदानिक अभिव्यक्तियों पर ध्यान देना आवश्यक है।
एक बीमारी की उपस्थिति जिसमें एक माध्यमिक
अमाइलॉइडोसिस (नैदानिक या anamnestic संकेत)।
प्रोटीनुरिया या शुरुआत की शुरुआत और प्रगति
गुर्दे का रोग।
ऐसी कोई बीमारी नहीं है जिसमें अमाइलॉइडोसिस विकसित हो सकता है,
हालांकि, प्रोटीनूरिया या नेफ्रोटिक सिंड्रोम है।
लगातार गंभीर दिल की विफलता की उपस्थिति, सिंड्रोम नहीं है
अवशोषण पर्याप्तता, पोलीन्यूरोपैथी (यदि एक ही समय में अंतिम)
अन्य कारणों से तीन सिंड्रोम की व्याख्या करना मुश्किल है)।
नेफ्रोटिक सिंड्रोम के निम्नलिखित प्रयोगशाला संकेतों के साथ अमाइलॉइडोसिस की उपस्थिति का संदेह किया जा सकता है (जो, जैसा कि आप जानते हैं, गुर्दे की अन्य बीमारियों के साथ विकसित हो सकता है):
ए) गंभीर डिस्प्रोटीनेमिया + हाइपोएल्ब्यूमिनमिया + हाइपर-एसजी- और जीआई-
पेर्गामाग्लोबुलिनमिया;
बी) एजी-ग्लाइकोप्रोटीन, पी-लिपोप्रोटीन के स्तर में वृद्धि;
ग) मूत्र में ए- और विशेष रूप से वाई-ग्लाइकोप्रोटीन और ए-लिपोप्रो-
टीड्स
सभी मामलों में, हेपेटो- और स्प्लेनोमेगाली का पता लगाने के साथ-साथ एमाइलॉयडोसिस की हृदय विशेषता में परिवर्तन के साथ एमाइलॉयडोसिस विकसित होने की संभावना बढ़ जाती है (ऐसे मामलों में, हम इडियोपैथिक सामान्यीकृत एमाइलॉयडोसिस के बारे में बात कर रहे हैं)।
इसलिए, गुर्दे की अमाइलॉइडोसिस का निदान उन्नत (नेफ्रोटिक) या टर्मिनल चरण में पर्याप्त निश्चितता के साथ किया जा सकता है, जबकि प्रारंभिक (प्रोटीन्यूरिक) चरण में ऐसा करना अधिक कठिन होता है। इन मामलों में, क्षणिक या स्थायी प्रोटीनमेह को ग्लोमेरुलोनेफ्राइटिस (तीव्र, जीर्ण) से अलग किया जाना चाहिए। इसे ध्यान में रखना चाहिए:
1) अमाइलॉइड में गुर्दे की क्षति की धीमी प्रगति
खुराक;
2) अमाइलॉइडोसिस में सर्दी के साथ स्पष्ट संबंध का अभाव
नियामी;
3) ग्लोमेरुलोनेफ्राइटिस में माइक्रोहेमेटुरिया की निरंतर उपस्थिति (साथ .)
20% मामलों में अमाइलॉइडोसिस)।
कभी-कभी रोगी के लंबे अवलोकन की अवधि के बाद ही सही निदान किया जा सकता है। यदि गुर्दे की पंचर बायोप्सी करना संभव हो तो समस्या का समाधान बहुत तेजी से होता है।
एक विस्तृत नैदानिक निदान का निरूपणअमाइलॉइडोसिस निम्नलिखित घटकों को ध्यान में रखता है: 1) अमाइलॉइडोसिस का रूप; 2) अमाइलॉइडोसिस का चरण (प्रोटीन्यूरिक, नेफ्रोटिक, टर्मिनल); 3) गुर्दे की कार्यात्मक स्थिति (गुर्दे की विफलता की अनुपस्थिति या उपस्थिति, इसकी गंभीरता की डिग्री); 4) अंतर्निहित बीमारी (माध्यमिक अमाइलॉइडोसिस के साथ); 5) अज्ञातहेतुक (प्राथमिक) अमाइलॉइडोसिस में अन्य अंगों (हृदय, यकृत, तंत्रिका तंत्र, आदि) की स्थिति।
इलाज।अमाइलॉइडोसिस के इलाज की समस्या अभी भी अनसुलझी बनी हुई है, क्योंकि अमाइलॉइडोजेनेसिस में वृद्धि और इसके पुनर्जीवन की अपर्याप्तता के कारणों को स्पष्ट नहीं किया गया है। फिर भी, रोगी की स्थिति में सुधार करने वाले चिकित्सीय उपायों की एक श्रृंखला करना संभव है। वर्तमान में, अमाइलॉइडोसिस वाले रोगी का उपचार निम्नलिखित को ध्यान में रखते हुए किया जाता है: 1) अंतर्निहित रोग पर प्रभाव, जिसके विरुद्ध अमाइलॉइडोसिस विकसित हुआ
(माध्यमिक); 2) रोगजनन के तंत्र पर प्रभाव; 3) मुख्य नैदानिक सिंड्रोम पर प्रभाव।
अंतर्निहित बीमारी पर प्रभाव, जिसके खिलाफ यह विकसित होता है
माध्यमिक अमाइलॉइडोसिस, इस तथ्य को ध्यान में रखते हुए आवश्यक है कि बार-बार
रोग प्रक्रिया की स्ट्राई या उच्च गतिविधि के कारण
अमाइलॉइडोसिस की प्रगति।
यह प्रभाव इस प्रकार है:
क) पुराने संक्रमण (तपेदिक, उपदंश) में
दीर्घकालिक विशिष्ट चिकित्सा;
बी) पुरानी गैर-विशिष्ट फेफड़ों की बीमारियों में - कॉम
एंटीबायोटिक दवाओं के साथ प्लेक्स थेरेपी, ब्रोन्कियल ड्रेनेज, और
यदि आवश्यक हो, और शल्य चिकित्सा हस्तक्षेप (उदाहरण के लिए, पुरानी के साथ
फेफड़े का फोड़ा);
ग) संयोजी ऊतक के प्रणालीगत रोगों के साथ, उदाहरण के लिए, के साथ
संधिशोथ, जटिल चिकित्सा का संकेत दिया जाता है, जिसमें शामिल हैं
मूल तैयारी का मूल्य (डी-पेनिसिलमाइन, सोना लवण, अमीनो-
नोलिन ड्रग्स)।
रोगजनन के तंत्र पर प्रभाव में कमी शामिल है
अमाइलॉइड संश्लेषण:
क) 6-12 महीनों के लिए प्रतिदिन 80-120 ग्राम कच्चे जिगर का सेवन
प्रोटीनमेह में कमी, यकृत के आकार में कमी की ओर जाता है
न ही तिल्ली;
बी) एमिनोक्विनोलिन की तैयारी (हिंगामिन, या डेलगिल, के अनुसार
0.25 - 0.5 ग्राम प्रति दिन कई महीनों और वर्षों तक)
yut प्रक्रिया की प्रगति। जाहिर है, प्रभाव के ये साधन
यूट अमाइलॉइड फाइब्रिल के संश्लेषण पर। इलाज ही कारगर
अमाइलॉइडोसिस के शुरुआती चरणों में; एक उन्नत प्रक्रिया में
(विस्तृत नेफ्रोटिक सिंड्रोम, गुर्दे की कमी)
नेस) इन दवाओं की नियुक्ति अव्यावहारिक है;
ग) आवधिक बीमारी के कारण अमाइलॉइडोसिस के विकास के साथ पुन:
कोल्सीसिन की सिफारिश की जाती है;
डी) प्राथमिक अमाइलॉइडोसिस में, मेलफलन भी निर्धारित किया जाता है, जो रोकता है
लिम्फोसाइटों के कुछ क्लोनों का कार्य, विशेष रूप से syn
टाइपिंग लाइट चेन इम्युनोग्लोबुलिन शामिल हैं
अमाइलॉइड तंतु का बनना (यह भी संबंधित है
अमाइलॉइडोसिस, जो मल्टीपल मायलोमा में विकसित होता है)।
मुख्य नैदानिक सिंड्रोम पर प्रभाव में शामिल हैं
एडिमा, उच्च रक्तचाप, साथ ही उपायों के उद्देश्य से उन्मूलन
गुर्दे की विफलता के विकास के खिलाफ लड़ाई:
ए) नेफ्रोटिक सिंड्रोम और गंभीर एडिमा के विकास के साथ
भोजन में प्रोटीन की पर्याप्त मात्रा आवश्यक है, में कमी
उबला हुआ नमक, साथ ही पूरे रक्त या एरिथ्रोसाइट की शुरूआत-
नोय मास (विशेषकर एनीमिया की उपस्थिति में), सावधानीपूर्वक आवेदन
मूत्रवर्धक का उपयोग;
बी) धमनी उच्च रक्तचाप शायद ही कभी अमाइलॉइडोसिस में होता है,
हालाँकि, जब यह उच्च संख्या में पहुँच जाता है, तो इसे नियुक्त करना आवश्यक होता है
विभिन्न प्रकार की उच्चरक्तचापरोधी दवाओं का उपयोग;
ग) गुर्दे की विफलता के विकास के साथ, आम तौर पर स्वीकृत योजना (भोजन में प्रोटीन का प्रतिबंध, पर्याप्त तरल पदार्थ का सेवन, खनिज चयापचय में सुधार) के अनुसार उपचार किया जाता है। अमाइलॉइडोसिस के कारण गुर्दे की विफलता में, हेमोडायलिसिस और गुर्दा प्रत्यारोपण का उपयोग करना संभव है।
भविष्यवाणी।प्रोटीन्यूरिक अवधि की अवधि को स्थापित करना मुश्किल है, हालांकि, इसकी पहचान के बाद, एडिमा आमतौर पर 3 साल बाद विकसित होती है, जिसके खिलाफ सीआरएफ जल्दी विकसित होता है। यह सब पूर्वानुमान को काफी गंभीर बनाता है।
निवारण।अज्ञातहेतुक और आनुवंशिक अमाइलॉइडोसिस में, प्राथमिक रोकथाम के उपाय अज्ञात हैं। माध्यमिक अमाइलॉइडोसिस में, रोकथाम में बीमारियों के उपचार में शामिल होता है जिससे एमिलॉयडोसिस का विकास होता है।
RCHD (कजाकिस्तान गणराज्य के स्वास्थ्य मंत्रालय के स्वास्थ्य विकास के लिए रिपब्लिकन केंद्र)
संस्करण: कजाकिस्तान गणराज्य के स्वास्थ्य मंत्रालय के नैदानिक प्रोटोकॉल - 2016
अमाइलॉइडोसिस (E85)
नेफ्रोलॉजी
सामान्य जानकारी
संक्षिप्त वर्णन
स्वीकृत
चिकित्सा सेवाओं की गुणवत्ता पर संयुक्त आयोग
कजाकिस्तान गणराज्य के स्वास्थ्य और सामाजिक विकास मंत्रालय
दिनांक 13 अक्टूबर 2016
प्रोटोकॉल #13
अमाइलॉइडोसिस- रोगों का एक समूह, जिसकी पहचान फाइब्रिलर ग्लाइकोप्रोटीन - अमाइलॉइड के ऊतकों और अंगों में जमाव है।
ICD-10 और ICD-9 कोड के बीच संबंध
| आईसीडी -10 | आईसीडी-9 | ||
| कोड | नाम | कोड | नाम |
| ई85 | अमाइलॉइडोसिस |
55.23 99.76 |
बंद [परक्यूटेनियस] [पंचर] किडनी बायोप्सी। हेमोडायलिसिस। चिकित्सीय प्लास्मफेरेसिस एक्स्ट्राकोर्पोरियल इम्यूनोएडॉर्प्शन |
| ई85.0 | न्यूरोपैथी के बिना वंशानुगत पारिवारिक अमाइलॉइडोसिस | ||
| ई85.1 | न्यूरोपैथिक वंशानुगत अमाइलॉइडोसिस | ||
| ई85.2 | वंशानुगत अमाइलॉइडोसिस, अनिर्दिष्ट | ||
| ई85.3 | माध्यमिक प्रणालीगत अमाइलॉइडोसिस | ||
| ई85.4 | सीमित अमाइलॉइडोसिस | ||
| E85.8 | अमाइलॉइडोसिस के अन्य रूप | ||
| ई85.9 | अमाइलॉइडोसिस, अनिर्दिष्ट | ||
प्रोटोकॉल के विकास/संशोधन की तिथि: 2016।
प्रोटोकॉल उपयोगकर्ता:सामान्य चिकित्सक, चिकित्सक, रुधिरविज्ञानी, नेफ्रोलॉजिस्ट।
साक्ष्य स्तर का पैमाना:
| लेकिन | उच्च गुणवत्ता वाले मेटा-विश्लेषण, आरसीटी की व्यवस्थित समीक्षा, या पूर्वाग्रह की बहुत कम संभावना (++) वाले बड़े आरसीटी जिनके परिणाम उपयुक्त आबादी के लिए सामान्यीकृत किए जा सकते हैं। |
| पर | उच्च-गुणवत्ता (++) कोहोर्ट या केस-कंट्रोल स्टडीज की व्यवस्थित समीक्षा या उच्च-गुणवत्ता (++) कॉहोर्ट या केस-कंट्रोल स्टडीज जिसमें पूर्वाग्रह या आरसीटी के बहुत कम जोखिम के साथ पूर्वाग्रह का कम (+) जोखिम होता है, के परिणाम जिसे उपयुक्त जनसंख्या के लिए सामान्यीकृत किया जा सकता है। |
| से |
पूर्वाग्रह (+) के कम जोखिम के साथ यादृच्छिकरण के बिना समूह या केस-नियंत्रण या नियंत्रित परीक्षण। जिसके परिणामों को उपयुक्त जनसंख्या या आरसीटी के लिए पूर्वाग्रह (++ या +) के बहुत कम या कम जोखिम के साथ सामान्यीकृत किया जा सकता है, जिसके परिणाम सीधे उपयुक्त आबादी के लिए सामान्यीकृत नहीं किए जा सकते हैं। |
| डी | केस सीरीज़ या अनियंत्रित अध्ययन या विशेषज्ञ की राय का विवरण। |
वर्गीकरण
अमाइलॉइड प्रकार और अमाइलॉइडोसिस के संबंधित रूप:
|
प्रोटीन कलफ़ |
अग्रदूत प्रोटीन | अमाइलॉइडोसिस का नैदानिक रूप |
| आ | एसएए प्रोटीन | आवधिक बीमारी और मकल-वेल्स सिंड्रोम सहित पुरानी सूजन संबंधी बीमारियों में माध्यमिक अमाइलॉइडोसिस |
| अली | , -इम्युनोग्लोबुलिन की हल्की शृंखला | प्लाज्मा सेल डिस्क्रेसियास में अमाइलॉइडोसिस - इडियोपैथिक, मल्टीपल मायलोमा और वाल्डेनस्ट्रॉम के मैक्रोग्लोबुलिनमिया में |
| एटीटीआर | ट्रान्सथायरेटिन | पोलीन्यूरोपैथिक, कार्डियोपैथिक और अन्य अमाइलॉइडोसिस के पारिवारिक रूप, प्रणालीगत सेनील अमाइलॉइडोसिस |
| Aβ2M | β2-माइक्रोग्लोब्युलिन | डायलिसिस अमाइलॉइडोसिस |
| एगेल | जेल्सोलिन | फ़िनिश पारिवारिक अमाइलॉइड पोलीन्यूरोपैथी |
| एएपीओएआई | अपोलिपोप्रोटीन A-I | अमाइलॉइड पोलीन्यूरोपैथी (टाइप III, वैन एलन के अनुसार, 1956) |
| AFIB | फाइब्रिनोजेन | अमाइलॉइड अपवृक्कता |
| एβ | β प्रोटीन | अल्जाइमर रोग, डाउन सिंड्रोम, अमाइलॉइडोसिस के साथ वंशानुगत मस्तिष्क रक्तस्राव, हॉलैंड |
| एपीआरपी स्क्रू | प्रियन प्रोटीन | Creutzfeldt-Jakob रोग, Gerstmann-Straussler-Scheinker रोग |
| एएएनएफ | आलिंद नैट्रियूरेटिक कारक | पृथक आलिंद अमाइलॉइडोसिस |
| एआईएपीपी | एमिलिन | टाइप II डायबिटीज मेलिटस, इंसुलिनोमा में लैंगरहैंस के आइलेट्स में पृथक अमाइलॉइडोसिस |
| एसील | प्रोकैल्सीटोनिन | मेडुलरी थायराइड कैंसर के लिए |
| एसीआईएस | सिस्टैटिन सी | अमाइलॉइडोसिस, आइसलैंड के साथ वंशानुगत मस्तिष्क रक्तस्राव |
अमाइलॉइडोसिस का नैदानिक वर्गीकरण
प्राथमिक अमाइलॉइडोसिस:
बिना किसी स्पष्ट कारण के घटित होना;
एकाधिक माइलोमा के साथ संबद्ध
माध्यमिक अमाइलॉइडोसिस:
जीर्ण संक्रमण में;
संधिशोथ और अन्य संयोजी ऊतक रोगों में;
ऑन्कोलॉजिकल रोगों में;
पारिवारिक (वंशानुगत) अमाइलॉइडोसिस:
आवधिक बीमारी के मामले में;
पुर्तगाली संस्करण और पारिवारिक अमाइलॉइडोसिस के अन्य रूप;
बूढ़ा अमाइलॉइडोसिस
स्थानीय अमाइलॉइडोसिस
वंशानुगत अमाइलॉइडोसिस:
न्यूरोपैथिक
निचले छोरों को नुकसान के साथ: पुर्तगाली, जापानी, स्वीडिश और अन्य प्रकार;
ऊपरी अंगों के घावों के साथ: स्विट्जरलैंड-इंडियाना, जर्मनी-मैरीलैंड के प्रकार;
नेफ्रोपैथिक:
आवधिक बीमारी
स्वीडन और सिसिली में बुखार और पेट दर्द;
दाने, बहरापन और गुर्दे की क्षति का एक संयोजन;
धमनी उच्च रक्तचाप के साथ संयोजन में गुर्दे की क्षति;
कार्डियोमायोपैथिक:
डेनिश - प्रगतिशील दिल की विफलता;
मैक्सिकन-अमेरिकी - बीमार साइनस सिंड्रोम, आलिंद गिरफ्तारी;
मिला हुआ:
फिनिश - कॉर्नियल डिस्ट्रोफी और कपाल नसों को नुकसान;
मस्तिष्क आघात।
गुर्दे के अमाइलॉइडोसिस के नैदानिक चरण
| मंच | नैदानिक प्रत्यक्षीकरण |
| 1 | प्रीक्लिनिकल या अव्यक्त (स्पर्शोन्मुख) चरण - अमाइलॉइड मध्यवर्ती क्षेत्र में मौजूद होता है और पिरामिड के सीधे जहाजों के साथ एडिमा और स्केलेरोसिस के फॉसी विकसित होते हैं। चरण 3-5 या अधिक वर्षों तक रहता है। इस अवधि के दौरान, प्रतिक्रियाशील अमाइलॉइडोसिस अंतर्निहित बीमारी (उदाहरण के लिए, फेफड़ों में शुद्ध प्रक्रिया, तपेदिक, संधिशोथ गठिया, आदि) के नैदानिक अभिव्यक्तियों का प्रभुत्व है। |
| 2 | प्रोटीन्यूरिक (एल्ब्यूमिन्यूरिक) चरण - अमाइलॉइड मुख्य रूप से मेसेंजियम में, केशिकाओं के छोरों में, पिरामिड में और ग्लोमेरुली के कॉर्टिकल पदार्थ में, जहाजों में दिखाई देता है। नेफ्रॉन, हाइपरमिया और लिम्फोस्टेसिस के स्केलेरोसिस और शोष विकसित होते हैं। गुर्दे बढ़े हुए और घने, सुस्त भूरे-गुलाबी रंग के होते हैं। शुरुआत में प्रोटीनुरिया मध्यम रूप से व्यक्त किया जाता है, यह कुछ अवधि के लिए क्षणिक भी हो सकता है, घट सकता है और बढ़ सकता है, लेकिन फिर लगातार (आंतरायिक प्रोटीनमेह का चरण) हो जाता है। कुछ शोधकर्ता इस चरण में दो अवधियों को भेद करते हैं: चयनात्मक और गैर-चयनात्मक प्रोटीनुरिया। चरण की अवधि 10 से 13 वर्ष तक है। |
| 3 | नेफ्रोटिक (एडेमेटस, एडेमेटस-हाइपोटोनिक) चरण - एमाइलॉयड-लिपोइड नेफ्रोसिस - नेफ्रॉन के सभी हिस्सों में एमाइलॉयड। मज्जा का काठिन्य और अमाइलॉइडोसिस है, लेकिन स्पष्ट स्क्लेरोटिक परिवर्तनों के बिना कॉर्टिकल परत। चरण की अवधि 6 वर्ष तक है। प्रोटीन्यूरिक और नेफ्रोटिक दोनों चरणों में, गुर्दे बढ़े हुए, घने (बड़े वसामय गुर्दे) होते हैं। नैदानिक रूप से, यह चरण क्लासिक नेफ्रोटिक सिंड्रोम द्वारा अपने सभी संकेतों के साथ प्रकट होता है: बड़े पैमाने पर प्रोटीनमेह के विकास के साथ (प्रति दिन 3-5 ग्राम से अधिक के मूत्र में प्रोटीन की हानि के साथ), हाइपोप्रोटीनेमिया हाइपोएल्ब्यूमिनमिया, हाइपरकोलेस्ट्रोलेमिया, लिपिडुरिया के साथ एडिमा अनासारका की डिग्री तक। मूत्र तलछट में हाइलिन कास्ट पाए जाते हैं, और जैसे-जैसे प्रोटीनूरिया बढ़ता है, दानेदार कास्ट पाए जाते हैं। पाइलोनफ्राइटिस के संकेतों के बिना संभव सूक्ष्म और मैक्रोहेमेटुरिया, ल्यूकोसाइटुरिया। |
| 4 | यूरेमिक (टर्मिनल, एज़ोटेमिचेस्की) चरण - अमाइलॉइड झुर्रीदार गुर्दा - आकार में कम, घने, खराब गुर्दे। क्रोनिक रीनल फेल्योर अन्य किडनी रोगों से बहुत कम भिन्न होता है। यह माना जाता है कि ग्लोमेरुलोनेफ्राइटिस के विपरीत, जिसमें पॉलीयूरिया के साथ होने वाली सीआरएफ की शुरुआत से एडिमा का कम से कम आंशिक अभिसरण हो सकता है, एमाइलॉयडोसिस में, एज़ोटेमिया निम्न रक्तचाप और नेफ्रोटिक सिंड्रोम की पृष्ठभूमि के खिलाफ विकसित होता है। |
डायग्नोस्टिक्स (आउट पेशेंट क्लिनिक)
आउट पेशेंट स्तर पर निदान
नैदानिक मानदंड
शिकायतें:
कमजोरी, थकान में वृद्धि;
· सरदर्द;
पैरों, बाहों और चेहरे में सूजन;
उच्च रक्तचाप;
मतली, दस्त (दस्त);
दिल के क्षेत्र में दर्द;
मांसपेशियों में दर्द।
इतिहास:
· वजन घटना;
अज्ञात मूल के मोनोक्लोनल गैमोपैथी की उपस्थिति;
पुरानी सूजन (प्यूरुलेंट) रोग;
जीर्ण संक्रमण;
वंशागति।
शारीरिक जाँच
सामान्य निरीक्षण:
पेरिओरिबिटल पुरपुरा (15% मामलों में देखा गया);
मैक्रोग्लोसिया प्राथमिक अमाइलॉइडोसिस (एएल) की विशेषता है;
शारीरिक परिश्रम के दौरान सांस की तकलीफ (लगभग 40% रोगियों में देखी गई);
कंधे का चिन्ह (अमाइलॉइड के पेरीआर्टिकुलर घुसपैठ से झूठी अतिवृद्धि होती है और कंधे की कमर और जांघ की मांसपेशियों की मात्रा में वृद्धि होती है)।
गुदाभ्रंश:
कार्डियक अतालता की संभावित उपस्थिति।
पैल्पेशन:
निचले छोरों की सूजन, हाइपोएल्ब्यूमिनमिया और नेफ्रोटिक सिंड्रोम के कारण, साथ ही प्रतिबंधात्मक कार्डियोमायोपैथी के कारण प्रणालीगत परिसंचरण में ठहराव के कारण (50% मामलों में मनाया जाता है);
जिगर और प्लीहा का इज़ाफ़ा;
पेरेस्टेसिया (लगभग 15% रोगियों में देखा गया);
जठरांत्र संबंधी मार्ग में स्पास्टिक दर्द;
सबमांडिबुलर लार ग्रंथियों में वृद्धि हो सकती है।
प्रयोगशाला अनुसंधान:
पूर्ण रक्त गणना - एनीमिया, ल्यूकोसाइटोसिस, ईएसआर में वृद्धि;
सामान्य मूत्र विश्लेषण - प्रोटीनमेह, माइक्रोहेमेटुरिया, सड़न रोकनेवाला ल्यूकोसाइटुरिया;
जैव रासायनिक रक्त परीक्षण (कुल प्रोटीन, एल्ब्यूमिन, Na, Ca, कोलेस्ट्रॉल, रक्त सीरम में शर्करा) - हाइपोप्रोटीनेमिया (हाइपोएल्ब्यूमिनमिया के कारण), हाइपरग्लोबुलिनमिया, हाइपोनेट्रेमिया, हाइपोप्रोथ्रोम्बिनमिया, हाइपोकैल्सीमिया, हाइपरकोलेस्ट्रोलेमिया।
पेट के अंगों और गुर्दे का अल्ट्रासाउंड - बढ़े हुए संकुचित गुर्दे (बड़े वसायुक्त गुर्दे) की कल्पना की जाती है।

निदान (अस्पताल)
स्थिर स्तर पर निदान:
अस्पताल स्तर पर नैदानिक मानदंड
शिकायतें और इतिहास:एम्बुलेटरी स्तर देखें।
शारीरिक जाँच:एम्बुलेटरी स्तर देखें।
प्रयोगशाला अनुसंधान:
| नैदानिक परीक्षण | परिणाम |
|
सीरम इम्यूनोफिक्सेशन प्रकाश श्रृंखला इम्युनोग्लोबुलिन (एएल) (6) के साथ 60% अमाइलॉइडोसिस रोगियों में परीक्षण सकारात्मक है। |
|
|
मूत्र का प्रतिरक्षण एएल अमाइलॉइडोसिस (6) वाले 80% रोगियों में परीक्षण सकारात्मक है। मूत्र में एक प्रकाश श्रृंखला प्रोटीन का पता लगाने से मल्टीपल मायलोमा और एमाइलॉयडोसिस की उपस्थिति का पता चलता है। |
एक मोनोक्लोनल प्रोटीन की उपस्थिति |
|
सीरम मुक्त प्रकाश श्रृंखला इम्युनोग्लोबुलिन परीक्षण एएल अमाइलॉइडोसिस (10) के निदान के लिए इस अपेक्षाकृत नए परीक्षण में बहुत अधिक संवेदनशीलता (>95%) है। इम्युनोग्लोबुलिन लाइट चेन, एए और ट्रान्सथायरेटिन के खिलाफ व्यावसायिक रूप से उपलब्ध एंटीसेरा आमतौर पर उपयोग किया जाता है, लेकिन इसमें पर्याप्त विशिष्टता और संवेदनशीलता नहीं हो सकती है। कई मामलों में, अंतर्निहित अमाइलॉइड प्रकार को निर्धारित करने के लिए मास स्पेक्ट्रोस्कोपी और इम्यूनो-इलेक्ट्रॉन माइक्रोस्कोपी की आवश्यकता होती है। |
असामान्य कप्पा लैम्ब्डा अनुपात |
|
अस्थि मज्जा बायोप्सी अस्थि मज्जा बायोप्सी संदिग्ध प्रकाश श्रृंखला अमाइलॉइडोसिस वाले सभी रोगियों में की जाती है और संदिग्ध अमाइलॉइडोसिस वाले किसी भी रोगी के निदान के लिए ऊतक का एक उत्कृष्ट स्रोत है। |
क्लोनल प्लाज्मा कोशिकाओं की उपस्थिति |
वाद्य अनुसंधान:
पेट के अंगों और गुर्दे का अल्ट्रासाउंड - बढ़े हुए संकुचित गुर्दे (बड़े वसायुक्त गुर्दे) की कल्पना की जाती है।
वृक्क अमाइलॉइडोसिस के लिए नैदानिक एल्गोरिथम
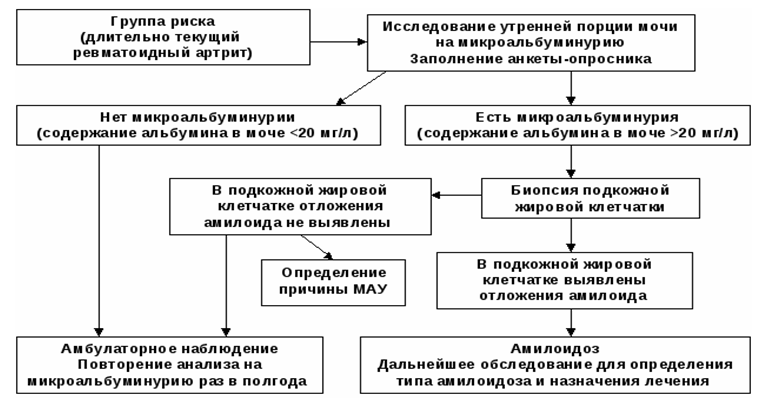
मुख्य नैदानिक उपायों की सूची:
· सामान्य रक्त विश्लेषण;
· सामान्य मूत्र विश्लेषण;
रक्त का जैव रासायनिक विश्लेषण (कुल प्रोटीन, एल्ब्यूमिन, Na, Ca, कोलेस्ट्रॉल, रक्त सीरम में शर्करा);
सीरम इम्यूनोफिक्सेशन;
मूत्र प्रतिरक्षण;
सीरम में मुक्त प्रकाश श्रृंखला इम्युनोग्लोबुलिन की जांच ;
अस्थि मज्जा बायोप्सी।
पेट के अंगों और गुर्दे का अल्ट्रासाउंड।
अतिरिक्त नैदानिक उपायों की सूची
प्रयोगशाला अनुसंधान:
| नैदानिक परीक्षण | परिणाम |
|
ऊतक बायोप्सी: अमाइलॉइडोसिस के निदान के लिए, यह आवश्यक है कि बायोप्सी सामग्री में ऊतकों में जमा कांगो रेड (11) के लिए सकारात्मक दाग हो। जब कांगो सामग्री को ध्रुवीकृत प्रकाश में लाल रंग से रंगा जाता है, तो चमकीले हरे रंग की द्विअर्थीता देखी जा सकती है। बायोप्सी सामग्री होंठ, त्वचा, मसूड़ों, चमड़े के नीचे की वसा, अस्थि मज्जा, नसों, मलाशय, गुर्दे, यकृत या हृदय के म्यूकोसा से प्राप्त की जा सकती है। जमा हमेशा बाह्य रूप से स्थित होते हैं और अनाकार होते हैं। |
सकारात्मक - हरे रंग की बायरफ्रींग जब कांगो लाल के साथ दागी जाती है |
|
अमाइलॉइड जमा का इम्यूनोहिस्टोलॉजिकल अध्ययन: वे आपको प्रणालीगत अमाइलॉइडोसिस के विभिन्न रूपों को पहचानने की अनुमति देते हैं। |
प्रकाश श्रृंखला इम्युनोग्लोबुलिन, एए और ट्रान्सथायरेटिन के खिलाफ एंटीसेरम |
|
मास - स्पेक्ट्रोस्कोपी: अमाइलॉइड प्रोटीन संरचना विश्लेषण प्रदान करता है। यह वर्तमान में अमाइलॉइडोसिस के प्रकार के निदान के लिए स्वर्ण मानक है। |
प्रोटीन के प्रकार की पुष्टि करता है |
|
इम्यूनो-इलेक्ट्रॉन माइक्रोस्कोपी: इलेक्ट्रॉन माइक्रोस्कोप के तहत अमाइलॉइड के सभी रूप रेशेदार, कठोर और अशाखित होते हैं। |
अमाइलॉइड में एक तंतुमय उपस्थिति होती है और ये कठोर और अशाखित होते हैं। |
|
आनुवंशिक परीक्षण: एक मोनोक्लोनल इम्युनोग्लोबुलिन/एमाइलॉयड मुक्त प्रकाश श्रृंखला प्रोटीन पहचान परीक्षण के संदिग्ध परिणामों की उपस्थिति में वंशानुगत अमाइलॉइडोसिस को रद्द करने के लिए आनुवंशिक परीक्षण अनिवार्य है। जीन की प्रत्यक्ष अनुक्रमण द्वारा जांच की जा सकती है और इसमें निम्नलिखित जीन शामिल हैं: TTR, फाइब्रिनोजेन, एपोलिपोप्रोटीन A1, लाइसोजाइम, MEFV (भूमध्यसागरीय बुखार), और ट्यूमर नेक्रोसिस फैक्टर रिसेप्टर 1 (TNFR1 या TNFRSF1A)। MEFV और TNFRSF1A वंशानुगत आवधिक बुखार सिंड्रोम हैं (यानी, AA अमाइलॉइडोसिस के संभावित कारण), और प्रति से वंशानुगत अमाइलॉइड नहीं हैं। |
सकारात्मक |
|
सीरम अमाइलॉइड पी (एसएपी) स्किन्टिग्राफिक स्कैन: हाल के वर्षों में, शरीर में अमाइलॉइड के वितरण का आकलन करने के लिए आयोडीन-लेबल सीरम पी-घटक (एसएपी) स्किन्टिग्राफी का उपयोग नैदानिक अभ्यास में किया जाने लगा है। |
अमाइलॉइड निक्षेपण के स्थलों पर अवशोषण |
|
सामान्य रक्त विश्लेषण: एनीमिया मुख्य रूप से गुर्दे की कमी या जठरांत्र संबंधी मार्ग से रक्तस्राव वाले रोगियों में होता है। थ्रोम्बोसाइटेमिया जिगर की भागीदारी और हाइपरस्प्लेनिज्म से जुड़ा हुआ है। |
आमतौर पर सामान्य |
|
जैव रासायनिक रक्त परीक्षण (यकृत और गुर्दा परीक्षण), चयापचय स्थिति संकेतक): हेपेटिक अमाइलॉइडोसिस को क्षारीय फॉस्फेट के ऊंचे स्तर की विशेषता है। वृक्क अमाइलॉइडोसिस के प्रारंभिक चरण में अधिकांश रोगी क्रिएटिनिन निकासी को बनाए रखते हैं, लेकिन मूत्र में प्रोटीन की कमी (नेफ्रोटिक सिंड्रोम) के कारण हाइपोएल्ब्यूमिनमिया की महत्वपूर्ण डिग्री हो सकती है। |
कम एल्बुमिन; क्षारीय फॉस्फेट में वृद्धि |
|
दैनिक प्रोटीनमेह (24 घंटों में मूत्र संग्रह): एल्ब्यूमिन का उत्सर्जन> 1 ग्राम / दिन अमाइलॉइडोसिस वाले रोगियों में गुर्दे की क्षति (गुर्दे की अमाइलॉइडोसिस) को इंगित करता है। प्रोटीनुरिया> 3 ग्राम / दिन के स्तर पर, नेफ्रोटिक सिंड्रोम विकसित होता है। |
पेशाब में बढ़ा हुआ प्रोटीन |
|
सीरम ट्रोपोनिन स्तर: मायोकार्डियल क्षति का निर्धारण करने के लिए एक संवेदनशील परीक्षण। पता लगाने योग्य ट्रोपोनिन के स्तर वाले मरीजों में इसके बिना (12) की तुलना में खराब पूर्वानुमान होता है। |
ऊपर उठाया हुआ |
|
बी-टाइप नैट्रियूरेटिक पेप्टाइड: रोधगलन और CHF की उपस्थिति के लिए संवेदनशील नैदानिक अध्ययन। यह कार्डियक अमाइलॉइडोसिस (13) की स्थापना में एक महत्वपूर्ण रोगसूचक मूल्य के लिए दिखाया गया है। बी-टाइप नैट्रियूरेटिक पेप्टाइड के स्तर पर > 300 एनजी/एल (> 300 पीजी/एमएल) मायोकार्डियल अमाइलॉइड भागीदारी (10) का सुझाव देता है। रोगियों के साथ<170 нг / л (<170 пг / мл) имеют значительно более длительную выживаемость, чем пациенты с >170 एनजी/ली (>170 पीजी/एमएल)। |
ऊपर उठाया हुआ |
|
बीटा -2 माइक्रोग्लोबुलिन: यह अमाइलॉइडोसिस के रोगियों में जीवित रहने का एक भविष्यवक्ता है। बीटा-2-माइक्रोग्लोबुलिन> 2.7 मिलीग्राम/ली के स्तर पर, पूर्वानुमान प्रतिकूल है (14)। |
ऊपर उठाया हुआ |
वाद्य अनुसंधान:
|
ईसीजी: हृदय की भागीदारी के मूल्यांकन के भाग के रूप में सभी रोगियों में किया जाना चाहिए। |
दिल के चालन विकार |
|
इकोकार्डियोग्राम (इकोसीजी): कार्डियक अमाइलॉइडोसिस वाले रोगियों में दिल की विफलता के नैदानिक लक्षण 22% से 34% (7) तक देखे जाते हैं। इकोकार्डियोग्राफी से कम से कम लक्षणों वाले रोगियों में अमाइलॉइड जमाव की एक उच्च घटना का पता चलता है (लगभग 50% एएल मामलों में हृदय की भागीदारी होती है)। अंतिम चरण में, इजेक्शन अंश में कमी होती है। |
डायस्टोलिक शिथिलता, इंटरवेंट्रिकुलर सेप्टम का मोटा होना, इजेक्शन अंश में कमी |
|
डॉपलर तनाव के साथ प्रतिध्वनित: मायोकार्डियम में अमाइलॉइड घुसपैठ की डिग्री का एक संकेतक। जब धमनी उच्च रक्तचाप या वाल्वुलर हृदय रोग नहीं होता है तो असामान्यताओं का पता लगाने में इसकी उच्च संवेदनशीलता होती है। मायोकार्डियल स्ट्रेच को मायोकार्डियल फाइबर की लंबाई प्रति यूनिट लंबाई में प्रतिशत परिवर्तन के रूप में परिभाषित किया गया है, और दर खिंचाव की अवधि (15-16) पर निर्भर करती है। |
मायोकार्डियम के अनुदैर्ध्य संकुचन और खिंचाव में कमी; वेंट्रिकुलर भरने का प्रतिबंध |
|
दिल का एमआरआई: चुंबकीय अनुनाद रिलैक्सोमेट्री एमआरआई डायग्नोस्टिक्स की विश्वसनीयता में सुधार करती है और हाइपरट्रॉफिक कार्डियोमायोपैथी से कार्डियक अमाइलॉइडोसिस को अलग करने में मदद करती है। |
आयु नियंत्रण की तुलना में T1 और T2 विश्राम समय में काफी वृद्धि हुई है |
क्रमानुसार रोग का निदान
गुर्दे के अमाइलॉइडोसिस का विभेदक निदान
| राज्य | अवकलनीय संकेत/लक्षण | अलग-अलग परीक्षण |
| हाइपरट्रॉफिक कार्डियोमायोपैथी | एचसीएम को कार्डियक अमाइलॉइडोसिस से अलग करना चिकित्सकीय रूप से कठिन है। |
इकोसीजी एचसीएम के लिए एक नैदानिक मानदंड है, जहां इंटरवेंट्रिकुलर सेप्टम के असममित अतिवृद्धि का पता लगाया जाता है; तनाव के साथ डॉपलर प्रतिध्वनि, अमाइलॉइडोसिस के संकेतों को बाहर करने के लिए उपयोग किया जाता है, एमाइलॉयडोसिस में पाए जाने वाले विशिष्ट प्रतिबंधात्मक फिलिंग परिवर्तनों को इंगित नहीं करता है; एमआरआई 2 सिंड्रोम को अलग कर सकता है |
| झिल्लीदार ग्लोमेरुलोपैथी | नेफ्रोटिक सिंड्रोम वाले रोगियों में नैदानिक रूप से समान अभिव्यक्तियाँ। | गुर्दे की बायोप्सी कांगो लाल के साथ दाग नहीं करती है। |
| अज्ञात मूल के मोनोक्लोनल गैमोपैथी (एमजीएनजी) से जुड़े न्यूरोपैथी | मरीजों में प्रोटीनुरिया, हेपेटोमेगाली या कार्डियोमायोपैथी की महत्वपूर्ण डिग्री नहीं होती है। | सुरल तंत्रिका बायोप्सी कांगो लाल के साथ दाग नहीं करता है। |
| एकाधिक मायलोमा | हड्डियों में दर्द, एनीमिया के लक्षण और किडनी फेल होना। |
सादा एक्स-रे लिटिक हड्डी के घावों, संपीड़न फ्रैक्चर, फैलाना ऑस्टियोपोरोसिस दिखाते हैं; कम एचबी; किडनी खराब। |
| गुर्दे का रोग | दैनिक प्रोटीनमेह 3.5 ग्राम / दिन से अधिक, एडिमा, हाइपोएल्ब्यूमिनमिया, डिस्लिपिडेमिया | केपी "नेफ्रोटिक सिंड्रोम" देखें |
चिकित्सा पर्यटन
कोरिया, इज़राइल, जर्मनी, यूएसए में इलाज कराएं
चिकित्सा पर्यटन
चिकित्सा पर्यटन पर सलाह लें
इलाज
ध्यान!
- स्व-औषधि द्वारा, आप अपने स्वास्थ्य को अपूरणीय क्षति पहुंचा सकते हैं।
- MedElement वेबसाइट पर पोस्ट की गई जानकारी व्यक्तिगत चिकित्सा परामर्श को प्रतिस्थापित नहीं कर सकती है और न ही करनी चाहिए। यदि आपको कोई बीमारी या लक्षण हैं जो आपको परेशान करते हैं तो चिकित्सा सुविधाओं से संपर्क करना सुनिश्चित करें।
- किसी विशेषज्ञ के साथ दवाओं की पसंद और उनकी खुराक पर चर्चा की जानी चाहिए। रोग और रोगी के शरीर की स्थिति को ध्यान में रखते हुए केवल एक डॉक्टर ही सही दवा और उसकी खुराक लिख सकता है।
- MedElement वेबसाइट केवल एक सूचना और संदर्भ संसाधन है। इस साइट पर पोस्ट की गई जानकारी का उपयोग डॉक्टर के नुस्खे को मनमाने ढंग से बदलने के लिए नहीं किया जाना चाहिए।
- MedElement के संपादक इस साइट के उपयोग से होने वाले स्वास्थ्य या भौतिक क्षति के किसी भी नुकसान के लिए ज़िम्मेदार नहीं हैं।
- शरीर की एक सामान्य, प्रणालीगत बीमारी, जिसमें अंगों और ऊतकों में बाद के बिगड़ा हुआ कार्य के साथ एक विशिष्ट ग्लाइकोप्रोटीन (एमाइलॉयड) का जमाव होता है। अमाइलॉइडोसिस के साथ, गुर्दे (नेफ्रोटिक सिंड्रोम, एडेमेटस सिंड्रोम), हृदय (दिल की विफलता, अतालता), जठरांत्र संबंधी मार्ग, मस्कुलोस्केलेटल सिस्टम और त्वचा प्रभावित हो सकते हैं। शायद पॉलीसेरोसाइटिस, रक्तस्रावी सिंड्रोम, मानसिक विकारों का विकास। अमाइलॉइडोसिस का विश्वसनीय निदान प्रभावित ऊतकों के बायोप्सी नमूनों में अमाइलॉइड का पता लगाने से सुगम होता है। अमाइलॉइडोसिस के उपचार के लिए, प्रतिरक्षादमनकारी और रोगसूचक चिकित्सा की जाती है; संकेतों के अनुसार - पेरिटोनियल डायलिसिस, किडनी और लीवर प्रत्यारोपण।
आईसीडी -10
ई85

सामान्य जानकारी
अमाइलॉइडोसिस प्रणालीगत डिस्प्रोटीनोज के समूह से एक बीमारी है जो एक जटिल प्रोटीन-पॉलीसेकेराइड यौगिक - अमाइलॉइड के ऊतकों में गठन और संचय के साथ होती है। दुनिया में अमाइलॉइडोसिस की व्यापकता काफी हद तक भौगोलिक रूप से निर्धारित होती है: उदाहरण के लिए, भूमध्यसागरीय बेसिन के देशों में आवधिक बीमारी अधिक आम है; अमाइलॉइड पोलीन्यूरोपैथी - जापान, इटली, स्वीडन, पुर्तगाल आदि में। जनसंख्या में अमाइलॉइडोसिस की औसत आवृत्ति प्रति 50 हजार जनसंख्या पर 1 मामला है। यह रोग आमतौर पर 50-60 वर्ष से अधिक उम्र के लोगों में विकसित होता है। इस तथ्य को देखते हुए कि अमाइलॉइडोसिस में लगभग सभी अंग प्रणालियां प्रभावित होती हैं, रोग का अध्ययन विभिन्न चिकित्सा विषयों द्वारा किया जाता है: रुमेटोलॉजी, यूरोलॉजी, कार्डियोलॉजी, गैस्ट्रोएंटरोलॉजी, न्यूरोलॉजी, आदि।
अमाइलॉइडोसिस के कारण
प्राथमिक अमाइलॉइडोसिस के एटियलजि को पूरी तरह से समझा नहीं गया है। इसी समय, यह ज्ञात है कि माध्यमिक अमाइलॉइडोसिस आमतौर पर पुरानी संक्रामक (तपेदिक, सिफलिस, एक्टिनोमाइकोसिस) और प्युलुलेंट-भड़काऊ रोगों (ऑस्टियोमाइलाइटिस, ब्रोन्किइक्टेसिस, बैक्टीरियल एंडोकार्डिटिस, आदि) से जुड़ा होता है, कम अक्सर ट्यूमर प्रक्रियाओं (लिम्फोग्रानुलोमैटोसिस, ल्यूकेमिया) के साथ। , आंत का कैंसर)। अंग)। प्रतिक्रियाशील अमाइलॉइडोसिस एथेरोस्क्लेरोसिस, सोरायसिस, रुमेटोलॉजी (संधिशोथ, एंकिलॉज़िंग स्पॉन्डिलाइटिस), पुरानी सूजन (अल्सरेटिव कोलाइटिस, क्रोहन रोग), मल्टीसिस्टम घाव (व्हीपल रोग, सारकॉइडोसिस) के रोगियों में विकसित हो सकता है। अमाइलॉइडोसिस के विकास में योगदान करने वाले कारकों में, हाइपरग्लोबुलिनमिया, सेलुलर प्रतिरक्षा के बिगड़ा हुआ कार्य, आनुवंशिक प्रवृत्ति आदि सर्वोपरि हैं।
रोगजनन
अमाइलॉइडोजेनेसिस के कई संस्करणों में, डिस्प्रोटीनोसिस के सिद्धांत, स्थानीय सेलुलर उत्पत्ति, प्रतिरक्षाविज्ञानी और उत्परिवर्तनीय सिद्धांतों के समर्थकों की सबसे बड़ी संख्या है। स्थानीय कोशिकीय उत्पत्ति का सिद्धांत केवल कोशिकीय स्तर पर होने वाली प्रक्रियाओं (मैक्रोफेज प्रणाली द्वारा तंतुमय अमाइलॉइड अग्रदूतों का निर्माण) पर विचार करता है, जबकि अमाइलॉइड का निर्माण और संचय कोशिका के बाहर होता है। इसलिए, स्थानीय सेलुलर उत्पत्ति के सिद्धांत को संपूर्ण नहीं माना जा सकता है।
डिस्प्रोटीनोसिस के सिद्धांत के अनुसार, अमाइलॉइड असामान्य प्रोटीन चयापचय का एक उत्पाद है। अमाइलॉइडोसिस के रोगजनन में मुख्य लिंक - डिस्प्रोटीनेमिया और हाइपरफिब्रिनोजेनमिया प्लाज्मा में मोटे प्रोटीन और पैराप्रोटीन अंशों के संचय में योगदान करते हैं। अमाइलॉइडोसिस की उत्पत्ति का प्रतिरक्षाविज्ञानी सिद्धांत अमाइलॉइड के गठन को एक एंटीजन-एंटीबॉडी प्रतिक्रिया के साथ जोड़ता है, जिसमें विदेशी प्रोटीन या अपने स्वयं के ऊतकों के क्षय उत्पाद एंटीजन के रूप में कार्य करते हैं। इस मामले में, अमाइलॉइड का जमाव मुख्य रूप से एंटीबॉडी के गठन और एंटीजन की अधिकता के स्थानों में होता है। सबसे सार्वभौमिक अमाइलॉइडोसिस का उत्परिवर्तन सिद्धांत है, जो विभिन्न प्रकार के उत्परिवर्तजन कारकों को ध्यान में रखता है जो असामान्य प्रोटीन संश्लेषण का कारण बन सकते हैं।
अमाइलॉइड एक जटिल ग्लाइकोप्रोटीन है जिसमें फाइब्रिलर और गोलाकार प्रोटीन होते हैं जो पॉलीसेकेराइड से निकटता से जुड़े होते हैं। अमाइलॉइड जमा रक्त वाहिकाओं के इंटिमा और एडिटिटिया, पैरेन्काइमल अंगों के स्ट्रोमा, ग्रंथियों की संरचनाओं आदि में जमा होते हैं। मामूली अमाइलॉइड जमा के साथ, केवल सूक्ष्म स्तर पर परिवर्तन का पता लगाया जाता है और कार्यात्मक विकारों का कारण नहीं बनता है। अमाइलॉइड का एक स्पष्ट संचय प्रभावित अंग (मात्रा में वृद्धि, चिकना या मोमी उपस्थिति) में मैक्रोस्कोपिक परिवर्तनों के साथ होता है। अमाइलॉइडोसिस, स्ट्रोमल स्केलेरोसिस और अंगों के पैरेन्काइमा के शोष के परिणामस्वरूप, उनकी नैदानिक रूप से महत्वपूर्ण कार्यात्मक कमी विकसित होती है।
वर्गीकरण
कारणों के अनुसार, प्राथमिक (अज्ञातहेतुक), माध्यमिक (प्रतिक्रियाशील, अधिग्रहित), वंशानुगत (पारिवारिक, आनुवंशिक) और सेनील एमाइलॉयडोसिस प्रतिष्ठित हैं। वंशानुगत अमाइलॉइडोसिस के विभिन्न रूप हैं: भूमध्यसागरीय बुखार, या आवधिक बीमारी (गर्म हमले, पेट में दर्द, कब्ज, दस्त, फुफ्फुस, गठिया, त्वचा पर चकत्ते), पुर्तगाली न्यूरोपैथिक अमाइलॉइडोसिस (परिधीय पोलीन्यूरोपैथी, नपुंसकता, हृदय चालन गड़बड़ी), फिनिश प्रकार ( कॉर्नियल शोष, कपाल न्यूरोपैथी), डेनिश संस्करण (कार्डियोपैथिक अमाइलॉइडोसिस) और कई अन्य। अन्य
अंगों और प्रणालियों को होने वाली प्रमुख क्षति के आधार पर, नेफ्रोपैथिक (गुर्दे का अमाइलॉइडोसिस), कार्डियोपैथिक (हृदय का अमाइलॉइडोसिस), न्यूरोपैथिक (तंत्रिका तंत्र का अमाइलॉइडोसिस), हेपेटोपैथिक (यकृत का अमाइलॉइडोसिस), एपिनेफ्रोपैथिक (अधिवृक्क ग्रंथियों का अमाइलॉइडोसिस) ), APUD-एमाइलॉयडोसिस, त्वचा के अमाइलॉइडोसिस और मिश्रित प्रकार के रोग प्रतिष्ठित हैं। । इसके अलावा, अंतरराष्ट्रीय अभ्यास में यह स्थानीय और सामान्यीकृत (प्रणालीगत) अमाइलॉइडोसिस के बीच अंतर करने के लिए प्रथागत है। स्थानीयकृत रूपों, जो आमतौर पर बुजुर्ग लोगों में विकसित होते हैं, में अल्जाइमर रोग में अमाइलॉइडोसिस, टाइप 2 मधुमेह मेलेटस, अंतःस्रावी ट्यूमर, त्वचा के ट्यूमर, मूत्राशय आदि शामिल हैं। अमाइलॉइड फाइब्रिल की जैव रासायनिक संरचना के आधार पर, एमाइलॉयडोसिस के निम्नलिखित प्रणालीगत रूप प्रतिष्ठित प्रकार हैं। :
- अली- तंतुओं के हिस्से के रूप में, आईजी प्रकाश श्रृंखला (वाल्डेनस्ट्रॉम रोग के साथ, मल्टीपल मायलोमा, घातक लिम्फोमा);
- आ- फाइब्रिल के हिस्से के रूप में, तीव्र-चरण सीरम α-globulin, सी-रिएक्टिव प्रोटीन (ट्यूमर और आमवाती रोगों, आवधिक बीमारी, आदि के लिए) की विशेषताओं के समान;
- Aβ2M- फाइब्रिल -2-माइक्रोग्लोबुलिन के हिस्से के रूप में (हेमोडायलिसिस पर रोगियों में पुरानी गुर्दे की विफलता में);
- एटीटीआर- तंतुओं की संरचना में, परिवहन प्रोटीन ट्रान्सथायरेटिन (पारिवारिक वंशानुगत और अमाइलॉइडोसिस के वृद्ध रूपों में)।
अमाइलॉइडोसिस के लक्षण
अमाइलॉइडोसिस की नैदानिक अभिव्यक्तियाँ विविध हैं और अमाइलॉइड जमा की गंभीरता और स्थानीयकरण, अमाइलॉइड की जैव रासायनिक संरचना, रोग का "अनुभव" और अंग की शिथिलता की डिग्री पर निर्भर करती हैं। अमाइलॉइडोसिस के अव्यक्त चरण में, जब अमाइलॉइड जमा का केवल सूक्ष्म रूप से पता लगाया जा सकता है, तो कोई लक्षण नहीं होते हैं। जैसे-जैसे एक या दूसरे अंग की कार्यात्मक अपर्याप्तता विकसित होती है और आगे बढ़ती है, रोग के नैदानिक लक्षण बढ़ जाते हैं।
गुर्दे के अमाइलॉइडोसिस के साथ, मध्यम प्रोटीनमेह के दीर्घकालिक वर्तमान चरण को नेफ्रोटिक सिंड्रोम के विकास से बदल दिया जाता है। उन्नत चरण में संक्रमण एक अंतःक्रियात्मक संक्रमण, टीकाकरण, हाइपोथर्मिया, अंतर्निहित बीमारी के तेज होने से जुड़ा हो सकता है। एडिमा धीरे-धीरे बढ़ती है (पहले पैरों पर, और फिर पूरे शरीर पर), नेफ्रोजेनिक धमनी उच्च रक्तचाप और गुर्दे की विफलता विकसित होती है। गुर्दे की शिरा घनास्त्रता हो सकती है। बड़े पैमाने पर प्रोटीन की हानि हाइपोप्रोटीनेमिया, हाइपरफिब्रिनोजेनमिया, हाइपरलिपिडिमिया और एज़ोटेमिया के साथ होती है। मूत्र में सूक्ष्म, कभी-कभी मैक्रोहेमेटुरिया, ल्यूकोसाइटुरिया पाए जाते हैं। सामान्य तौर पर, गुर्दे के एमिलॉयडोसिस के दौरान, एक प्रारंभिक गैर-एडेमेटस चरण, एक एडेमेटस चरण, और एक यूरीमिक (कैशेक्टिक) चरण प्रतिष्ठित होते हैं।
हृदय की अमाइलॉइडोसिस विशिष्ट नैदानिक संकेतों के साथ प्रतिबंधात्मक कार्डियोमायोपैथी के प्रकार के अनुसार आगे बढ़ती है - कार्डियोमेगाली, अतालता, प्रगतिशील हृदय विफलता। मरीजों को सांस की तकलीफ, सूजन, कमजोरी की शिकायत होती है जो मामूली शारीरिक परिश्रम के साथ होती है। कम अक्सर, दिल के अमाइलॉइडोसिस के साथ, पॉलीसेरोसाइटिस विकसित होता है (जलोदर, एक्सयूडेटिव फुफ्फुस और पेरिकार्डिटिस)।
अमाइलॉइडोसिस में जठरांत्र संबंधी मार्ग की हार जीभ (मैक्रोग्लासिया), अन्नप्रणाली (कठोरता और बिगड़ा हुआ क्रमाकुंचन), पेट (नाराज़गी, मतली), आंतों (कब्ज, दस्त, malabsorption सिंड्रोम, आंतों की रुकावट) की अमाइलॉइड घुसपैठ की विशेषता है। गैस्ट्रोइंटेस्टाइनल रक्तस्राव विभिन्न स्तरों पर हो सकता है। जिगर के अमाइलॉइड घुसपैठ के साथ, हेपेटोमेगाली, कोलेस्टेसिस और पोर्टल उच्च रक्तचाप विकसित होते हैं। अमाइलॉइडोसिस में अग्नाशय की भागीदारी आमतौर पर पुरानी अग्नाशयशोथ के रूप में सामने आती है।
त्वचा का अमाइलॉइडोसिस चेहरे, गर्दन, त्वचा की प्राकृतिक सिलवटों में कई मोमी सजीले टुकड़े (पपल्स, नोड्यूल) की उपस्थिति के साथ होता है। बाह्य रूप से, त्वचा के घाव स्क्लेरोडर्मा, न्यूरोडर्माेटाइटिस या लाइकेन प्लेनस के सदृश हो सकते हैं। मस्कुलोस्केलेटल सिस्टम के अमाइलॉइड घावों के लिए, सममित पॉलीआर्थराइटिस, कार्पल टनल सिंड्रोम, ह्यूमेरोस्कैपुलर पेरिआर्थराइटिस और मायोपैथी का विकास विशिष्ट है। तंत्रिका तंत्र की भागीदारी के साथ होने वाले अमाइलॉइडोसिस के अलग-अलग रूप, पोलीन्यूरोपैथी, निचले छोरों के पक्षाघात, सिरदर्द, चक्कर आना, ऑर्थोस्टेटिक हाइपोटेंशन, पसीना, मनोभ्रंश आदि के साथ हो सकते हैं।
निदान
विभिन्न चिकित्सक अमाइलॉइडोसिस के नैदानिक अभिव्यक्तियों का सामना कर सकते हैं: रुमेटोलॉजिस्ट, मूत्र रोग विशेषज्ञ, हृदय रोग विशेषज्ञ, गैस्ट्रोएंटेरोलॉजिस्ट, न्यूरोलॉजिस्ट, त्वचा विशेषज्ञ, चिकित्सक, आदि। नैदानिक और anamnestic संकेतों का एक व्यापक मूल्यांकन, एक व्यापक प्रयोगशाला और वाद्य परीक्षा सही निदान के लिए सबसे महत्वपूर्ण हैं।
अमाइलॉइडोसिस एक प्रणालीगत बीमारी है, जब प्रोटीन चयापचय में गड़बड़ी होती है, तो प्रतिरक्षा प्रणाली काम करना बंद कर देती है। इस संबंध में, अमाइलॉइड बनता है - एक प्रोटीन-सैकराइड कॉम्प्लेक्स जो मानव अंगों के सभी ऊतकों में जमा होता है।
समय के साथ, अमाइलॉइड सामान्य कोशिकाओं को बाहर निकालते हुए, अंगों पर अधिक से अधिक हमला करता है। नतीजतन, अंग अपनी कार्यक्षमता खो देता है, अपरिवर्तनीय परिवर्तन देखे जाते हैं। यदि लंबे समय तक बीमारी का इलाज नहीं किया जाता है, तो कई अंगों के कार्य बाधित हो जाते हैं, जिससे मृत्यु हो जाती है।
डब्ल्यूएचओ के शोध के अनुसार, दुनिया के लगभग 1% निवासियों में अमाइलॉइडोसिस का निदान किया जाता है। सबसे आम माध्यमिक अमाइलॉइडोसिस है। आनुवंशिक अमाइलॉइडोसिस का अक्सर यहूदी, अर्मेनियाई राष्ट्रीयता से संबंधित लोगों के साथ-साथ भूमध्यसागरीय बेसिन के देशों के निवासियों में निदान किया जाता है।
पुरुषों में घटना दर महिलाओं की तुलना में दोगुनी है। अमाइलॉइडोसिस के सभी रूपों में, नेफ्रोपैथिक (गुर्दे की क्षति) और सामान्यीकृत (सभी ऊतकों और अंगों को नुकसान) एमाइलॉयडोसिस का निदान किया जाता है।
अमाइलॉइडोसिस के प्रकार, विकास के कारण
अमाइलॉइडोसिस के कारण के आधार पर, ऐसे रोग हैं जो स्वतंत्र रूप से या अन्य प्रणालियों और अंगों में विकृति के कारण विकसित हो सकते हैं। निम्न प्रकार के अमाइलॉइडोसिस होते हैं: सेनील, ट्यूमर के साथ, प्राथमिक या अज्ञातहेतुक अमाइलॉइडोसिस, वंशानुगत, माध्यमिक या प्रतिक्रियाशील, साथ ही हेमोडायलिसिस से गुजरने वाले रोगियों में। प्रजातियों के आधार पर, अमाइलॉइडोसिस का विकास अलग तरह से होता है, लक्षण और रोग का निदान भिन्न होता है। अमाइलॉइडोसिस के प्रकार और चरणों के बारे में नीचे विस्तार से चर्चा की जाएगी।
प्राथमिक (अज्ञातहेतुक)
ज्यादातर मामलों में प्राथमिक अमाइलॉइडोसिस बिना किसी कारण के शुरू होता है। रोग के इस रूप के साथ, अमाइलॉइड ऊतकों और अंगों में जमा हो जाता है, और प्रतिरक्षा प्रणाली की कोशिकाओं का एक उत्परिवर्तन देखा जाता है। इस प्रक्रिया में बनने वाला AL-amyloid मांसपेशियों, त्वचा, हृदय प्रणाली और तंत्रिकाओं में जमा हो जाता है। इसके अलावा, AL-amyloid ट्यूमर मायलोमा की पृष्ठभूमि के खिलाफ बनता है, जब प्लाज्मा कोशिकाएं बड़ी मात्रा में ग्लोब्युलिन का स्राव करना शुरू करती हैं। प्लाज्मा न्यूक्लियोप्रोटीन के लिए बाध्य होने के बाद, असामान्य ग्लोब्युलिन अमाइलॉइड में परिवर्तित हो जाते हैं।
माध्यमिक (प्रतिक्रियाशील)
माध्यमिक अमाइलॉइडोसिस समय के साथ प्रगतिशील भड़काऊ प्रक्रियाओं की पृष्ठभूमि के खिलाफ विकसित होता है। इस मामले में, अन्य बीमारियों की जटिलता के रूप में एए-एमिलॉयड बनता है। माध्यमिक अमाइलॉइडोसिस के कारण हैं:
- जीर्ण संक्रमण - कुष्ठ, मलेरिया, तपेदिक, उपदंश, पायलोनेफ्राइटिस, ब्रोन्किइक्टेसिस।
- पुरुलेंट पुरानी बीमारियां - लंबे समय तक घावों का दबना, ऑस्टियोमाइलाइटिस।
- ट्यूमर - ल्यूकेमिया, लिम्फोग्रानुलोमैटोसिस, आदि।
- गैर-विशिष्ट अल्सरेटिव कोलाइटिस (बड़ी आंत की सूजन) की उपस्थिति।
- रुमेटोलॉजिकल रोग - एंकिलोसिंग स्पॉन्डिलाइटिस, रुमेटीइड गठिया, आदि।
माध्यमिक अमाइलॉइडोसिस शरीर के किसी भी अंग, ऊतक को प्रभावित कर सकता है। रोग की तस्वीर की अभिव्यक्ति तुरंत ध्यान देने योग्य नहीं है। अंतर्निहित बीमारी की शुरुआत के वर्षों बाद, कोई भी उस अंग के कार्यों के उल्लंघन को देख सकता है जहां एमिलॉयड सबसे अधिक जमा किया गया था। अधिक बार, इस विकार से यकृत, गुर्दे, प्लीहा और लिम्फ नोड्स प्रभावित होते हैं। समय के साथ, अन्य अंग भी प्रभावित होते हैं, जिससे कई अंग विफल हो जाते हैं और मृत्यु हो जाती है।
वंशानुगत अमाइलॉइडोसिस
अमाइलॉइडोसिस का वंशानुगत रूप प्रतिरक्षा प्रणाली की कोशिकाओं में उत्परिवर्तित जीन की उपस्थिति के कारण होता है। ये अनुवांशिक उत्परिवर्तन पीढ़ियों के माध्यम से पारित हो जाते हैं, जिसके परिणामस्वरूप एमिलॉयडोब्लास्ट बनते हैं। वंशानुगत रूप किसी विशेष क्षेत्र या किसी विशेष जातीय समूह से संबंधित लोगों को प्रभावित करता है। वंशानुगत अमाइलॉइडोसिस को प्रकारों में विभाजित किया गया है:
- कार्डियोपैथिक। ज्यादातर डेनमार्क के निवासियों में निदान किया जाता है। रोग की नैदानिक तस्वीर सामान्यीकृत प्रकार के प्राथमिक अमाइलॉइडोसिस जैसा दिखता है।
- न्यूरोपैथिक। यह तंत्रिका ऊतक को नुकसान की विशेषता है। घाव के स्थानीयकरण के आधार पर, पुर्तगाली (पैरों की नसें), अमेरिकी (हाथों की नसें), फिनिश (तंत्रिका तंत्र, आंखों के कॉर्निया, गुर्दे) एमाइलॉयडोसिस हैं।
- पारिवारिक नेफ्रोपैथिक। एक अन्य नाम अंग्रेजी अमाइलॉइडोसिस (मकल एंड वेल्स रोग) है। नैदानिक तस्वीर पित्ती, बुखार के लक्षण, बहरापन है।
- आवधिक (पारिवारिक भूमध्य बुखार)। यह रोग यहूदियों, अरबों, अर्मेनियाई लोगों में अधिक आम है। अभिव्यक्तियाँ - 39ºС से ऊपर का तापमान, सिर और मांसपेशियों में दर्द, अत्यधिक पसीना आना। फेफड़े, पेरिटोनियल अंगों, श्लेष की झिल्लियों की सूजन होती है। मानस में बार-बार विचलन।
बूढ़ा अमाइलॉइडोसिस
80 वर्ष की आयु तक पहुंचने वाले लोगों में, अमाइलॉइड स्थानीय रूप से विभिन्न ऊतकों और अंगों में जमा हो जाता है। यह रोग अन्य उम्र से संबंधित बीमारियों से जुड़ा हुआ है। बूढ़ा अमाइलॉइडोसिस दो प्रकार का होता है:
- सेरेब्रल या सेरेब्रल। यह अल्जाइमर रोग की पृष्ठभूमि के खिलाफ विकसित होता है। अमाइलॉइड एब मस्तिष्क के ऊतकों में जमा होता है।
- सौहार्दपूर्ण। यह हृदय के निलय को प्रभावित कर सकता है (जब उत्परिवर्तित रक्त प्रोटीन ट्रान्सथायरेटिन से अमाइलॉइड बनता है) और अटरिया (जब अमाइलॉइड हृदय कोशिकाओं द्वारा स्रावित नैट्रियूरेटिक पेप्टाइड से बनता है)। दोनों ही मामलों में, अमाइलॉइड फेफड़े, अग्न्याशय और प्लीहा के ऊतकों में पाए जाते हैं।
ट्यूमर के लिए
कुछ प्रकार के ट्यूमर रोगग्रस्त अंग की कोशिकाओं के घातक परिवर्तन को प्रभावित करते हैं, जिसके परिणामस्वरूप फाइब्रिलर प्रोटीन का उत्पादन होता है। इस मामले में, ट्यूमर से प्रभावित अंग के ऊतक में स्थानीय रूप से अमाइलॉइडोसिस विकसित होता है। कारण जो ट्यूमर में अमाइलॉइडोसिस को भड़काते हैं:
- थायरॉयड ग्रंथि का मेडुलरी ट्यूमर। कैंसर थायरॉयड ग्रंथि की सी-कोशिकाओं से विकसित होता है, जो आमतौर पर कैल्सीटोसिन के उत्पादन के लिए जिम्मेदार होते हैं। जब कैल्सीटोसिन का संश्लेषण बिगड़ा होता है, तो इसके टुकड़े अमाइलॉइड एई का हिस्सा बन जाते हैं।
- थायराइड आइलेट्स का कैंसर। आइलेट्स हार्मोन के उत्पादन के लिए जिम्मेदार कोशिकाओं के संचय हैं - ग्लूकागन, इंसुलिन, सोमैटोस्टैटिन, आदि। कोशिकाओं के घातक अध: पतन से फाइब्रिलर प्रोटीन की रिहाई होती है, जो बाद में अमाइलॉइड में पतित हो जाती है।
हेमोडायलिसिस में अमाइलॉइडोसिस
 हेमोडायलिसिस को उन रोगियों के लिए जीवन रक्षक प्रक्रिया कहा जाता है जिनके गुर्दे विषाक्त पदार्थों, चयापचय उप-उत्पादों के रक्त को साफ करने में सक्षम नहीं हैं। गुर्दे की विफलता (तीव्र, पुरानी) से निदान लोगों को हेमोडायलिसिस असाइन करें।
हेमोडायलिसिस को उन रोगियों के लिए जीवन रक्षक प्रक्रिया कहा जाता है जिनके गुर्दे विषाक्त पदार्थों, चयापचय उप-उत्पादों के रक्त को साफ करने में सक्षम नहीं हैं। गुर्दे की विफलता (तीव्र, पुरानी) से निदान लोगों को हेमोडायलिसिस असाइन करें।
प्रक्रिया का सार एक उपकरण के माध्यम से रक्त का मार्ग है जो इससे हानिकारक पदार्थों को निकालता है, रोगी के शरीर में शुद्ध रक्त की वापसी।
डायलिसिस के दौरान, बी 2-माइक्रोग्लोब्युलिन शरीर से उत्सर्जित नहीं किया जा सकता है, और यदि रोगी को लंबे समय तक हेमोडायलिसिस से गुजरना पड़ता है, तो प्रोटीन अत्यधिक मात्रा में शरीर में जमा हो जाता है। यह प्लाज्मा न्यूक्लियोप्रोटीन से बांधता है, विभिन्न अंगों में बसता है, और अमाइलॉइड का आधार बन जाता है।
अमाइलॉइडोसिस के लक्षण
यह देखते हुए कि रोग किसी भी अंग या ऊतक में फैल सकता है, लक्षण अलग-अलग होंगे। पाठ्यक्रम की शुरुआत में रोग के विभिन्न रूपों को मानव शरीर में एक अंग की क्षति और शिथिलता की विशेषता है।
समय के साथ, रोग (यदि यह स्थानीय अमाइलॉइडोसिस नहीं है) बढ़ता है, अन्य अंगों और ऊतकों को प्रभावित करता है। अमाइलॉइडोसिस की अभिव्यक्तियाँ गुर्दे, यकृत, हृदय और अधिवृक्क ग्रंथियों, प्लीहा, जठरांत्र संबंधी मार्ग और तंत्रिका तंत्र, जोड़ों, मांसपेशियों और त्वचा में देखी जा सकती हैं। रोग के प्रकारों का नीचे विस्तार से वर्णन किया गया है।
गुर्दे खराब
अन्य अंगों को नुकसान की तुलना में गुर्दे की अमाइलॉइडोसिस को सबसे खतरनाक बीमारी माना जाता है। गुर्दे की अमाइलॉइडोसिस की नैदानिक तस्वीर चरण पर निर्भर करती है। कुल मिलाकर, उनमें से 4 हैं - अव्यक्त, नेफ्रोटिक, एज़ोटेमिक, प्रोटीन्यूरिक।
अव्यक्त अवस्था में, गुर्दा अमाइलॉइडोसिस व्यावहारिक रूप से लक्षण नहीं दिखाता है। यदि यह एक द्वितीयक रूप है, तो रोगी को अंतर्निहित बीमारी के लक्षण महसूस होते हैं। केवल वर्षों बाद, गुर्दा की क्षति रोगसूचक रूप से प्रकट होगी।
प्रोटीन्यूरिक अवस्था में, गुर्दे का अमाइलॉइडोसिस 10 साल या उससे अधिक समय तक रहता है। इस समय, अमाइलॉइडोसिस धीरे-धीरे वाहिकाओं, अंतरकोशिकीय स्थान और गुर्दे के ग्लोमेरुली में जमा हो जाता है। इस वजह से, मूत्र निर्माण प्रदान करने वाले नेफ्रॉन संकुचित, शोष और मर जाते हैं। गुर्दा फिल्टर की अखंडता, जो आम तौर पर बड़े आणविक प्रोटीन और रक्त कोशिकाओं के माध्यम से नहीं जाने देती है, टूट जाती है। इसके बाद, मूत्र में प्रोटीन उत्सर्जित होते हैं। इस स्तर पर, गुर्दे के अमाइलॉइडोसिस पर संदेह करना मुश्किल है, क्योंकि उत्सर्जन समारोह बिगड़ा नहीं है। आप प्रयोगशाला परीक्षणों के परिणामों में समस्या का पता लगा सकते हैं।
नेफ्रोटिक चरण में वृक्क अमाइलॉइडोसिस वृक्क फिल्टर के और विनाश से प्रकट होता है। इस वजह से, मूत्र में बड़ी मात्रा में प्रोटीन खो जाता है, रक्त में इसकी एकाग्रता कम हो जाती है। प्रोटीन वाहिकाओं में रक्त रखने की प्रक्रिया का हिस्सा हैं। प्रोटीन की एकाग्रता में कमी के साथ, तरल ऊतकों में प्रवेश करता है, सूजन दिन के किसी भी समय होती है, शरीर की स्थिति की परवाह किए बिना। इसके अलावा, गुर्दे की अमाइलॉइडोसिस की प्रगति होती है, एडिमा दृढ़ता से स्पष्ट होती है। पेरिटोनियम, फुफ्फुस गुहा, हृदय थैली में द्रव जमा होता है। यह अवस्था 4-6 वर्ष तक रहती है।
एज़ोटेमिक अवस्था में, वृक्क ऊतक की संपूर्ण मात्रा का केवल 25% कार्य करता है। हानिकारक विषाक्त पदार्थों, यूरिया को हटाने के लिए यह पर्याप्त नहीं है, और इसलिए उनकी एकाग्रता बढ़ रही है। गुर्दे की विफलता की नैदानिक तस्वीर निम्नलिखित में प्रकट होती है:
- बिगड़ा हुआ पेशाब। प्रति दिन निर्धारित 800 मिलीलीटर के बजाय, रोगी 50 मिलीलीटर से कम मूत्र उत्सर्जित करता है;
- स्वास्थ्य बिगड़ता है, कमजोरी, थकान दिखाई देती है;
- पाचन परेशान है, भूख गायब हो जाती है, मतली और उल्टी होती है, शुष्क मुंह एक अप्रिय गंध के साथ होता है;
- त्वचा पीली, शुष्क, लगातार खुजलीदार हो जाती है;
- हृदय प्रणाली ग्रस्त है, जो अतालता का कारण बनती है, रक्तचाप बढ़ जाता है, हृदय की मांसपेशियों में वृद्धि संभव है;
- मस्तिष्क, यूरिक एसिड की उच्च सांद्रता के प्रभाव में, क्षतिग्रस्त हो जाता है, अनिद्रा और स्मृति हानि, चिड़चिड़ापन और मानसिक क्षमताओं में कमी दिखाई देती है;
- हीमोग्लोबिन और लाल रक्त कोशिकाओं में कमी से एनीमिया होता है।
यकृत को होने वाले नुकसान
प्रणालीगत अमाइलॉइडोसिस अक्सर जिगर की क्षति से प्रकट होता है। अमाइलॉइड जमा पित्त नलिकाओं, रक्त वाहिकाओं और यकृत कोशिकाओं पर दबाव डालते हैं, जिसके परिणामस्वरूप बिगड़ा हुआ अंग कार्य होता है। अमाइलॉइडोसिस के सिंड्रोम पर प्रकाश डालते हुए, यकृत में वृद्धि का संकेत मिलता है, जो तालु पर महसूस होता है।
लीवर की सतह चिकनी रहती है, दर्द नहीं होता है। रोग के लंबे पाठ्यक्रम के मामले में, जिगर की विफलता शायद ही कभी विकसित होती है, जो अंग की पुनर्योजी क्षमताओं से जुड़ी होती है।
हेपेटिक अमाइलॉइडोसिस लक्षणों के साथ प्रकट होता है:
- जिगर का बढ़ना।
- पोर्टल हायपरटेंशन। आम तौर पर, आंतरिक अंगों से रक्त यकृत में प्रवेश करता है, जहां इसे साफ किया जाता है और फिर रक्त प्रवाह में वापस आ जाता है। अमाइलॉइड के साथ यकृत के जहाजों को निचोड़ते समय, आंतरिक अंगों की नसों में दबाव बढ़ जाता है। नतीजतन, पैरों में सूजन, रक्त के साथ दस्त, जठरांत्र संबंधी मार्ग में रक्तस्राव होता है।
- पीलिया दुर्लभ है, केवल अमाइलॉइड जमा द्वारा पित्त नलिकाओं के संपीड़न के मामले में। यही कारण है कि पीलिया के साथ खुजली होगी।
दिल की धड़कन रुकना
हृदय का अमाइलॉइडोसिस प्राथमिक और वंशानुगत प्रकृति के अन्य रूपों में विकसित होता है। मायोकार्डियम और हृदय की झिल्लियों में अमाइलॉइड जमा होने के परिणामस्वरूप, रक्त परिसंचरण गड़बड़ा जाता है, मांसपेशियों की कोशिकाएं मर जाती हैं।
रोग के लक्षण:
- अतालता;
- प्रतिबंधात्मक कार्डियोमायोपैथी;
- दिल की धड़कन रुकना।
अतालता हृदय की मांसपेशियों में अमाइलॉइड जमा की पृष्ठभूमि के खिलाफ होती है, जो तंत्रिका आवेग के प्रवाहकत्त्व को बाधित करती है। नतीजतन, हृदय के कक्ष असमान रूप से सिकुड़ते हैं, एक अतालता प्रकट होती है। रोगी को चक्कर आता है, बेहोशी होती है। मस्तिष्क को खराब रक्त की आपूर्ति के कारण, घातक परिणाम संभव है।
मायोकार्डियम में अमाइलॉइड जमा की पृष्ठभूमि के खिलाफ प्रतिबंधात्मक कार्डियोमायोपैथी होती है। नतीजतन, हृदय की मांसपेशी मोटी हो जाती है, कम एक्स्टेंसिबल हो जाती है, जिससे हृदय कक्षों का खराब कामकाज होता है। रोग की नैदानिक तस्वीर थकान, सांस की तकलीफ, क्षैतिज स्थिति से ऊर्ध्वाधर स्थिति में बदलते समय रक्तचाप में तेज कमी है।
हृदय गति रुकने से शरीर में रक्त संचार गड़बड़ा जाता है। यह सूजन, सांस की तकलीफ से प्रकट होता है। अमाइलॉइडोसिस में दिल की विफलता हृदय रोग के लिए मानक उपचार के लिए उत्तरदायी नहीं है। रोग तेजी से बढ़ता है, जिससे कुछ महीनों में मृत्यु हो जाती है।
अधिवृक्क ग्रंथियों और प्लीहा को नुकसान
 अधिवृक्क ग्रंथियां प्रत्येक गुर्दे पर स्थित ग्रंथियां होती हैं और हार्मोन स्रावित करने के लिए जिम्मेदार होती हैं। अमाइलॉइडोसिस हार्मोन संश्लेषण को रोककर अंग के कार्य को बाधित करता है। यदि प्लीहा में अमाइलॉइड जमा हो जाता है, तो अंग आकार में बढ़ जाता है, जो तालु पर ध्यान देने योग्य होता है।
अधिवृक्क ग्रंथियां प्रत्येक गुर्दे पर स्थित ग्रंथियां होती हैं और हार्मोन स्रावित करने के लिए जिम्मेदार होती हैं। अमाइलॉइडोसिस हार्मोन संश्लेषण को रोककर अंग के कार्य को बाधित करता है। यदि प्लीहा में अमाइलॉइड जमा हो जाता है, तो अंग आकार में बढ़ जाता है, जो तालु पर ध्यान देने योग्य होता है।
आम तौर पर, प्लीहा रक्तप्रवाह से विकृत कोशिकाओं को हटा देता है जो इसकी संरचना में फंस जाते हैं। प्लीहा में अमाइलॉइड जमा होने से स्वस्थ लाल रक्त कोशिकाएं, प्लेटलेट्स और सफेद रक्त कोशिकाएं फंस जाती हैं।
नतीजतन, एनीमिया (सामान्य कमजोरी, त्वचा का पीलापन, सांस की तकलीफ), थ्रोम्बोसाइटोपेनिया (नाक से खून बहना, त्वचा से रक्तस्राव), ल्यूकोपेनिया (संक्रमण के लिए संवेदनशीलता) विकसित होता है।
गैस्ट्रोइंटेस्टाइनल घाव
आंतों के अमाइलॉइडोसिस को सामान्यीकृत किया जा सकता है, जब पोषक तत्वों का अवशोषण बिगड़ा होता है, और स्थानीय, जब अमाइलॉइड का संचय एक ट्यूमर की नकल करता है। पहले मामले में दस्त, वजन कम होना, कमजोरी, मानसिक विकार, एनीमिया जैसे लक्षण दिखाई देते हैं। दूसरे मामले में, रोग कब्ज, पेट दर्द, सूजन की विशेषता है।
जोड़ और मांसपेशियों को नुकसान
अमाइलॉइड सबसे पहले पैरों, हाथों पर छोटे जोड़ों को प्रभावित करता है, जैसे-जैसे रोग बढ़ता है, यह कोहनी और घुटनों में बस जाता है। इस रोग में चलने के दौरान दर्द, ऊतक की सूजन और त्वचा का लाल होना, प्रभावित क्षेत्र में बुखार, जोड़ का खराब होना आदि लक्षणों की विशेषता है।
मांसपेशियों की संरचना को प्रभावित किए बिना और प्रकट हुए बिना, अमाइलॉइड लंबे समय तक संयोजी ऊतक में अगोचर रूप से जमा रहता है। समय के साथ, मांसपेशियों के ऊतकों की कोशिकाएं संकुचित हो जाती हैं, उन्हें रक्त की आपूर्ति बाधित हो जाती है, और वे मर जाते हैं। रोग की विशेषता मांसपेशियों में कमजोरी, दर्द, सख्त होना और मांसपेशी अतिवृद्धि है।
अमाइलॉइडोसिस का निदान
अमाइलॉइडोसिस जैसे निदान पर विभिन्न विशेषज्ञता के डॉक्टरों द्वारा संदेह किया जा सकता है - रुमेटोलॉजिस्ट, हृदय रोग विशेषज्ञ और मूत्र रोग विशेषज्ञ, न्यूरोलॉजिस्ट, त्वचा विशेषज्ञ, आदि। इसलिए, अमाइलॉइडोसिस का निदान इतिहास, नैदानिक संकेतों, प्रयोगशाला और वाद्य परीक्षा के व्यापक मूल्यांकन पर आधारित होना चाहिए। . अंगों की स्थिति की जांच करने के लिए, एक ईसीजी, अन्नप्रणाली का एक्स-रे, एंडोस्कोपी, सिग्मोइडोस्कोपी निर्धारित किया जाता है। यदि गुर्दे के अमाइलॉइडोसिस का संदेह है, तो निदान में आवश्यक रूप से उदर गुहा का अल्ट्रासाउंड शामिल है।
अमाइलॉइडोसिस उपचार
इस तथ्य के बावजूद कि विभिन्न गंभीर बीमारियां हैं, अमाइलॉइडोसिस रोग एक खराब रोग का निदान करता है। तथ्य यह है कि प्रारंभिक अवस्था में रोग की पहचान करना संभव नहीं है, और रोग की शुरुआत के कई वर्षों बाद इसकी नैदानिक अभिव्यक्तियाँ ध्यान देने योग्य हैं। गुर्दे के अमाइलॉइडोसिस के रूप में इस तरह के निदान के साथ, उपचार केवल सहायक होता है, क्योंकि चिकित्सीय उपाय प्रभावी नहीं होते हैं।
रोग की उपस्थिति के पहले संदेह में, जननांग प्रणाली की जांच के लिए नेफ्रोलॉजी में अस्पताल में भर्ती होना आवश्यक है, क्योंकि गुर्दे की क्षति को सबसे खतरनाक अभिव्यक्ति माना जाता है। अन्य अंगों को नुकसान की उपस्थिति की जांच करने के लिए अन्य विशेषज्ञ भी शामिल हैं।
यदि निदान ने महत्वपूर्ण अंगों के कामकाज में गंभीर उल्लंघन प्रकट नहीं किया है, तो एमिलॉयडोसिस का उपचार घर पर किया जा सकता है, जहां रोगी को डॉक्टर के सभी नुस्खे का सख्ती से पालन करना चाहिए। उपचार में दवा, आहार, डायलिसिस और अंग प्रत्यारोपण शामिल हो सकते हैं।
"एमाइलॉयडोसिस" एक ऐसा शब्द है जो रोगों के एक समूह को एकजुट करता है जो विभिन्न प्रकार की नैदानिक अभिव्यक्तियों द्वारा प्रतिष्ठित होते हैं और अंगों और ऊतकों में अघुलनशील पैथोलॉजिकल फाइब्रिलर प्रोटीन के बाह्य कोशिकीय जमाव की विशेषता होती है। इस विकृति का पहली बार 17 वीं शताब्दी में वर्णन किया गया था। बोनट - लीवर फोड़ा वाले रोगी में साबूदाना प्लीहा। XIX सदी के मध्य में। विरचो ने शव परीक्षा में यकृत में पाए जाने वाले बाह्य पदार्थ का वर्णन करने के लिए वनस्पति शब्द "एमिलॉयड" (ग्रीक एमिलॉन, स्टार्च से) का इस्तेमाल किया, क्योंकि उनका मानना था कि यह संरचना में स्टार्च के समान था। इसके बाद, जमा की प्रोटीन प्रकृति स्थापित की गई थी, लेकिन "एमिलॉयड" शब्द को आज तक संरक्षित किया गया है।
20 के दशक में। 20 वीं शताब्दी में, बेनहोल्ड ने कांगो लाल के साथ अमाइलॉइड को दागने का प्रस्ताव रखा, फिर ध्रुवीकृत प्रकाश में दोहरे अपवर्तन के प्रभाव की खोज की गई - ईंट लाल से सेब के हरे रंग में परिवर्तन। 1959 में, कोहेन और कल्किंस ने इलेक्ट्रॉन माइक्रोस्कोपी का उपयोग करके अमाइलॉइड की तंतुमय संरचना की स्थापना की।
अमाइलॉइडोसिस की नैदानिक अवधारणाओं का भी विकास हुआ है: रोकिटांस्की ने 1842 में "वसामय रोग" और तपेदिक, उपदंश और रिकेट्सियोसिस के बीच एक संबंध स्थापित किया; विल्क्स ने 1856 में एक रोगी में "वसा अंगों" का वर्णन किया, जिसे कोई सहवर्ती रोग नहीं था; 1937 में एटकिंसन ने मल्टीपल मायलोमा रोगियों में अमाइलॉइडोसिस की खोज की। बीमारी के सेनील (सोइका, 1876) और वंशानुगत (एंड्रेड, 1952) रूपों की पहचान की गई, अमाइलॉइडोसिस को आनुवंशिक, प्राथमिक और माध्यमिक में विभाजित किया गया था, और अंत में, 1993 में, डब्ल्यूएचओ वर्गीकरण को अपनाया गया था, जो कि विशिष्टता के आधार पर था। मुख्य तंतुमय अमाइलॉइड प्रोटीन।
हमारे देश में, एमिलॉयडोसिस के बारे में विचारों के विकास में एक महान योगदान ई। एम। तारीव, आई। ई। तारीवा, वी। वी। सेरोव द्वारा किया गया था। अमाइलॉइडोसिस और आवधिक बीमारी के प्राथमिक और आनुवंशिक रूपों के अध्ययन में एक बड़ी भूमिका ओ। एम। विनोग्रादोवा की है, जिनके मोनोग्राफ, 1973 और 1980 में प्रकाशित हुए, आज उनकी प्रासंगिकता नहीं खोई है।
वर्तमान में, अमाइलॉइडोसिस को चिकित्सकीय रूप से प्रणालीगत और स्थानीय रूपों में विभाजित किया गया है। प्रणालीगत रूपों में, फाइब्रिलर जमा की संरचना के आधार पर, चार प्रकार होते हैं ( ).
अमाइलॉइडोसिस के स्थानीय रूपों में वर्तमान में अल्जाइमर रोग (ए-बीटा, फाइब्रिल में मस्तिष्क में जमा β-प्रोटीन होता है), अग्नाशयी आइलेट्स का अमाइलॉइडोसिस, संभवतः टाइप 2 मधुमेह के साथ रोगजनक संबंध होने, अंतःस्रावी ट्यूमर में होने वाले एमाइलॉयडोसिस, एमाइलॉयड ट्यूमर शामिल हैं। त्वचा, नासोफेरींजल क्षेत्र, मूत्राशय और अन्य दुर्लभ प्रकार।
एएल अमाइलॉइडोसिस
AL-amyloidosis का विकास मल्टीपल मायलोमा, Waldenström की बीमारी, B-सेल लिम्फोमा में संभव है, और यह प्राथमिक amyloidosis में अज्ञातहेतुक हो सकता है। ये सभी प्रकार एक सामान्य रोगजनन द्वारा एकजुट होते हैं, प्राथमिक अमाइलॉइडोसिस एक हेमटोलॉजिकल रोग के स्पष्ट संकेतों की अनुपस्थिति के कारण पहचानना सबसे कठिन है, इसलिए यह इस रूप पर विस्तार से रहने लायक है।
प्राथमिक अमाइलॉइडोसिस में, मल्टीपल मायलोमा से संबंधित एक सौम्य प्लाज्मा सेल डिस्क्रेसिया, असामान्य अस्थि मज्जा प्लाज्मा सेल क्लोन अमाइलॉइडोजेनिक इम्युनोग्लोबुलिन का उत्पादन करते हैं। इन इम्युनोग्लोबुलिन की प्रकाश श्रृंखलाओं के चर क्षेत्रों में कुछ अमीनो एसिड एक असामान्य स्थिति पर कब्जा कर लेते हैं, जो उनकी अस्थिरता की ओर जाता है और फाइब्रिलोजेनेसिस की प्रवृत्ति का कारण बनता है। प्राथमिक अमाइलॉइडोसिस वाले रोगियों में, अस्थि मज्जा में प्लाज्मा कोशिकाओं की सामग्री 5-10% तक बढ़ जाती है (आमतौर पर 4% से कम, मल्टीपल मायलोमा के साथ - 12% से अधिक), और वे इम्युनोग्लोबुलिन प्रकाश श्रृंखलाओं का एक निश्चित आइसोटाइप उत्पन्न करते हैं, जो इम्यूनोहिस्टोकेमिकल धुंधला में प्रमुख है। प्रमुख लैम्ब्डा या (कम सामान्यतः) कप्पा आइसोटाइप की मुक्त मोनोक्लोनल प्रकाश श्रृंखलाएं रक्त और मूत्र में पाई जाती हैं, लेकिन उनकी सामग्री मल्टीपल मायलोमा की तुलना में कम होती है।
प्राथमिक अमाइलॉइडोसिस की नैदानिक तस्वीर विविध है और रोग प्रक्रिया में कुछ अंगों की प्रमुख भागीदारी से निर्धारित होती है - हृदय, गुर्दे, तंत्रिका तंत्र, जठरांत्र संबंधी मार्ग, यकृत, आदि। पहले लक्षण कमजोरी और वजन घटाने हैं, लेकिन इस पर चरण, अंग के लक्षणों की उपस्थिति से पहले, निदान अत्यंत दुर्लभ है।
AL amyloidosis में सबसे आम लक्षित अंग गुर्दे और हृदय हैं। गुर्दे की क्षति नेफ्रोटिक सिंड्रोम द्वारा प्रकट होती है, लगातार और पुरानी गुर्दे की विफलता की शुरुआत के साथ, हेमट्यूरिया और धमनी उच्च रक्तचाप विशिष्ट नहीं हैं।
मायोकार्डियम में अमाइलॉइड के जमाव के साथ, विभिन्न प्रकार की लय गड़बड़ी विकसित होती है, प्रगतिशील हृदय विफलता, जो दांतों के वोल्टेज में कमी के रूप में ईसीजी पर स्पर्शोन्मुख परिवर्तनों से पहले हो सकती है। इकोकार्डियोग्राफी से बाएं और दाएं वेंट्रिकल की दीवारों का गाढ़ा मोटा होना, हृदय गुहाओं की मात्रा में कमी, इजेक्शन अंश में मामूली कमी और बाएं वेंट्रिकुलर मायोकार्डियम की डायस्टोलिक शिथिलता का पता चलता है।
अक्सर तंत्रिका तंत्र की भागीदारी के लक्षण होते हैं - स्वायत्त, ऑर्थोस्टेटिक हाइपोटेंशन के रूप में, और परिधीय - संवेदनशीलता विकारों के रूप में। हाल के वर्षों में, केंद्रीय तंत्रिका तंत्र के घावों का भी वर्णन किया गया है, हालांकि पहले यह माना जाता था कि वे प्राथमिक अमाइलॉइडोसिस की विशेषता नहीं थे।
अपच संबंधी घटना (पूर्णता, कब्ज, दस्त की भावना) और malabsorption सिंड्रोम स्वायत्त तंत्रिका तंत्र को नुकसान और जठरांत्र संबंधी मार्ग के अमाइलॉइडोसिस दोनों के कारण हो सकते हैं। हेपेटोमेगाली बहुत विशेषता है, जिसकी प्रकृति को हृदय की विफलता और अमाइलॉइड यकृत क्षति के कारण भीड़ के बीच विभेदित किया जाना चाहिए। उत्तरार्द्ध की पुष्टि रक्त सीरम में क्षारीय फॉस्फेट के स्तर में वृद्धि से होती है। प्लीहा अक्सर प्रभावित होता है, लेकिन स्प्लेनोमेगाली हमेशा नहीं पाई जाती है और इसका बहुत बड़ा नैदानिक महत्व नहीं है।
मैक्रोग्लोसिया, प्राथमिक अमाइलॉइडोसिस का एक क्लासिक संकेत, 20% रोगियों में होता है; नरम ऊतक घुसपैठ से मांसपेशियों और त्वचा शोष, नाखून डिस्ट्रोफी, खालित्य, और ट्यूमर जैसी संरचनाओं की उपस्थिति हो सकती है - एमाइलॉयड।
संवहनी क्षति कम आम है, जिसके लक्षण पेरिऑर्बिटल पुरपुरा हैं - "रैकून आंखें" और इकोस्मोसिस। रक्तस्राव हो सकता है, जिसमें मूत्राशय से रक्तस्राव भी शामिल है, जो संवहनी दीवार में परिवर्तन और जमावट प्रणाली के उल्लंघन के कारण होता है, मुख्य रूप से कारक एक्स की कमी, जो एमाइलॉयड से बांधता है। यह जमावट कारकों की कमी से एमाइलॉयडोसिस की थ्रोम्बोसाइटोसिस विशेषता की व्याख्या करने के लिए प्रथागत है।
पल्मोनरी अमाइलॉइडोसिस अक्सर केवल शव परीक्षा में पाया जाता है। हालांकि, कुछ मामलों में, सांस की तकलीफ, हेमोप्टाइसिस और हाइड्रोथोरैक्स न केवल हृदय की विफलता और नेफ्रोटिक सिंड्रोम के कारण हो सकते हैं, बल्कि अमाइलॉइड फेफड़ों की बीमारी के कारण भी हो सकते हैं। एल्वियोली में अमाइलॉइड का जमाव और फुफ्फुसीय अमाइलॉइडोमा का विकास संभव है। रेडियोग्राफिक रूप से, फेफड़े के ऊतकों में जाली और गांठदार परिवर्तनों का पता लगाया जा सकता है।
अधिवृक्क भागीदारी से अधिवृक्क अपर्याप्तता हो सकती है, जो अक्सर अपरिचित हो जाती है क्योंकि हाइपोटेंशन और हाइपोनेट्रेमिया को हृदय की विफलता और स्वायत्त तंत्रिका तंत्र क्षति के लक्षणों के रूप में देखा जाता है। 10-20% रोगियों में, हाइपोथायरायडिज्म थायरॉयड क्षति की अभिव्यक्ति के रूप में हो सकता है, अक्सर सबमांडिबुलर लार ग्रंथियों में वृद्धि होती है।
प्राथमिक अमाइलॉइडोसिस का निदान, संकेतित नैदानिक विशेषताओं के अलावा, जो माध्यमिक अमाइलॉइडोसिस में समान हो सकता है, कई प्रयोगशाला डेटा पर आधारित है। 85% रोगियों में, रक्त सीरम और मूत्र प्रोटीन के इम्यूनोइलेक्ट्रोफोरेसिस से मोनोक्लोनल इम्युनोग्लोबुलिन का पता चलता है। नियमित अध्ययनों में, वही मोनोक्लोनल इम्युनोग्लोबुलिन मूत्र में बेंस-जोन्स प्रोटीन के रूप में पाए जाते हैं। अस्थि मज्जा बायोप्सी मल्टीपल मायलोमा के साथ एक विभेदक निदान की अनुमति देता है, साथ ही इम्यूनोहिस्टोकेमिकल धुंधला द्वारा प्लाज्मा कोशिकाओं की संख्या और उनकी मोनोक्लोनलिटी में मध्यम वृद्धि का पता लगाता है।
हालांकि, यहां तक कि एक विशिष्ट नैदानिक तस्वीर का संयोजन और मोनोक्लोनल प्लाज्मा कोशिकाओं और प्रोटीन की उपस्थिति अभी भी प्राथमिक अमाइलॉइडोसिस के निदान की पुष्टि करने के लिए अपर्याप्त है। बायोप्सी डेटा यहां निर्णायक भूमिका निभाते हैं। कम से कम आक्रामक पूर्वकाल पेट की दीवार के चमड़े के नीचे के वसायुक्त ऊतक की आकांक्षा है, जो AL-amyloidosis में 80-90% सकारात्मक परिणाम देता है (इस विधि का अभी तक हमारे देश में उपयोग नहीं किया गया है)। मसूड़ों और रेक्टल म्यूकोसा की बायोप्सी का एक निश्चित नैदानिक मूल्य होता है, लेकिन सकारात्मक परिणामों का प्रतिशत प्रक्रिया के चरण के आधार पर व्यापक रूप से भिन्न होता है, इसलिए प्रभावित अंगों में से एक - गुर्दे, यकृत की बायोप्सी करने की सलाह दी जाती है। दिल, जो एमाइलॉयडोसिस एएल टाइप में लगभग 100% सकारात्मक परिणाम देता है।
सबसे पहले, बायोप्सी सामग्री कांगो लाल रंग से सना हुआ है। यदि अध्ययन के तहत सामग्री के कांगोफिलिया का पता चला है, तो इसका ध्रुवीकृत प्रकाश में अध्ययन करना आवश्यक है, द्विअर्थी प्रभाव केवल अमाइलॉइड के लिए विशेषता है, अन्य कांगोफिलिक पदार्थ एक सेब-हरा रंग प्राप्त नहीं करते हैं। उसके बाद, अमाइलॉइड टाइपिंग वांछनीय है। अमाइलॉइड अग्रदूत प्रोटीन के लिए मोनोक्लोनल एंटीबॉडी का उपयोग करके सबसे सटीक इम्यूनोहिस्टोकेमिकल विधि है। हालाँकि, वर्तमान में हमारे देश में यह व्यावहारिक रूप से अनुपलब्ध है। इसलिए, निदान के लिए क्षारीय गुआनिडीन या पोटेशियम परमैंगनेट के समाधान के साथ धुंधला हो जाना उपयोग किया जाता है, जो अप्रत्यक्ष रूप से, फाइब्रिलर जमा के प्रकार को निर्धारित करने की अनुमति देता है।
प्राथमिक अमाइलॉइडोसिस के लिए रोग के अन्य रूपों की तुलना में खराब है, औसत जीवन प्रत्याशा दो साल से अधिक नहीं है, उपचार के बिना हृदय रोग या मल्टीसिस्टम घावों की उपस्थिति में, कुछ महीनों के भीतर रोगियों की मृत्यु हो जाती है। मृत्यु के सबसे आम कारण हृदय और गुर्दे की विफलता, सेप्सिस, संवहनी जटिलताओं और कैशेक्सिया हैं। मल्टीपल मायलोमा के साथ रोगजनक समानता हमें कीमोथेरेपी के दौरान रोग की प्रगति के अवरोध पर भरोसा करने की अनुमति देती है, जो मोनोक्लोनल प्लाज्मा कोशिकाओं को दबाने के लिए किया जाता है। कई उपचार आहार हैं ()।
सफल उपचार के मामले में कीमोथेरेपी के उपयोग से रोगियों की जीवन प्रत्याशा 10 से 18 महीने तक बढ़ सकती है। लेकिन चिकित्सा की प्रभावशीलता कम है, विशेष रूप से, इस तथ्य के कारण कि कई मामलों में रोग की प्रगति उपचार के पूरा होने से पहले रोगियों की मृत्यु की ओर ले जाती है, साथ ही साइटोपेनिया के विकास के कारण, संक्रामक जटिलताओं, डेक्साज़ोन की अति-उच्च खुराक के साथ उपचार में घातक अतालता। ऑटोलॉगस स्टेम कोशिकाओं के प्रत्यारोपण के साथ मेलफोलन की उच्च खुराक का उपयोग 50% से अधिक मामलों में छूट प्राप्त करने की अनुमति देता है, हालांकि, इस पद्धति का उपयोग स्थिति की गंभीरता, रोगियों की आयु और कार्यात्मक विकारों द्वारा सीमित है। दिल और गुर्दे। कई मामलों में, केवल रोगसूचक सहायक चिकित्सा संभव है।
एए अमाइलॉइडोसिस
एए-एमिलॉयडोसिस का विकास पुरानी सूजन प्रक्रियाओं के दौरान होता है, एए-एमिलॉयड के अग्रदूत सीरम तीव्र-चरण प्रोटीन होते हैं, विभिन्न प्रकार की कोशिकाओं द्वारा उत्पादित α-ग्लोब्युलिन, मुख्य रूप से न्यूट्रोफिल और फाइब्रोब्लास्ट। माध्यमिक अमाइलॉइडोसिस संधिशोथ, बेचटेरू रोग, सोरियाटिक गठिया, विभिन्न ट्यूमर, हॉजकिन रोग, अल्सरेटिव कोलाइटिस और क्रोहन रोग, आवधिक बीमारी (पारिवारिक भूमध्य बुखार), साथ ही तपेदिक, अस्थिमज्जा का प्रदाह, ब्रोन्किइक्टेसिस में विकसित होता है।
एए अमाइलॉइडोसिस की विशेषता नैदानिक विशेषताएं अधिकांश रोगियों में गुर्दे की क्षति है, साथ ही यकृत और / या प्लीहा (लगभग 10%) और हृदय (केवल इकोकार्डियोग्राफी द्वारा पता लगाया गया) को अपेक्षाकृत दुर्लभ क्षति है। मैक्रोग्लोसिया माध्यमिक अमाइलॉइडोसिस के लिए विशिष्ट नहीं है। निदान वृक्क अमाइलॉइडोसिस और एक पुरानी सूजन की बीमारी के संयोजन पर आधारित है, जिसकी पुष्टि बायोप्सी सामग्री के इम्यूनोहिस्टोकेमिकल धुंधला होने से होती है; हमारे देश में, पहले से ही ऊपर बताए गए अप्रत्यक्ष धुंधला तरीकों का उपयोग किया जाता है।
रोग का निदान काफी हद तक अंतर्निहित बीमारी की प्रकृति पर निर्भर करता है; एक प्राकृतिक पाठ्यक्रम में, प्रोटीनूरिया का पता लगाने के 5 साल बाद एक तिहाई रोगियों में गुर्दे की विफलता विकसित होती है। आवधिक बीमारी के साथ, पांच साल की जीवित रहने की दर 25% है।
उपचार फोकस के दमन पर आधारित है - सीरम अग्रदूत प्रोटीन के उत्पादन का स्रोत। ट्यूमर को हटाना, सीक्वेस्ट्रेक्टोमी, आंत्र का उच्छेदन, तपेदिक का उपचार, रुमेटीइड गठिया की गतिविधि में कमी (साइटोस्टैटिक्स के उपयोग के साथ) अमाइलॉइडोसिस की प्रगति की समाप्ति की ओर ले जाती है, और कभी-कभी नैदानिक अभिव्यक्तियों के विपरीत विकास के लिए, विशेष रूप से नेफ्रोटिक में सिंड्रोम।
आवधिक बीमारी में कोल्सीसिन का उपयोग पसंद की विधि है, इसकी प्रभावशीलता सिद्ध हो चुकी है, उपचार अमाइलॉइडोसिस के विकास को रोकता है और इसकी प्रगति को धीमा कर देता है। माध्यमिक अमाइलॉइडोसिस के अन्य रूपों में, कोल्सीसिन की प्रभावशीलता की पुष्टि नहीं की गई है।
प्रणालीगत अमाइलॉइडोसिस के पुराने और वंशानुगत रूप, साथ ही साथ स्थानीय रूप, दुर्लभ हैं, डायलिसिस अमाइलॉइडोसिस विशेषज्ञों के लिए अच्छी तरह से जाना जाता है, सामान्य व्यवहार में यह लगभग कभी सामने नहीं आता है।
रोगसूचक चिकित्सा अमाइलॉइडोसिस के प्रकार पर निर्भर नहीं करती है, बल्कि प्रभावित लक्षित अंगों पर निर्भर करती है ( ).
अमाइलॉइडोसिस, विशेष रूप से प्राथमिक, को एक दुर्लभ विकृति माना जाता है, लेकिन वास्तव में यह इतना दुर्लभ नहीं है क्योंकि इसका निदान करना मुश्किल है। पर्याप्त निदान के लिए न केवल इस बीमारी के क्लिनिक और रोगजनन के ज्ञान की आवश्यकता होती है, बल्कि कुछ नैदानिक क्षमताओं की उपलब्धता भी होती है। इस बिंदु को स्पष्ट करने के लिए, हम अपना स्वयं का डेटा प्रस्तुत करते हैं ( ) 1993-2003 में मास्को सिटी क्लिनिकल अस्पताल के नेफ्रोलॉजी विभाग में एस.पी. बोटकिन के नाम पर। 88 रोगियों को देखा गया जिन्हें एमाइलॉयडोसिस का निदान किया गया था।
एएल-एमाइलॉयडोसिस, सेनील और अनिर्दिष्ट अमाइलॉइडोसिस वाले सभी रोगियों में निदान की पुष्टि की गई थी, और माध्यमिक अमाइलॉइडोसिस वाले 30 रोगियों में - कुल 53 मामले। 12 रोगियों में गुर्दे की बायोप्सी की गई, 2 रोगियों में यकृत की बायोप्सी की गई, 8 रोगियों में आंतों की बायोप्सी की गई, 12 मामलों में मसूड़ों का प्रदर्शन किया गया और 19 मामलों में अनुभागीय सामग्री की रूपात्मक परीक्षा द्वारा निदान की पुष्टि की गई।
ज्यादातर मामलों में, नेफ्रोलॉजी विभाग में एक परीक्षा के परिणामस्वरूप पहली बार अमाइलॉइडोसिस का निदान स्थापित किया गया था। हमने AL-amyloidosis के रोगियों के बीच रेफरल और नैदानिक निदान की तुलना की ( ).
20 (10%) में से केवल दो मामलों में, रेफरल निदान "प्राथमिक अमाइलॉइडोसिस" था, और इन रोगियों में से एक में यह चिकित्सा और व्यावसायिक रोगों के लिए एमएमए क्लिनिक में और दूसरे में एक विदेशी क्लिनिक में किया गया था।
एएल-एमाइलॉयडोसिस के विकास के साथ कई मायलोमा का निदान करने वाले सभी रोगियों को हेमेटोलॉजी विभागों में स्थानांतरित कर दिया गया था। प्राथमिक अमाइलॉइडोसिस वाले 11 रोगियों में से, सात रोगियों को मेलफोलन और मौखिक प्रेडनिसोलोन के संयोजन के साथ आंतरायिक कीमोथेरेपी प्राप्त हुई, उनमें से चार डायलिसिस उपचार के संयोजन में, और एक अन्य रोगी को केवल डायलिसिस और रोगसूचक उपचार मिला। इन रोगियों में से, उपचार शुरू होने से दो सप्ताह से दो साल के भीतर पांच की मृत्यु हो गई (सभी गुर्दे की विफलता और कई अंग क्षति के साथ), एक रोगी डायलिसिस पर है, एक रोगी को ऑटोलॉगस स्टेम सेल प्रत्यारोपण के लिए भेजा गया था, और एक रोगी उपचार प्राप्त कर रहा है। वर्तमान काल तक। एक रोगी में, लंबे समय तक गैर-स्कारिंग गैस्ट्रिक अल्सर की उपस्थिति के कारण कीमोथेरेपी में देरी हुई, और दो और रोगियों ने इलाज से इनकार कर दिया।
हमारे अध्ययन में माध्यमिक अमाइलॉइडोसिस वाले रोगियों में, रुमेटीइड गठिया के रोगी प्रबल थे, कारणों में दूसरे स्थान पर क्रोनिक ऑस्टियोमाइलाइटिस और सोरियाटिक गठिया थे, अन्य रोग कम आम थे ( ).
रुमेटीइड गठिया और सोरियाटिक गठिया का उपचार साइटोस्टैटिक्स (मेटाट्रेक्सेट, एज़ैथियोप्रिन) के उपयोग के साथ किया गया था, हालांकि कई मामलों में सीआरएफ और कॉमरेडिडिटी की उपस्थिति के कारण चिकित्सा की संभावनाएं सीमित थीं। पुरानी ऑस्टियोमाइलाइटिस वाले मरीजों को प्युलुलेंट सर्जरी के विभागों में भेजा गया था। बेचटेरू रोग और क्रोहन रोग के रोगियों को विशिष्ट उपचार प्राप्त हुआ, सीओपीडी और तपेदिक के रोगियों को भी विशेष अस्पतालों में भेजा गया। पेट के ट्यूमर वाले रोगियों में से एक का सफलतापूर्वक ऑपरेशन किया गया था, और चार वर्षों के अवलोकन के दौरान, नेफ्रोटिक सिंड्रोम धीरे-धीरे वापस आ गया, ट्यूमर के अन्य मामलों में, प्रक्रिया की व्यापकता ने केवल रोगसूचक उपचार की अनुमति दी, रोगी के साथ लिम्फोग्रानुलोमैटोसिस को एक टर्मिनल अवस्था में भर्ती कराया गया था। माध्यमिक अमाइलॉइडोसिस वाले रोगियों में मृत्यु दर 38% थी (निदान के समय उन्नत घावों वाले रोगियों के कारण)। आवधिक बीमारी वाले सभी रोगियों को कोल्सीसिन थेरेपी मिली।
प्राथमिक अमाइलॉइडोसिस के उपचार के आधुनिक तरीकों के निदान और अनुप्रयोग की विशेषताओं को निम्नलिखित उदाहरण द्वारा चित्रित किया जा सकता है: रोगी के।, 46 वर्ष, को पहली बार अक्टूबर 2002 के अंत में पैरों में सूजन, धड़कन, एमेनोरिया की शिकायत के साथ अस्पताल में भर्ती कराया गया था। उसे सर्दी, एपेंडेक्टोमी, दो सामान्य अत्यावश्यक प्रसव, गुर्दे की बीमारी के संकेत और कोई पुरानी बीमारी नहीं है। अप्रैल 2002 में, वह दाहिने फेफड़े के ऊपरी लोब में तीव्र निमोनिया से पीड़ित थी, एक आउट पेशेंट के आधार पर इलाज किया गया था, अबैक्टल और लिनकोमाइसिन के इंजेक्शन प्राप्त किए थे। निमोनिया के स्थानीयकरण के कारण, एक तपेदिक औषधालय में उसकी जांच की गई, तपेदिक के निदान को बाहर रखा गया था। जून की शुरुआत में, पहली बार पैरों पर एडिमा दिखाई दी, जिसके लिए उसकी जांच नहीं की गई थी। एडिमा थोड़े समय के बाद स्वतंत्र रूप से समाप्त हो गई, फिर फिर से शुरू हो गई। रोगी को एक चिकित्सीय अस्पताल में भर्ती कराया गया था, परीक्षा में 1.65% तक प्रोटीनमेह, हाइपोप्रोटीनेमिया (कुल सीरम प्रोटीन 52 ग्राम / लीटर), रक्तचाप सामान्य (120/80 मिमी एचजी), मूत्र तलछट अपरिवर्तित, क्रिएटिनिन प्लाज्मा स्तर भी थे। सामान्य सीमा के भीतर। "तीव्र ग्लोमेरुलोनेफ्राइटिस" का निदान स्थापित किया गया था, एम्पीसिलीन, झंकार, हेपरिन, ट्रायमपुर के साथ उपचार किया गया था, टॉन्सिल्लेक्टोमी किया गया था। प्रोटीनुरिया बना रहा, एडिमा धीरे-धीरे बढ़ गई, और इसलिए, आगे की जांच और उपचार के लिए, क्रोनिक ग्लोमेरुलोनेफ्राइटिस के निदान वाले रोगी को अस्पताल भेजा गया। एस पी बोटकिन।
जांच करने पर, त्वचा साफ होती है, सामान्य रंग की, अनासारका, सूजन बड़े पैमाने पर, घनी होती है, जलोदर निर्धारित होता है, परिधीय लिम्फ नोड्स बढ़े हुए नहीं होते हैं। बीपी 110/70 मिमी एचजी। कला।, हृदय की ध्वनियाँ सुरीली, स्पष्ट, लयबद्ध होती हैं, हृदय गति 90 बीट / मिनट होती है, यकृत और प्लीहा बढ़े हुए नहीं होते हैं, डायरिया 1000 मिली / दिन तक होता है, मल नियमित होता है, बिना रोग संबंधी अशुद्धियों के। परीक्षा में नेफ्रोटिक सिंड्रोम का पता चला - प्रोटीनुरिया 3 ग्राम / लीटर, मूत्र तलछट कम, हाइपोडिस्प्रोटीनमिया, हाइपरलिपिडिमिया (कुल सीरम प्रोटीन 39 ग्राम / लीटर, एल्ब्यूमिन 12 ग्राम / लीटर, ग्लोब्युलिन 7-30-15-19%, क्रमशः α 1 -α 2 -β-γ कोलेस्ट्रॉल 17.8 mmol/l, β-lipoproteins 250 U), बेंस-जोन्स प्रोटीन के लिए मूत्र का विश्लेषण करते समय, प्रतिक्रिया नकारात्मक होती है, 17-KS का दैनिक उत्सर्जन कम नहीं होता है। नैदानिक रक्त परीक्षण और अन्य जैव रासायनिक पैरामीटर सामान्य सीमा के भीतर हैं, कोगुलोग्राम - गंभीर हाइपरफिब्रिनोजेनमिया, आरकेएफएम स्तर में वृद्धि। रक्त इम्युनोग्लोबुलिन का अध्ययन: Ig-A - 0.35, Ig-M - 35.7 (दो मानदंड), Ig-G - 1.96 g / l। छाती का एक्स-रे, खोपड़ी और श्रोणि की हड्डियां, उदर गुहा का अल्ट्रासाउंड, गुर्दे, थायरॉयड ग्रंथि, पैथोलॉजी के बिना ईसीएचओ-केजी, छोटे श्रोणि का अल्ट्रासाउंड - गर्भाशय शरीर के एडेनोमायोसिस के संकेत, एंडोस्कोपी - भाटा ग्रासनलीशोथ, जीर्ण जठरशोथ। जब एक न्यूरोपैथोलॉजिस्ट द्वारा जांच की गई, तो कोई विकृति नहीं मिली; एक ऑन्कोलॉजिस्ट ने फाइब्रोसिस्टिक मास्टोपाथी का निदान किया।
अल्ट्रासाउंड मार्गदर्शन के तहत स्थानीय संज्ञाहरण के तहत नेफ्रोटिक सिंड्रोम की उत्पत्ति को स्पष्ट करने के लिए, दाहिने गुर्दे की एक सुई-सुई पंचर बायोप्सी की गई; कोई जटिलता नहीं थी। ग्लोमेरुली के मेसेंजियम और एक्स्ट्राग्लोमेरुलर वाहिकाओं में बायोप्सी के अध्ययन में, अमाइलॉइड का जमाव नोट किया जाता है। अमाइलॉइड ग्लोमेरुलर वैस्कुलर लूप्स के 25% तक लोड करता है। इम्यूनोहिस्टोकेमिकल अध्ययन ने विशिष्ट ल्यूमिनेसिसेंस को प्रकट नहीं किया। जब तैयारी को 2 घंटे के लिए एक क्षारीय गुआनिडीन समाधान के साथ इलाज किया जाता है, तो कॉन्गोफिलिया और उनके गुणों को ध्रुवीकृत प्रकाश में संरक्षित किया जाता है, जो कि एएल-एमाइलॉयडोसिस के लिए विशिष्ट है।
एएल-एमिलॉयडोसिस की प्रकृति को स्पष्ट करने के लिए, इम्यूनोटेस्ट प्रयोगशाला में रक्त और मूत्र का एक इम्यूनोकेमिकल अध्ययन किया गया था। एम-लैम्ब्डा पैराप्रोटीनेमिया पॉलीक्लोनल इम्युनोग्लोबुलिन के स्तर में कमी और बड़े पैमाने पर गैर-चयनात्मक प्रोटीनूरिया की पृष्ठभूमि के खिलाफ बेंस-जोन्स लैम्ब्डा-प्रकार पैराप्रोटीनुरिया के साथ प्रकट हुआ था। रोगी को एक हेमटोलॉजिस्ट द्वारा परामर्श दिया गया था, यह सुझाव दिया गया था कि वाल्डेनस्ट्रॉम की बीमारी मौजूद थी, और एक अस्थि मज्जा ट्रेफिन बायोप्सी की गई थी। निष्कर्ष: मौजूदा अस्थि मज्जा गुहाओं में, सामान्य हेमटोपोइजिस के सभी तीन स्प्राउट्स की कोशिकाएं दिखाई देती हैं, साथ ही लिम्फोइड कोशिकाएं जो क्लस्टर नहीं बनाती हैं। अस्थि मज्जा के लिम्फोइड घुसपैठ की अनुपस्थिति, बढ़े हुए लिम्फ नोड्स और प्लीहा, और ट्यूमर सब्सट्रेट की अनुपस्थिति के कारण वाल्डेनस्ट्रॉम रोग का निदान खारिज कर दिया गया था।
गुर्दे की क्षति, नेफ्रोटिक सिंड्रोम, संरक्षित गुर्दे समारोह के साथ प्राथमिक अमाइलॉइडोसिस का निदान स्थापित किया गया था, अन्य अंग क्षति के कोई संकेत नहीं पाए गए थे। जनवरी 2003 से, कीमोथेरेपी को मेलफोलन 16 मिलीग्राम / दिन और प्रेडनिसोलोन 100 मिलीग्राम / दिन, हर छह सप्ताह में चार दिनों के पाठ्यक्रम के साथ शुरू किया गया था। रोगसूचक उपचार भी किया जाता है: फ़्यूरोसेमाइड, वर्शपिरोन, पोटेशियम की तैयारी, फैमोटिडाइन, एल्ब्यूमिन आधान। आज तक, कीमोथेरेपी के पांच पाठ्यक्रम अच्छी सहनशीलता के साथ किए गए हैं, एडिमा में कमी आई है, प्रोटीनुरिया घटकर 1.8 ग्राम / लीटर हो गया है, हाइपोडिस्प्रोटीनेमिया की गंभीरता थोड़ी कम हो गई है (कुल प्रोटीन 46 ग्राम / लीटर, एल्ब्यूमिन 18 ग्राम / एल, α 2-ग्लोबुलिन 20%)। गुर्दा का कार्य बरकरार रहता है, प्लाज्मा क्रिएटिनिन 1.3 मिलीग्राम / डीएल है, नियंत्रण गतिशील परीक्षाओं के दौरान अन्य अंगों और प्रणालियों को नुकसान का कोई संकेत नहीं मिला।
यह मामला स्पष्ट रूप से इस तथ्य को दर्शाता है कि अमाइलॉइडोसिस के निदान के लिए रूपात्मक, प्रतिरक्षाविज्ञानी और प्रतिरक्षा रासायनिक परीक्षाएं आवश्यक हैं। इस प्रकार, हमारे रोगी में, सबसे स्पष्ट नैदानिक निदान "क्रोनिक ग्लोमेरुलोनेफ्राइटिस" था, और गुर्दे की बायोप्सी करने की संभावना के अभाव में, यह निदान सबसे अधिक संभावना है। आईजी-एम के स्तर में वृद्धि के अपवाद के साथ, रोगी के पास रोग की एक प्रणालीगत प्रकृति, एक पुरानी सूजन प्रक्रिया, रक्त प्रणाली की बीमारी का कोई नैदानिक संकेत नहीं था। और केवल गुर्दे की बायोप्सी के अध्ययन में प्राप्त आंकड़ों के परिणामस्वरूप अस्थि मज्जा की एक ट्रेपैनोबायोप्सी और एक इम्यूनोकेमिकल अध्ययन हुआ, जिसने एक साथ प्रणालीगत क्षति की उपस्थिति से पहले प्राथमिक अमाइलॉइडोसिस का निदान करना संभव बना दिया। रोगजनक चिकित्सा शुरू की गई थी, हालांकि पहले से विकसित नेफ्रोटिक सिंड्रोम की पृष्ठभूमि के खिलाफ, लेकिन गुर्दे की विफलता की शुरुआत से पहले और केवल 25% ग्लोमेरुली के साथ एमिलॉयड से भरा हुआ था, जो अपेक्षाकृत अनुकूल रूप से अनुकूल है।
अंत में, हम ध्यान दें कि अमाइलॉइडोसिस एक उच्च मृत्यु दर के साथ एक गंभीर बीमारी है, जिसका निदान करना बेहद मुश्किल है, हालांकि, रोगियों की समय पर और उच्च गुणवत्ता वाली जांच से पहले निदान करना संभव हो जाता है, और पर्याप्त चिकित्सा का समय पर प्रशासन संभव हो जाता है। बारी, इस अवधि में रोग का निदान में सुधार करना संभव बनाता है रोगियों का समूह।
साहित्य
- Varshavsky V. A., Proskurneva E. P. आधुनिक चिकित्सा में अमाइलॉइडोसिस के रूपात्मक निदान का महत्व और तरीके // प्रैक्टिकल नेफ्रोलॉजी। - 1998. - 2:16-23।
- विनोग्रादोवा ओएम एमाइलॉयडोसिस के प्राथमिक और आनुवंशिक रूप। - एम .: मेडिसिन, 1980।
- ज़खारोवा ई.वी., ख्रीकिना ए.वी., प्रोस्कुर्नेवा ई.पी., वार्शवस्की वी.ए. प्राथमिक अमाइलॉइडोसिस का मामला: निदान और उपचार में कठिनाइयाँ // नेफ्रोलॉजी और डायलिसिस। - 2002. - 1:54-61।
- रामीव वीवी एए और एएल-एमाइलॉयडोसिस में गुर्दे की क्षति की ख़ासियत: डिस ... कैंड। शहद। विज्ञान। - एम।, 2003।
- Kozlovskaya L. V., Varshavsky V. A., Chegaeva T. V. et al। अमाइलॉइडोसिस: समस्या पर एक आधुनिक दृष्टिकोण // प्रैक्टिकल नेफ्रोलॉजी। - 1998. - 2:24-26।
- रॉडने एच।, रेमंड एलसी और स्किनर एम। // प्रणालीगत अमाइलॉइड्स; न्यू इंग्लैंड जर्नल ऑफ मेडिसिन, 1997. 337:898-909।
- धोडापकर एम.वी., जगन्नाथ एस., वेसोल डी. एट अल // डेक्सामेथासोन प्लस अल्फा इंटरफेरॉन / ल्यूक लिम्फोमा के साथ एएल-एमाइलॉयडोसिस का उपचार। 1997. - 27(3-4):351-365
- गर्ट्ज़ एम.ए., लैसी एम.क्यू., वासना जे.ए. एट सभी // पहले से इलाज किए गए इम्युनोग्लोबुलिन लाइट-चेन एमाइलॉयडोसिस के लिए उच्च-खुराक डेक्सामेथासोन का चरण II परीक्षण। एम जे हेमटोल, 1999,61(2):115-119।
- गर्ट्ज़ एमए, लैसी एम।, क्यू।, वासना जे.ए. एट अल // प्राथमिक सिस्टेनिक अमाइलॉइडोसिस वाले अनुपचारित रोगियों के उच्च खुराक डेक्सामेथासोन का द्वितीय चरण परीक्षण। मेड ऑनकोल 1999.-16(2):104-109
- Sezer O., Schmid P., Shweigert M. et al // VAD के बाद प्राथमिक प्रणालीगत AL amyloidosis के कारण नेफ्रोटिक सिंड्रोम का रैपिड रिवर्सल और बाद में ऑटोलॉगस स्टेम सेल सपोर्ट के साथ उच्च खुराक कीमोथेरेपी। अस्थि मज्जा प्रत्यारोपण। 1999. - 23(9): 967-969।
- सेज़र ओ।, निमोलर के।, जैकब सी। एट अल // प्राथमिक अमाइलॉइडोसिस के उपचार के लिए उपन्यास दृष्टिकोण। एक्सपर्ट ओपिन इन्वेस्टिग ग्रग्स। 2000. - 9(10):2343-2350
- Sezer O., Eucker J., Jakob C., Possinger K. // AL amyloidosis का निदान और उपचार। क्लिनिक नेफ्रोल। 2000.-53(6):417-423।
- स्किनर एम। "एमाइलॉयडोसिस" एलर्जी, इम्यूनोलॉजी और रुमेटोलॉजी में करंट थेरेपी। मोस्बी-ईयर बुक। 1996. - 235-240।
- पल्लादिनी जी।, अनेसी ई।, परफेटी वी। एट अल। प्राथमिक प्रणालीगत (एएल) अमाइलॉइडोसिस के लिए एक संशोधित उच्च खुराक डेक्सामेथासोन आहार। हेमेटोलॉजी के ब्रिटिश जर्नल। 2001.-113:1044-1046।
ई. वी. ज़खारोवा
मॉस्को सिटी क्लिनिकल अस्पताल। एस. पी. बोटकिना
तालिका 2. प्राथमिक अमाइलॉइडोसिस के लिए उपचार के नियम
- मेलफोलन (प्रति दिन शरीर के वजन का 0.15-0.25 मिलीग्राम/किलोग्राम) और प्रेडनिसोलोन (1.5-2.0 मिलीग्राम/किलोग्राम प्रति दिन) का चक्रीय मौखिक प्रशासन एक वर्ष के लिए हर चार से छह सप्ताह में चार से सात दिनों के लिए, एक कोर्स खुराक प्राप्त करने तक 600 मिलीग्राम . का
- तीन सप्ताह के लिए 4 मिलीग्राम / दिन की खुराक पर मेलफोलन का मौखिक उपयोग, फिर, दो सप्ताह के ब्रेक के बाद - 2-4 मिलीग्राम / दिन सप्ताह में चार दिन लगातार, जब तक कि 600 मिलीग्राम की एक कोर्स खुराक तक नहीं पहुंच जाती है, के साथ संयोजन में प्रेडनिसोलोन
- मेलफोलन की उच्च खुराक (दो दिनों के लिए शरीर की सतह के 100-200 मिलीग्राम / वर्ग मीटर) के अंतःशिरा प्रशासन के बाद ऑटोलॉगस स्टेम कोशिकाओं के प्रत्यारोपण के बाद
- चतुर्थ डेक्सामेथासोन 40 मिलीग्राम चार दिनों के लिए हर तीन सप्ताह में आठ चक्रों के लिए
- 35-दिन के चक्र के पहले-चौथे, 9-12वें और 17-20वें दिनों में 40 मिलीग्राम की खुराक पर डेक्सामेथासोन का अंतःशिरा प्रशासन, तीन से छह चक्र, इसके बाद 3- की खुराक पर ए-इंटरफेरॉन का उपयोग। सप्ताह में तीन बार 6 मिलियन यूनिट
- Vincristine-doxoribucin-dexamethasone (VAD) योजना

